Факты о Периодической системе химических элементов, которые вы не знали
Вы, вероятно, уже видели Периодическую таблицу элементов раньше. Возможно, она все еще является вам во снах, или, может быть, он канула для вас в небытие, будучи не более чем украшением стены класса, призванной сделать кабинет более солидным. Однако в этой системе, казалось бы, случайно расположенных ячеек есть нечто большее, чем кажется на первый взгляд.Периодическая таблица (или ПТ, поскольку эта статья будет периодически ссылаться на нее) и элементы, которые в ней описываются, имеют особенности, о которых вы, возможно, никогда не догадывались. От неправдоподобного происхождения до новых дополнений, вот десять фактов, которые вы, вероятно, не знаете о Периодической таблице элементов.
10. Менделееву помогли
Фото: Wikimedia
Периодическая таблица используется с 1869 года, когда ее создал бородатый Димитрий Менделеев. Большинство людей думают, что Менделеев был единственным, кто изобрел таблицу и стал гениальным химиком века. Тем не менее, его усилия поддержали несколько европейских ученых, которые внесли важный вклад, чтобы сделать эту колоссальную диаграмму элементов полной.
Менделеев, как и положено, широко известен как отец Периодической таблицы, но он не документировал каждый известный нам элемент.
9. Новые дополнения

Фото: IUPAC
Хотите верьте, хотите нет, но Периодическая таблица не сильно изменилась с 1950-х годов. Однако 2 декабря 2016 года были добавлены четыре новых элемента: нихоний (элемент 113), московий (элемент 115), теннесин (элемент 117) и оганесон (элемент 118). Эти новые дополнения были озвучены в июне 2016 года, но, чтобы их можно было официально добавить в ПТ, потребовалось пять месяцев анализа.
Каждый из этих элементов был назван в честь города или государства, в котором они были обнаружены, за исключением оганесона, который был назван в честь российского физика-ядерщика Юрия Оганесяна за его усилия по документированию этого элемента.
8. Нет буквы «J»

В английском алфавите есть 26 замечательных букв, и каждая из них не менее важна, чем предыдущая и последующая. Однако Менделеев смотрел на это иначе. Попробуйте угадать, какая несчастная буква ни разу не встречается в ПТ? Вот подсказка: произносите буквы и загибайте пальцы на руках, пока не загнете все (если у вас есть все десять). Угадали? Правильно, это буква «J», которой ни разу не появилась в ПТ.
Говорят, один в поле не воин? Тогда, возможно, J — самая одинокая буква. Однако вот забавный факт: буква «J» чаще всего используется в именах для мальчиков, начиная с 2000 года. Итак, «J» получает достаточно внимания, не переживайте.
7. Искусственные элементы

Фото: Popocatomar
Как вы только что узнали, в Периодической таблице теперь есть целых 118 элементов. Можете догадаться, сколько из этих 118 сделано человеком? Из 118 элементов 90 можно найти в красивом месте, которое мы называем природой.
Как 28 элементов могут быть искусственными? Это, действительно, так. Мы синтезировали элементы с 1937 года и продолжаем делать это и сейчас. Хорошая новость заключается в том, что ПТ удивительна, и эти искусственные элементы можно легко обнаружить, если вам когда-нибудь станет любопытно. Просто посмотрите на элементы с 93 по 118. Полное разоблачение: этот диапазон включает в себя несколько элементов, которые очень редко встречаются в природе и поэтому почти всегда создаются в лабораториях, что также верно для элементов 43, 61, 85 и 87.
6. Элемент 137

В середине 20-го века, известный ученый по имени Ричард Фейнман (Richard Feynman) сделал серьезное заявление, которое задело за живое ученых всего мира, заставив их вечно ломать голову. Он сказал, что, если мы когда-нибудь обнаружим 137-й элемент, у нас не будет никакого способа количественно определить его протоны и электроны. 137 элемент отличается тем, что это значение константы тонкой материи, определяемой как вероятность того, что электрон поглотит фотон. Теоретически, 137 элемент будет иметь 137 электронов и 100-процентную вероятность поглощения фотона. Его электроны вращались бы со скоростью света. Еще более безумно, что электроны элемента 139, если такое вещество существует, должны вращаться быстрее скорости света.
Достаточно физики? Обдумайте это, и вам станет интересно (ну, так же интересно, как чтение об электронах). Элемент 137 в теории может объединить три важные части физики: скорость света, квантовую механику и электромагнетизм. С начала 1900-х годов физики предположили, что элемент 137 может лежать в основе Великой Единой Теории, которая могла бы соединить воедино все три вышеупомянутые области. По общему мнению, это звучит так же безумно, как Зона 51 с инопланетянами или Бермудский треугольник.
5. Что необычного в названии?

Почти все названия элементов имеют больше смысла и значения, чем вы могли бы представить. Они выбираются на случайно. Мы бы, например, назвали элемент первым словом, пришедшим нам в голову. «Керфлумп». Да, отлично.
Далее, свои истоки названия элементов берут в одной из пяти основных категорий. Одна из них – имена известных ученых, классический пример эйнштейниум. Элементы также могут быть названы в честь мест, где их задокументировали, например, германий, америций, галлий и так далее. Вариантом для названий могут служить названия небесных тел, таких как планеты. Уран впервые был обнаружен вскоре после открытия планеты Уран. Элементы могут получить имена из мифологии: например, есть титан в честь греческих Титанов и торий в честь скандинавского Бога грома—или Звездного Мстителя, что вам больше нравится.
Наконец, есть названия, которые описывают свойства элементов. Аргон происходит от греческого слова argos, что означает «ленивый» или «праздный». Сейчас вы решите, что аргон самый ленивый элемент. Эй, аргон, иди работать. Бром – еще одно такое название от греческого слова bromos, что означает «зловоние», что очень точно описывает ужасный запах брома.
4. Вряд ли это было вдохновение

Если вы хороши в картах, то этот факт только для вас. Менделееву необходимо было каким-то образом сортировать все элементы, и для этого нужен был системный подход. Естественно, чтобы разбить таблицу по категориям, он обратился к игре в пасьянс. Менделеев написал на отдельных картах атомный вес каждого элемента, и приступил к безумной игре в пасьянс, так сказать. Он укладывал элементы в соответствии со специфическими свойствами, которые формировали тип «масти». Затем он смог распределить эти вошедшие в определенную категорию элементы в колонки в соответствии с их атомным весом.
Многие из нас с трудом могут пройти уровни обычной игры в пасьянс, поэтому этот парень-игрок 1000-го уровня, очень впечатляет. Что дальше? Кто-то решит обратиться к шахматам, чтобы произвести революцию в астрофизике, а также построить ракету, которая сможет совершить полет к краю галактики и обратно, оставаясь при этом абсолютно стабильной? Это вполне возможно, если такой сумасшедший профессор, как Менделеев, смог систематизировать нечто огромное с помощью карточной игры.
3. «Нет» инертным газам

Фото: Wikimedia
Помните, как мы классифицировали аргон как самый ленивый и скучный элемент в истории Вселенной? Менделеев чувствовал нечто подобное. Когда в 1894 году аргон удалось впервые выделить, он не вписывался ни в одну из колонок новой таблицы, поэтому вместо того, чтобы найти способ внести дополнение, ученый решил отрицать существование этого элемента.
Еще более удивительно, что аргон не единственный несчастный элемент, который настигла подобная участь. Еще пяти элементам было оказано в существовании, как и неклассифицированному аргону. Просто какая-то дискриминация элементов. Шутки в сторону, радон, неон, криптон, гелий, ксенон – всем им было отказано в существовании, только потому, что Менделеев не смог найти для них место в таблице. После многих лет реконфигурации и повторной классификации эти счастливые элементы (называемые инертными газами) смогли войти в элитный клуб под названием «Существующие элементы».
2. Романтические соединения

Этот факт для вас, романтики. Если взять бумажную копию Периодической таблицы и вырезать средние столбцы, то получится периодическая таблица, в которой отсутствуют элементы. Сложите ее один раз в середине IV группы, и тадам — вы узнали, какие элементы могут образовывать соединения друг с другом.
Элементы, которые при этом «поцеловались», образуют стабильные соединения. У них дополняющие друг друга электронные структуры, которые позволяют их объединять. Если это не настоящая любовь, такая же как у Ромео и Джульетты, или даже Шрека и Фионы, тогда что это?
1. Углерод главный

Углерод желает быть самым главным. Вы думаете, что знаете об углероде все, но нет. Этот плохой парень способен на большее, чем вы когда-либо думали. Знаете ли вы, что большее количество соединений содержит углерод, чем не содержит его? Как насчет того, что 20% веса живых организмов составляет углерод? Еще более странно, что каждый атом углерода в вашем теле был когда-то частью доли углекислого газа в атмосфере. Углерод не только является практически суперэлементом, но и четвертым по распространенности элементом во всей Вселенной.
Если бы Периодическая таблица была вечеринкой, вы бы захотели оказаться на ней рядом с углеродом. Кажется, этот элемент действительно умеет веселиться. Это также основной элемент алмазов, поэтому добавьте немного блеска в список его удивительных качеств.
7 малоизвестных фактов о химических элементах и таблице Менделеева
Генеральная ассамблея ООН провозгласила 2019 год Международным годом Периодической таблицы химических элементов.
Дело в том, что именно в этом году мы отпраздновали юбилей — 150 лет со дня открытия Дмитрием Ивановичем Менделеевым Периодического закона.
Во времена Менделеева уже было открыто больше шести десятков разных химических элементов, но всё ещё не было единой понятной и удобной классификации. Хотя многие учёные не раз пытались придумать концепцию для систематизации. Например, химик и музыкант Джон Александр Ньюленд предложил схему элементов, схожую с той, что впоследствии придумал Менделеев, но научное сообщество не восприняло всерьёз эту попытку, хотя бы потому, что там чрезмерно много внимания было уделено гармонии и связи с музыкой. Ещё один химик — Лотар-Юлиус Мейер — сначала старался расположить элементы по возрастанию степеней их окисления. Он предложил объединять элементы в «группы», но никак не раскрыл это понятие.
В 1868 году в журнале Русского химического общества была опубликована схема периодической таблицы Менделеева. Извещение об этом получили все именитейшие учёные того времени. Суть открытия была в том, что изменения в свойствах веществ происходят не монотонно, а периодически, то есть свойства в группах элементов начинают повторяться. В 1871 году все свои идеи Менделеев объединил в один периодический закон. Это позволило не только упорядочить известные элементы, но и увидеть тенденцию и предсказать некоторые на тот момент ещё не открытые вещества.
Вокруг этого открытия, как и вокруг самой личности Дмитрия Ивановича, до сих пор вьётся много слухов и домыслов. Самые известные из них уже множество раз опровергнуты, но всё равно почему-то упорно повторяются в анекдотах. Например, принято считать, что Менделеев увидел концепцию своей таблицы во сне. То, что это далеко от истины, говорил и сам Менделеев. Он возмущался, что на протяжении двадцати лет бился над упорядочиванием элементов, это не было каким-то спонтанным озарением, и думать так, значит, обесценивать многолетний труд учёного. Ещё есть байка о том, что Менделеев якобы изобрёл водку. На самом же деле, это всего лишь локальная шутка, возникшая из-за темы его диссертации: «Рассуждение о соединении спирта с водой». Водку изобрели задолго до Менделеева.
В общем, всё, что касается жизни самого Менделеева, очень часто вспоминается и обсуждается. Но мы сегодня попробуем рассказать немного больше о его периодической таблице и о некоторых элементах, открытие которых было интересным или курьёзным.
Вашему вниманию представляются 7 фактов о химических элементах, их свойствах и об их отношениях с таблицей Менделеева.
При чём здесь петух?
Шёл 1875 год. Молодой химик Лекок-де-Буабодран в совершенстве владел таким умением как спектральный анализ веществ. Это значит, что он отлично разбирался в том, какие цвета получаются при разложении света, пропускаемого через раскалённые вещества. Лекок практически наизусть знал все спектры, на которые можно разложить тот или иной элемент.
И вот однажды Буабодран изучал минерал сфалерит — цинковую обманку. Химик обнаруживает в его спектре новый цвет. Ярко-фиолетовая линия, которую увидел Лекок, ранее ещё никем не была описана, а значит вполне возможно, что французскому учёному удалось открыть новый элемент.
Лекок-де-Буабодран сразу же описал своё открытие и поместил в конверт. Конверт отдал своему учителю — академику Вюрцу, но попросил его не вскрывать, а просто сохранить. Почему? Потому что прежде, чем делать громкое заявление об открытии нового элемента, он хотел это ещё много раз перепроверить, чтобы со своими преждевременными выводами не прослыть опрометчивым. Но осторожный Лекок боялся, что пока он будет перепроверять, кто-нибудь другой заявит о таком же открытии и опередит его, так что описанное и датированное описание эксперимента в запечатанном конверте было доказательством, что Лекок обнаружил это первым.
И вот, Лекок полностью убедился в своей правоте, множество перепроверок доказали, что он действительно открыл новый, неизвестный до этого химический элемент. Имя этому элементу он дал в честь своей родины — Франции, что по-латински «Галлия». По крайнее мере, это официальная версия. Некоторые же считают, что элемент галлий так назван из-за латинского слова «галлус» — петух. Почему петух? Потому что именно так переводится имя Лекок с французского.

Кстати, галлий — один из тех элементов, существование которых предсказал Менделеев. Так что этот элемент, найденный ещё при его жизни, доказал, что открытый им периодический закон работает.
Галлий плавится при очень низкой температуре: всего 30 градусов. Если взять в руку кусочек галлия, он расплавится. Зато если вы захотите этот кусочек испарить, то придётся нагреть его аж до 2200°C.
Металл против монахов
Антимониум — серебристо-белый металл, среди химиков больше известный как сурьма. Этот металл известен уже много тысяч лет. Например, археологами доказано, что примерно три тысячи лет назад в Вавилоне из сурьмы делали сосуды. Но чаще, конечно, применялся не чистый металл, а его сульфид — «сурьмяный блеск».
В 1604 году появилось первое описание получения сурьмы из соединений. Это описание было в книге довольно известного монаха, а по совместительству алхимика, Василия Валентина.
Василий Валентин верил, что соединения сурьмы могут помочь очистить организм от «вредоносных начал». Он пытался применять сурьму в качестве лекарства. Например, он считал отличным «рвотным средством» вино, которое было выдержано в сурьмяных сосудах. А как вам «вечные пилюли», которые можно было использовать много раз — они просто проходили весь кишечный тракт? Все эти лекарства Василий использовал на монахах, и некоторых из них забирала мучительная смерть. Вот откуда взялось название «антимониум» — противомонашеский металл.

Сегодня есть мнение, что такого человека как Василий Валентин не существовало, ведь его не было в списках монахов ордена, к которому он себя причислял. Вполне возможно, что все его книги — коллективный труд нескольких алхимиков.
И ещё интересный факт про сурьму: в России это название произошло от турецкой косметической процедуры — «чернение бровей». И хотя в качестве краски для бровей сурьму употребляли редко, выражение насурьмить брови» довольно часто можно было услышать в быту.
Ленивый элемент, которому не нашли места
Здесь речь пойдёт о газе аргоне, который был впервые обнаружен английским химиком Кавендишем. Он установил, что в воздухе помимо всех известных находится ещё какой-то газ, но какой именно, установить ему не удалось.
Чуть позже, в 1892 году, в совершенно другом эксперименте этот газ снова был обнаружен, теперь уже физиком Джоном-Уильямом Страттом.
Уже в 1894 два химика выступили с публичным обращением и рассказали миру о своём открытии. Но вот что интересно: когда впервые удалось получить чистый аргон (что в переводе означает «ленивый» или «медленный»), он никак не вписывался в уже существовавшую периодическую таблицу. Казалось, что Менделеев просто решил это открытие проигнорировать, раз оно не вписывалось в его концепцию.
Точно такая же ситуация была с радоном, неоном, криптоном, гелием и ксеноном — люди поначалу не признавали эти газы, потому что было непонятно, куда их пристроить в таблице. Понадобилось несколько лет, чтобы выделить их в отдельную группу инертных газов и перестать отрицать их существование.
Цвета в названиях элементов
Вообще названия химическим элементам дают всегда примерно одинаково: в основном либо по каким-то внешним свойствам, либо по месту открытия, либо по имени учёного, которому мир обязан новым элементом.
И если обратить внимание конкретно на элементы, названные по каким-то своим свойствам, то очень частое явление — «цветное» название, как будто именно разнообразие цветов больше всего впечатляло химиков.
Например, название «хлор» происходит от греческого слова «хлорус», что в переводе гласит «жёлто-зелёный». А элемент йод — «йодес» с греческого — это фиолетовый. Здесь надо пояснить, что имеется в виду не цвет самого вещества, а, как и в первой истории про Лекока-де-Буабодрана, цвет спектральный линий в спектрах излучения соединений.
Иридий тоже был назван в соответствии с греческим языком: слово «ирис» означает радуга. Соли иридия имеют множество разнообразных окрасок.
«Таллос» в переводе означает «молодая зелёная ветка», вот и элемент таллий так назван из-за ярко-зелёной линии в спектре излучения его соединений.
«Цезиум» — голубой цвет «небесного свода», соответственно, у цезия в спектре излучения солей были найдены именно голубые линии. А у серы такое название потому, что в древнеиндийском языке «сира» означает светло-жёлтый цвет.
И это далеко не всё, с цветами связано огромное количество названий элементов.
А вот названий в честь запаха элемента всего два: бром — «бромос» — «зловоние», и осмий — «осме» — «запах».
Кстати, довольно логично, но по вкусу элементы ни разу не называли.
Элементы, открытые случайно
Так или иначе, почти все элементы были открыты незапланированно. Просто, например, не сходились расчёты, или внезапно проявлялись неожиданные свойства. Но некоторые пробелы в таблице Менделеева были заполнены как будто не учёными, а чередой обстоятельств. Совпадение? Абсолютное.
Вот, скажем, фосфор был открыт солдатом Хённинг Брандом в 1669 году. Правда, он не искал фосфор, он вообще пытался синтезировать философский камень, и для этого он занимался выпариванием солдатской мочи. В какой-то момент он заметил уже привычное для нас зеленоватое свечение в сосуде. Но Бранд так никогда и не узнал, что его открытие было важным, ведь в его время ещё даже не было представления о химических элементах.

А ещё одно открытие было фактически сделано котом! У одного известного химика был кот, имевший обыкновение сидеть на плече своего хозяина. И вот однажды, испугавшись чего-то в лаборатории, кот спрыгнул с плеча на пол и задел стоявшие там бутылки с веществами. В одной бутылке была концентрированная серная кислота, а в другой — суспензия золы для водорослей в этаноле. В общем, жидкости случайно смешались, появился сине-фиолетовый пар, и постепенно на всех близстоящих предметах начали образовываться небольшие фиолетовые кристаллики с особыми свойствами. Оказалось, что это был новый на тот момент элемент — йод. А фамилия учёного, который с помощью кота его открыл, — Куртуа.
Открытие несуществующих элементов
Довольно часто в науке были курьёзные ситуации, когда казалось, что открыт новый элемент, но при подробнейшем изучении это «новшество» оказывалось всего лишь очередным изотопом чего-нибудь уже давно известного.
Вот, например, истории открытия таких элементов как «небулий» и «короний».
Астрономы исследовали солнечную систему, точнее «корону» Солнца — внешний атмосферный слой нашей звезды. Во время этих исследований были найдены спектральные линии, совершенно ни на что не похожие, по крайней мере, их раньше не видели на Земле. Логично было предположить, что они принадлежат какому-то новому элементу. Его назвали «короний» в честь места, где нашли его спектральный линии.
Точно так же нашли ещё один «новый элемент», теперь уже при изучении спектров газовых туманностей. Ещё один новый элемент был назван небулием.
Оба эти элемента не вписывались в таблицу Менделеева, для веществ с такими свойствами там просто не было места. И при более подробном исследовании оказалось, что это вовсе не необычные новые элементы, а в первом случае сильно ионизированное железо, а во втором — обычный земной кислород.
Могут ли химические элементы «вымереть»?
В принципе, большая часть химических элементов на нашей планете довольно устойчива. Но есть среди них и те, содержание которых в атмосфере, гидросфере и земной коре исчезающе мало.

Например, сравнительно мало радиоактивных элементов. Технеций, астат, актиний, полоний или франций уже считаются «вымершими». Учёные полагают, что раньше этих элементов было гораздо больше, но именно в силу своей радиоактивности и стремления к распаду их количество уменьшается.
Сейчас есть несколько элементов, находящихся на грани «вымирания»: атомы калия-40, астата-211 и актиния-235.
Такая же судьба ждёт и уран, хотя вымирать он будет гораздо дольше. По примерным расчётам, в каждом килограмме урана за сто лет образовывается тринадцать граммов свинца и два грамма гелия. А это значит, что всему урану, который сегодня есть на Земле, осталось примерно четыре миллиарда лет. Когда он полностью исчезнет, все урановые месторождения будут свинцовыми, а атмосфера заметно обогатится гелием.
Стендовый материал по химии «Занимательная химия»
Запоминалки для школьников
Реакции двойного обмена идут до конца:
Если выделится газ —
Это раз;
И получится вода —
Это два;
А еще — нерастворимый
Осаждается продукт…
«Есть осадок,» — говорим мы.
Это третий важный пункт.
Химик правила обмена
Не забудет никогда:
В результате — непременно
Будет газ или вода,
Выпадет осадок —
Вот тогда — порядок!
А вот анионы кислот, содержащих серу:
S2— — сульфид-анион
SO32— — сульфит-анион
SO42— — сульфат-анион
Сульфит не путайте с сульфидом,
Чтоб места не было обидам:
Сульфиды — сероводорода
Родня. И нет в них кислорода!
А вот сульфит. Скорей смотри:
В нем кислорода сразу три!
Добавим кислорода атом —
И познакомимся с сульфатом!
Запоминательные стихи
…ПРО ГАЛОГЕНЫ
Хлор хвалился: «Нет мне равных!
Галоген я самый главный.
Зря болтать я не люблю:
Всё на свете отбелю!»
Иод красой своей гордился,
Твердым был, но испарился.
Фиолетовый, как ночь,
Далеко умчался прочь.
Бром разлился океаном,
Хоть зловонным, но — румяным.
Бил себя он грозно в грудь:
«Я ведь бром! Не кто-нибудь!..»
Фтор молчал и думал: «Эх!..
Ведь приду — окислю всех…»
Разбавление серной кислоты водой:
Сначала вода, а потом кислота –
Иначе случится большая беда!

Запоминательные стихи по органической химии
Запомним, друг, и я, и ты,
Чем отличаются спирты —
В них углерод и гидроксид,
И каждый спирт легко горит.
R — это значит радикал,
Он может быть велик и мал,
Предельный или непредельный.
Но это разговор отдельный.
Приятно пахнут альдегиды,
Но группа C(H)O их выдаст.
Среди карбоновых кислот
Известных «лиц» невпроворот.
В кислотах — группы карбоксильные,
Но все кислоты здесь — несильные.
В кетонах группа есть CO,
Но это тоже ничего…
Горит прекрасно ацетон,
И растворитель — тоже он.
Мы говорим спокойно: жир.
А между прочим, он — эфир,
Он из кислот и глицерина.
Такая вот у нас картина…
Если ты, придя с мороза,
Наливаешь крепкий чай,
Хорошенько сахарозу
В чашке ложкой размешай.
Виноградную глюкозу
И медовую фруктозу
И молочную лактозу
Любит взрослый и малыш.
Но крахмалом и клетчаткой,
Что совсем-совсем несладки
Тоже нас не удивишь.
Так устроена природа —
Это тоже углеводы.

Интересные факты о химии
…..В древности не было аптек: лекарства врачи составляли сами. Сырье для изготовления целебных снадобий они покупали у «копателей корешков растений» и хранили на складе — аптеке. Само слово «аптека» происходит от греческого «склад». В России при царе Михаиле Федоровиче (1613-1645) при аптеках уже существовала должность «алхимиста» (химика-лаборанта), который готовил лекарства. Многие знаменитые ученые, вошедшие в историю как химики, по своей основной должности были именно аптекарями и фармацевтами.
…..Для организма человека определенно установлена роль около 30 химических элементов, без которых он не может нормально существовать. Эти элементы называют жизненно необходимыми. Кроме них, имеются элементы, которые в малых количествах не сказываются на функционировании организма, но при определенном содержании являются ядами.
…..Небьющееся стекло было изобретено случайно. В 1903 году французский химик Эдуард Бенедиктус нечаянно уронил колбу, заполненную нитроцеллюлозой. Стекло треснуло, но не разлетелось на мелкие кусочки. Поняв, в чём дело, Бенедиктус изготовил первые лобовые стёкла современного типа, чтобы уменьшить количество жертв автомобильных аварий.
…..За всю историю периодической системы элементов было несколько сот вариантов ее графического изображения. Известны ее изображения в виде различных геометрических фигур: пространственных, плоскостных, аналитических фигур-спиралей. Наибольшее распространение получили три формы: короткая, предложенная Менделеевым и получившая всеобщее признание, длинная и лестничная. Длинную также разрабатывал Менделеев, а в усовершенствованном виде она была предложена в 1905 г. А. Вернером. Лестничная форма разрабатывалась английским ученым Т. Бейли (1882), датским ученым Ю. Томсоном (1895), а позднее была усовершенствована Н. Бором (1921).
…..В 1985 году группа американских и английских исследователей открыли молекулярные соединения из углерода, сильно напоминающие своей формой футбольный мяч. В честь него и хотели назвать открытие, однако учёные не договорились, какой термин использовать — football или soccer (как зовут футбол в США). В итоге соединения назвали фуллеренами в честь архитектора Фуллера, который придумал геодезический купол, составленный из тетраэдров. 
…..По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». 
…..Водород — самое распространённое вещество во Вселенной (примерно 90% всех атомов во вселенной). Атомы водорода настолько малы, что если их в количестве 100 миллионов разместить в цепочку друг за другом, получится длина лишь в один сантиметр.
…..Радиоактивный химический элемент астат — наиболее редкий элемент из всех, что встречаются в природе. Если суммировать содержание астата в земной коре в любой момент времени, получится не более одного грамма. Но число это будет почти одинаковым, так как скорость образования радионуклидов астата, входящих в состав радиоактивных рядов урана, постоянна и равна скорости их распада.
…..Стенки мыльного пузыря – пожалуй, самая тонкая материя, которую человек способен увидеть невооруженным взглядом. Для примера, толщина папиросной бумаги или волоса в несколько тысяч раз толще.
Скорость лопания мыльного пузыря составляет 0.001 секунды. Скорость ядерной реакции – 0.000 000 000 000 000 001 секунды.
Железо, очень твердый и прочный материал в обычном его состоянии, становится газообразным при температуре 5 тысяч градусов Цельсия.
…..В состав пластмассы для деталей конструктора «Лего» входит сульфат бария. Эта соль не растворяется в воде, что делает её нетоксичной для организма, и хорошо видна на рентгеновских снимках. Таким образом, если ребёнок проглотит деталь, её будет легко найти по этим снимкам.

Химия в жизни человека ℹ️ роль химии в повседневной жизни современного общества, значение химии в быту, вред и польза химических веществ, интересные факты, примеры применения
Нередко учащимся 8 класса задают написать сочинение, сообщение, эссе, выполнить проект на тему «Химия в жизни человека»? Это неслучайно. Уже не одно столетие химия занимает важное место в жизни людей.
Лекарства, косметика, бытовая химия, многие пищевые добавки, вещи первой необходимости – все это получено с помощью химических веществ и их реакций. Роль этой науки большей частью положительна. И лишь бесконтрольное ее использование в отраслях потребительского рынка может нанести вред.
Роль химии в жизни человека
Химия – не только научно-теоретическая дисциплина. Это одна из самых применимых на практике наук. Ее открытиями пользуются промышленность, сфера услуг и просто любая семья.
Химия в быту

Каждая современная семья использует огромное количество средств бытовой химии – на кухне, в ванной, гостиной, спальне. Они помогают экономить время, сохранять здоровье, поддерживать чистоту, создавать красивый интерьер, выращивать растения, ухаживать за автомобилями.
Вот только некоторые из этих средств:
-
стиральные порошки, мыло;
-
шампуни;
-
клеи, краски, лаки;
-
пятновыводители, очистители, крема для обуви;
-
удобрения, вещества для защиты домашних растений от насекомых, болезней.
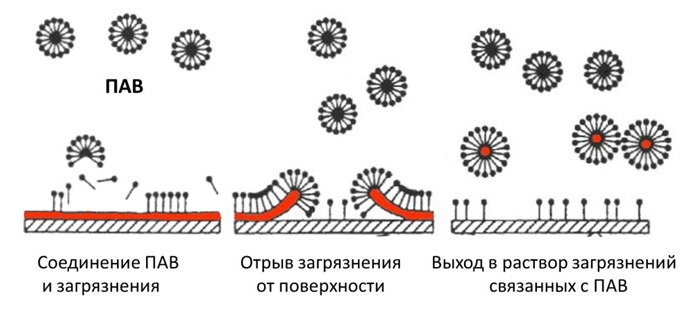
Так, при стирке активные вещества вступают в реакцию с грязью, в результате чего она как бы отталкивается от ткани. В хозяйственном мыле – это обычная щелочь природного происхождения, в порошках – синтетические ПАВ. Для создания красок тоже используют химию: едкий натр в гуаши, олифа – в масляных разновидностях.
Однако химия оставила свой след и в привычных операциях. Когда готовят пирог, то смешивают соду и лимонный сок. Происходит процесс растворения соды и выделения углекислого газа СО2. Он пробивает себе выходы, и тесто поднимается.
Очистка металлической посуды от накипи с помощью лимонной кислоты производится в результате растворения твердых карбонатных пленок (накипи) в кислой среде.
Химия и человеческий организм
Человек – это сложная система, состоящая из различных элементов и органических веществ. Но требуется постоянное их пополнение. Кальций, калий, кислород, фосфор, аминокислоты – все это должно поступать в организм с едой.
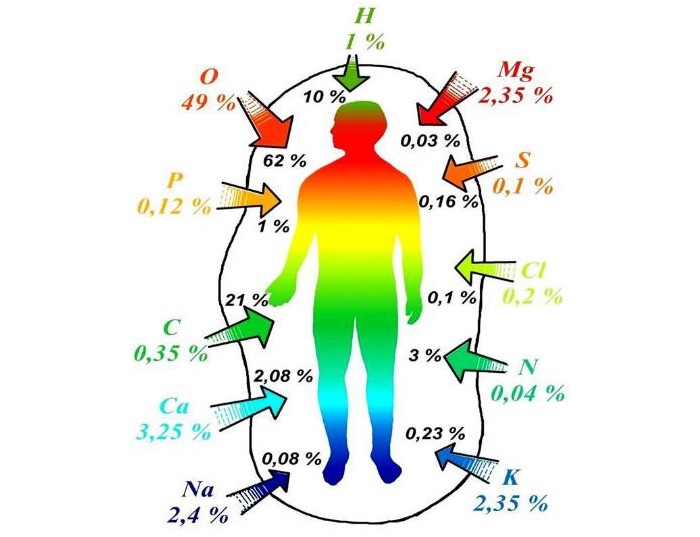
Влияние внешних веществ по-разному воздействует на человека. Так, принятие аспирина с помощью химических реакции разжижает кровь. Для одного человека, с густой кровью и склонностью к тромбам, — это спасение. Для другого, с нарушением свертываемости крови, применение этого лекарства может довести до летального исхода.
Поэтому химические вещества или продукты с ними сопровождаются инструкциями, как обезопасить себя.
Пример: уксусную кислоту нельзя употреблять, не разбавив большим количеством воды. При работе с чистящими гелями, пастами, надо надевать перчатки. Нельзя употреблять слишком много соли из-за накопления натрия, ведущего к отекам.
Химия в промышленности
На химических реакциях основано большинство промышленных производств мира.

Так, благодаря промышленной химии, получают:
-
лекарства;
-
продукты питания;
-
пластиковые, резинотехнические изделия;
-
бензин;
-
бумажные изделия;
-
синтетические ткани;
-
строительные и отделочные материалы;
-
металлы и сплавы с новыми свойствами для медицины, космоса, электроники;
-
кисломолочную продукцию и многое другое.
Как отдельный комплекс выделяют химическую промышленность, состоящую из фармацевтической, нефтехимической, горно-химической отраслей. Общество получает от них значительный объем продукции.
Значение химии в нашей жизни
Влияние химии на качество жизни человека двояко. Она способна как помогать, так и наносить вред человеку и окружающей среде.
Вредное воздействие
Несмотря на огромную пользу, химия способна причинить вред. От стиральных порошков может возникнуть раздражение на коже, особенно у детей.
Лаки и некоторые краски при продолжительном вдыхании способны привести к интоксикации с головокружением, тошнотой, слабостью.
Удобрения при передозировке накапливаются в плодах и зелени, приводя к поражению желудочно-кишечного тракта.
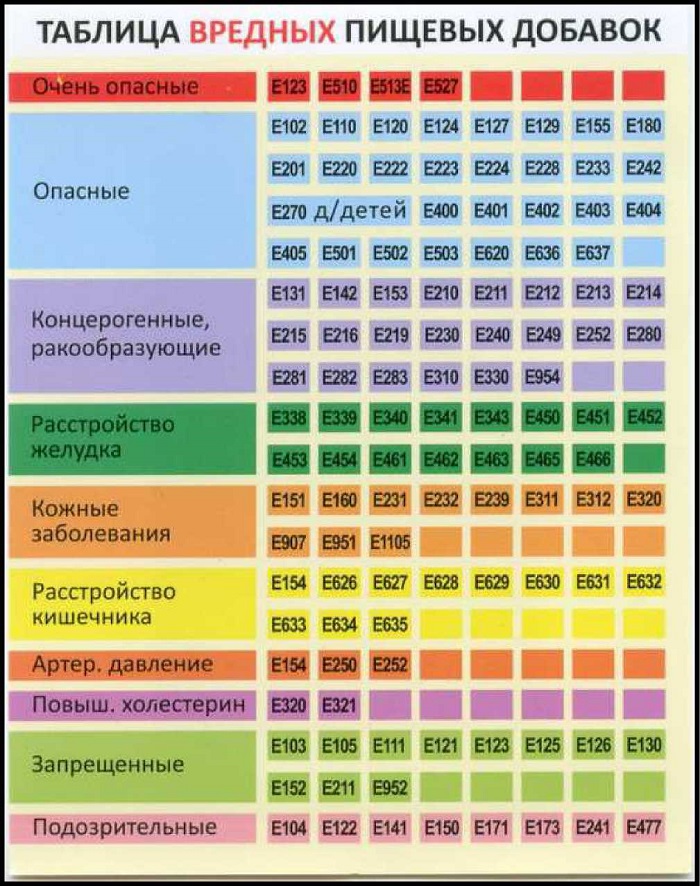
Но наибольший вред способны привести пищевые химические добавки с кодом «Е», особенно если они не прошли длительного изучения или если их употреблять в больших количествах с едой.
Пример: модифицированный крахмал в йогуртах способен пагубно влиять на поджелудочную железу. А волокна, обработанные специальными химикатами для прочности и сохранения яркой окраски, вызывают аллергические дерматиты. Особенно это характерно для продукции одной из азиатских стран.
Чтобы оградить свой организм от вредного воздействия, следует:
-
соблюдать меры предосторожности, если используются такие вещества;
-
не приобретать продукцию, производитель которой неизвестен;
-
питаться полезной натуральной едой, ограничивая вкусные, но вредные продукты.
Эти простые правила позволят без риска для здоровья пользоваться всеми достижениями современной химии.
Польза химии
Вещества, полученные химическим путем, используют в медицине. Они помогают сохранить больным людям жизнь, поддерживают здоровье.
Одно из достижений – способность улучшать вкусовые качества: сахар, ванилин – тому наглядный пример.
В доме химические вещества убивают микробов, поддерживают комфортный микроклимат в квартире, дают тепло.
Сельским жителям и сельскохозяйственным предприятиям помогают обезопасить поле, сад, огород, приусадебное хозяйство, птицефабрику, повысить урожайность или надои. Это дает возможность обеспечивать едой жителей планеты.
Интересные факты о химии в повседневной жизни

Несколько любопытных фактов, где еще мы можем наблюдать химические реакции:
-
Абсорбция – это способность поглощать что-либо. Например, активированный уголь захватывает вредные, болезнетворные соединения. Однако такими же способностями обладает обычный рис. Если в слишком соленый суп опустить мешочек с этим злаком, то соль впитается в него, и суп будет спасен.
-
Мозг – это минилаборатория, в которой ежеминутно происходит около ста тысяч химических реакций.
-
Садовые и дикие яблоки, оставленные в разрезанном виде, через 5-10 минут становятся буроватыми. Но они не испортились. Это произошла реакция окисления железа, содержащегося в мякоти. Но в воздухе железо соединилось с кислородом, и произошло образование оксида.
- Если вы думали, что железо – это что-то прочное и надежное, вы ошибаетесь. Железо, нагретое до 5000 градусов Цельсия, становится газообразным.
- Множество химических элементов получили своё название в честь стран или других географических объектов. Сразу 4 элемента — иттрий, иттербий, тербий и эрбий — были названы в честь шведской деревни Иттербю, около которой обнаружили крупное месторождение редкоземельных металлов.
- По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
- Литий — самый легкий металл. Он всплывает, например, в керосине.
- Водород — самое распространённое вещество во Вселенной (примерно 90% всех атомов во вселенной).
- Водород — самый лёгкий газ. Масса 1 литра водорода в газообразном состоянии составляет всего 0,08988 грамм.
- Вода может замёрзнуть в трубопроводе при температуре +20 °C, если в этой воде присутствует метан (если быть точнее, из воды и метана образуется газовый гидрат). Молекулы метана «расталкивают» молекулы воды, так как занимают больший объём. Это приводит к понижению внутреннего давления воды и повышению температуры замерзания.
- В каждом литре морской воды примерно 25 граммов соли.
- В Мировом океане в 1 т воды содержится примерно 7 мг золота. А общая масса этого металла в водах океана составляет 10 млрд.тонн.
- Самым крупным существующим в настоящий момент платиновым самородком является «Уральский гигант» весом 7 кг 860,5 г. Хранится в Алмазном фонде Московского Кремля.
- Ртуть — не единственный металл, который пребывает в жидком состоянии при комнатной температуре. Галлий (Ga) в руках плавится, цезий (Cs) и франций (Fr) также находятся в жидком состоянии при комнатной температуре.
- В химии есть такое понятие — сублимация, которое обозначает прямой переход вещества из твердого в газообразное состояние, минуя жидкую фазу. В быту чаще всего такое явление встречается при испарении сухого льда, который превращается в углекислый газ.
- Дмитрий Менделеев принимал у Петра Столыпина экзамен по химии и поставил «пять».
- Менделеев разработал стандарт для русской водки, чем прославился никак не меньше, чем открытием периодической таблицы. А во-вторых, Менделеев любил изготавливать чемоданы, причем некоторые соседи по улице знали его именно как отличного чемоданного мастера, а не гениального химика…
- Интересное свойство серебра.
В IV веке до нашей эры войска Александра Македонского вторглись в Индию. На берегах реки Инд в войсках разразилась эпидемия желудочно-кишечных заболеваний, которая. как ни странно, не затронула ни одного военачальника. Оказалось, что простые воины пользовались оловянной посудой, а их командиры-серебряной. Тогда и вспомнили, что персидский Царь Кир II Великий о время военных походов приказывал хранить питьевую воду в серебряных сосудах. Много позже римские легионеры стали носить панцири, наколенники и поножи из серебра. Серебро обладает бактерицидными свойствами, обезараживая воду, а также способствовало быстрому заживлению ран без нагноений. - А знаете ли вы, что у мочи в древности было много применений, которые, пожалуй, сейчас никому не придут в голову. Древние греки, заметив, что моча обладает ярко выраженными антисептическими свойствами, промывали ей раны и даже использовали в качестве ополаскивателя для рта. У древних римлян собранную мочу продавали в мастерские по пошиву одежды – ее использовали для очистки шерсти от грязи, а иногда и вымачивали ткани перед окраской. А алхимики на протяжении многих веков пытались получить из нее золото. Кстати, последний факт привел к открытию белого фосфора Хенигом Брандом в 1669 году.
- Парацельс утверждал, что задача алхимии — изготовление лекарств; при этом медицина Парацельса основывалась на ртутно-серной теории. Он считал, что в здоровом организме три принципа — Ртуть, Сера и Соль, — находятся в равновесии; болезнь представляет нарушение равновесия между принципами. Для его восстановления Парацельс ввёл в практику лекарственные препараты минерального происхождения — соединения мышьяка, сурьмы, свинца, ртути и т. п., — в дополнение к традиционным растительным препаратам.
- Хлорид кобальта можно успешно использовать для тайнописи: буквы, написанные его раствором, содержащим в 25 мл воды 1 г соли, совершенно невидимы и проявляются, делаясь синими, при легком нагревании бумаги.
- Платина в переводе с испанского буквально означает «серебришко». Объясняется такое пренебрежительное название, данное этому металлу конкистадорами, исключительной тугоплавкостью платины, которая не поддавалась переплавке, долгое время не находила применения и ценилась вдвое ниже, чем серебро. Сейчас на мировых биржах платина дороже серебра примерно в 100 раз.
- Шерлок Холмс был первым детективом, использовавшим химические знания для раскрытия преступлений
- Небьющееся стекло было изобретено случайно. В 1903 году французский химик Эдуард Бенедиктус нечаянно уронил колбу, заполненную нитроцеллюлозой. Стекло треснуло, но не разлетелось на мелкие кусочки. Поняв, в чём дело, Бенедиктус изготовил первые лобовые стёкла современного типа, чтобы уменьшить количество жертв автомобильных аварий.
Интересные факты о химии и химических элементах
Все мы учим или учили химию, но что интересного в этом предмете — всем запоминаются длинные формулы, валентности, определения. Мало кто знает интересные факты о химии и химических элементах — а прочитав эту статью вы взглянете на этот предмет по-новому и с большим интересом.
Интересные факты о химии и химических элементах
Теперь вы знаете интересные факты о химии, химических элементах, ученых, а если вы знаете еще интересные факты о химии оставляйте их в комментариях.

