Интересное в химии. Химия — интересные факты
Интересное в химии. Химия — интересные факты
В 21 веке химия, наряду с математикой и физикой, проникла во все сферы жизни людей. Лекарства, зеркала, покрышки машин… Химические элементы окружают нас повсюду. Даже сам человек состоит из молекул и химических цепочек. Представляем интересные факты о химии.
Удивительное рядом
- Процесс перехода вещества из твёрдого состояния в газообразное в химии называется сублимацией.
- Для изготовления кваса используется реакция брожения.
- Если опустить в пересоленный суп марлю с рисом, блюдо можно спасти, так как за счёт абсорбции соль вытянется.
- В фекалиях содержится скатол, и именно из-за него они неприятно пахнут. Интересно то, что в небольших количествах скатол приятно пахнет, и его добавляют в сигареты и парфюм.
- 100000 – именно столько химических реакций проходят за секунду в мозге человека.
- В состав пластмассы для «Lego» входит сульфат бария. Это вещество совершенно безвредно для человеческого организма.
- 16 сентября – Международный день охраны такого химического элемента, как озон.
- Слезы у человека при нарезании лука вызывает содержащаяся в нём сера.
- Интересные факты о химических элементах. Множество элементов называют в честь стран – Америций, Индий, в честь городов – Иттербий, Берклий, Гольмий, в честь учёных – Бор, Менделевий.
- Дефлогистрированный воздух – принятое в науке название кислорода.
- Американец Чарльз Гудьир случайно открыл процесс вулканизации и создал прочную резину, которая не размягчается в жару и не трескается на холоде. Он просто забыл на горячей плите смесь серы и синтетического каучука.
- Во время стирки белья происходит гидролиз солей.
Интересные факты о химических элементах в организме человека. Интересные и занимательные факты о некоторых химических элементах
— занимает первое место в периодической системе Менделеева, невесомый газ, образующий воду при соединении с кислородом.
Литий — это легчайший металл на земле, почти наполовину легче воды, а еще его можно разрезать ножом.
Скандий — используется с целью получения сверхтвёрдых веществ в индустрии.
Титан — не вызывает аллергических реакций и может быть использован в хирургии и для пирсинга.
Медь — губительна для бактерий. Оказывается, медные водопроводные трубы обладают дезинфицирующими качествами, а дверные ручки из этого материала — антибактериальными.
Теллур — токсичный элемент с запахом тухлого чеснока.
Ванадий — если его добавить в сталь или чугун, то сплав получит необычайную прочность.
Галлий — металлический элемент, у которого низкая температура плавления, всего 28 градусов. Если попытаться размешать галлиевой ложкой чай, то она растворится в стакане.
Сурьма — в древние времена использовалась в косметических целях для подводки глаз и бровей, а так же в качестве слабительного. На самом же деле, сурьма чрезвычайно токсична, а в современной промышленности из нее изготавливают сильнейшие кислоты, которыми можно прожечь стекло.
Европий — применяется для защиты от подделок денежных банкнот евро, которые считаются самой защищенной валютой в мире на сегодняшний день.
Азот — главный компонент воздуха, которым мы дышим, но при попадании в легкие в чистом виде способен вызвать летальный исход.
Сера — в чистом виде имеет неприятный запах, но является незаменимым элементом для человеческого организма и замедляет его старение.
Ртуть — единственный металл, который при комнатной температуре находится в жидком состоянии, и один из тяжелейших — 1 литр весит больше 13 кг.
Иридий — назван в честь древнегреческой богини радуги. Он один из наиболее прочных, тяжеловесных и редких металлов на земле. С его помощью смогли определить возраст древних динозавров и других палеонтологических ископаемых.
Осмий — наиболее тяжелое металлическое вещество на планете, которое практически не поддается обработке. Свое название обрел из-за мерзкого амбре, состоящего из смеси хлора и чесночных капель.
Источник: https://interesnyefakty.com/novosti/interesno-o-himii-himiya-interesnye-fakty
Химия вокруг нас интересные факты. 10 интересных фактов, о химическом элементе Азоте.

Азот — это очень важный элемент, имеющий особое биологическое значение для всех живых существ, а так же, он играет особую роль в современной промышленности. В периодической системе химических элементов Д.И. Менделеева азот находится во II периоде, V группе, главной подгруппе. Но, что же в нем такого особенного? Возможно десять ниже перечисленных фактов об азоте, помогут пролить свет на это вопрос.
1. В конце XVII века, три независимых друг от друга исследователя смогли получить азот во время своих опытов. Имена этих исследователей: Генри Кавендиш, Джозеф Пристли и Даниэль Резерфорд. В 1772 году Генри Кавендиш провёл следующий опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался в углекислый газ, который затем поглощался щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое простое вещество (химический элемент). В результате подобного эксперимента азот был получен и Джозефом Пристли и кстати схожие эксперименты в то время проводил так же Карл Шееле. Однако, лишь Даниэль Резерфорд в том же 1772 г. в своей диссертации «Испорченный воздух» подробнее всех описал свойства полученного им вещества: оно не реагирует со щелочами, не поддерживает горение и непригодно для дыхания. Именно поэтому он и стал считаться первооткрывателем азота. Слово «азот» происходит от греческих терминоэлементов а – отрицающий, зоэ – жизнь. Позже, Лавуазье предложил латинское название данного элемента Nitrogenium. Поэтому в периодической системе азот обозначается символом N. Как простое вещество азот образует двухатомные молекулы N2.

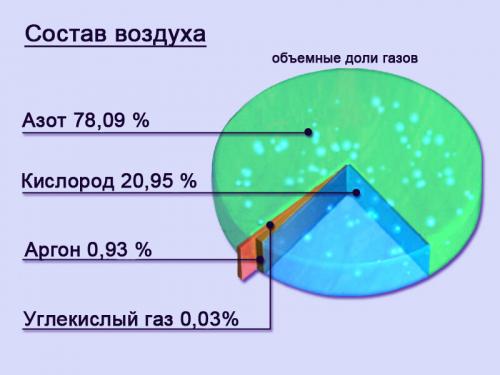
2. По объему азот занимает 4/5 земной атмосферы. Значительные количества азота содержатся в водах мирового океана и в земной коре. 2.5% массы всех живых организмов приходится на азот.
3. Как правило, чистый азот совершенно безвреден для человека. В конце концов, на 78.1% из него состоит воздух, которым мы дышим. В обычном состояние это газ, без цвета, вкуса и запаха. Однако, при высокой концентрации в воздухе, азот может вызывать чувство опьянения, удушья и даже привести к смерти. Так же страшен азот и при кессонной болезни ныряльщиков на глубину.
4. Раньше азот получали из множества различных минеральных веществ. Например, при разложение нитрита аммония:
Nh5NO2 = N2 + h3O
При нагревание дихромата калия с сульфатом аммония:
K2Cr2O7 + (Nh5)2SO4 = (Nh5)2Cr2O7 + K2SO4
(Nh5)2Cr2O7 = N2 + Cr2O3 + 4h3O
При пропускание аммиака над оксидом меди (II):
3CuO + 2Nh4 = N2 + 3Cu + 3h3O
И т.д.
Однако сейчас примерно миллиард тон азота в год добываются прямо из атмосферы.
5. Мгновенная заморозка чего бы то ни было в жидком азоте, это распространенный кинематографический миф. Жидкий азот действительно имеет очень низкую температуру (-192 градуса Цельсия), но и теплоемкость этого газа низка настолько, что время замораживания даже небольших предметов исчисляется множеством минут.
Активнее всего жидкий азот используется в различных охлаждающих аппаратах, так как инертность азота в отношение других веществ делает его идеальным хладагентом.

6. Азот – очень эффективное средство пожаротушения. Пожары в городе им тушат редко, так как газ сложно оперативно доставить к очагу возгорания и он быстро испаряется на открытой местности. Однако, внутри шахт такой метод тушения пожаров применяется очень часто.
7. Оксид азота (I) (N2O), так же известный как закись азота или веселящий газ, используется для наркоза и улучшает работу двигателей автомобилей. Сам он не горит, но очень хорошо поддерживает горение.
Оксид азота (II) (NO) – очень ядовитое вещество. Однако, в микродозах он содержится во всех живых организмах. В теле человека монооксид азота вырабатывается для нормализации работы сердца, а так же для предотвращения гипертонии и инфарктов.
8. Огромные количества получаемого сегодня азота расходуются на производства садовых удобрений и взрывчатых веществ.
9. А знаете ли вы, что в трубочке ртутного медицинского градусника, помимо серебристого вещества ртути находится так же бесцветный газ азот.

10. Азот, вместе с водородом, кислородом и гелием являются четверкой самых распространенных элементов во Вселенной.
На этом все. Если вам понравилась данная статья, ставьте лайки, пишите в комментариях и не забывайте подписываться на мой канал.
Интересные вопросы по химии. Интеллектуальная игра по химии для 8-х классов: «Эрудиты, вперед!»
Цели мероприятия:
- Расширить кругозор, активизировать опыт учащихся, развить логические и аналитические способности мышления.
- Мотивировать учащихся на успех и индивидуальное и коллективное творчество.
- Формировать и совершенствовать навыки самостоятельной и коллективной творческой работы.
- Формировать умения и навыки, которые носят в современных условиях общенаучный, общеинтеллектуальный характер.
- Воспитывать устойчивый интерес к изучаемому предмету – к химии.
“Просто знать – еще не все, знания нужно использовать”
И.В. Гете
Добрый день, дорогие ребята, уважаемые учителя! Мы рады приветствовать всех, кто собрался сегодня на нашу интеллектуальную игру: зрителей, жюри, и, конечно же, команды. Цель нашей игры – расширить кругозор знаний, полученных на начальном этапе изучения химии, повысить эрудицию, в увлекательной форме провести викторину по предмету. Выступление команд будет оценивать жюри. Пи выступлении команд будет учитываться не только глубина знаний, но и остроумие, находчивость, оригинальность ответов, активность и сплоченность. Пусть этот праздник откроет для каждого что-то новое и интересное, пусть запомнятся улыбки и шутки, крепче станет дружба между вами.
Команды по очереди выбирают себе область знаний и цену вопроса в соответствии с таблицей. Вопрос зачитывает ведущий. На обдумывание дается 5 – 10 с. При правильном ответе команда получает баллы в соответствии с ценой вопроса, при неправильном – такое же количество баллов снимается. Если команда, выбравшая вопрос затрудняется с ответом, то игра переходит в индивидуальную, и каждый участник игры может набирать баллы, подняв сигнальную карточку. Если на данный вопрос нет ответа, то его дает ведущий.
В “Синем” и “Красном” раундах предусмотрены по два вопроса “Кот в мешке”, обозначенные в перечне вопросов звездочкой. Команда, получившая такой вопрос, имеет право передать его другой команде.
Вопросы “Синего раунда”
| Металлы и неметаллы | 10 | 20 | 30 | 40 | 50 |
| Химические загадки | 10 | 20 | 30 | 40 | 50 |
| Закончите фразу | 10 | 20 | 30 | 40 | 50 |
| Верите ли вы, что… | 10 | 20 | 30 | 40 | 50 |
| Первоначальные химические понятия | 10 | 20 | 30 | 40 | 50 |
| Превращение без превращений | 10 | 20 | 30 | 40 | 50 |
| Узнай вещество или элемент | 10 | 20 | 30 | 40 | 50 |
Этот раунд проводится аналогично “синему”, но изменяются области знаний и цена вопроса в соответствии с таблицей, а также предусмотрены два вопроса “Своя игра”, обозначенные в перечне вопросов двумя звездочками. Команда, получившая такой вопрос, делает свою ставку, не превышающую суммы заработанных баллов. Другие команды тоже делают свои ставки, но отвечает та команда у которой ставка выше.
interesnyefakty.com
Факты из химии. Интересные факты о химии + Видео
Факты из химии. Интересные факты о химии + Видео
Химия – всем знакомый школьный предмет. Наблюдать за реакцией реагентов нравилось всем. Но мало кому известны интересные факты о химии, о которых мы расскажем в данной статье.
- 1. Современные пассажирские самолеты во время девятичасового полета используют от 50 до 75 тонн кислорода. Столько же этого вещества вырабатывает 25000-50000 гектаров леса в процессе фотосинтеза.
- 2. Один литр морской воды содержит 25 граммов соли.
- 3. Атомы водорода настолько малы, что если их в количестве 100 миллионов разместить в цепочку друг за другом, получится длина лишь в один сантиметр.
- 4. В одной тонне воды Мирового океана содержится 7 миллиграмм золота. Общая же сумма данного драгоценного металла в водах океанов составляет 10 миллиардов тонн.
- 5. В человеческом организме примерно 65-75% воды. Она используется системами органов для транспортировки полезных веществ, регуляции температуры и растворения питательных соединений.
- 6. Интересные факты о химии касаются нашей планеты Земля. К примеру, за последних 5 веков ее масса увеличилась на целый миллиард тонн. Такой вес прибавили космические вещества.
- 7. Стенки мыльного пузыря – пожалуй, самая тонкая материя, которую человек способен увидеть невооруженным взглядом. Для примера, толщина папиросной бумаги или волоса в несколько тысяч раз толще.
- 8. Скорость лопания мыльного пузыря составляет 0.001 секунды. Скорость ядерной реакции – 0.000 000 000 000 000 001 секунды.
- 9. Железо, очень твердый и прочный материал в обычном его состоянии, становится газообразным при температуре 5 тысяч градусов Цельсия.
- 10. Всего за минуту Солнце вырабатывает энергии больше, чем наша планета расходует за целый год. Но мы не используем ее полностью. 19% солнечной энергии поглощает атмосфера, 34% возвращается в космос, а лишь 47% доходит до Земли.
- 11. Как ни странно, но лучше, чем воздух звук проводит гранит. Так, если бы между людьми была бы гранитная стена (сплошная), они бы слышали звуки на расстоянии одного километра. В обычной жизни в подобных условиях звук распространяется лишь на сто метров.
- 12. Шведский ученый Карл Шелле является рекордсменом по количеству открытых химических элементов. На его счету хлор, фтор, барий, вольфрам, кислород, марганец, молибден.
- Второе место разделили шведы Яком Берцелиус, Карл Монсандер, англичанин Гемфри Дэви и француз Поль Лекок де Буабордан. Им принадлежит открытие четверти всех известных современной науке элементов (то есть по 4 каждый).
- 13. Самый крупный самородок из платины – так называемый «Уральский гигант». Его вес составляет 7 килограммов и 860,5 граммов. Хранится этот гигант в Алмазном фонде Московского Кремля.
- 14. 16 сентября с 1994 года – Международный день охраны озонового слоя, согласно указу Генеральной ассамблеи ООН.
- 15. Углекислый газ, который широко используется для создания современных газированных напитков, был открыт английским учёным Джозефом Пристли еще в 1767 году. Тогда Пристли заинтересовали пузырьки, образуемые при брожении пива.
- 16. Танцующий кальмар – так называется удивительное блюдо в Японии. Недавно пойманного и убитого кальмара кладут в миску с рисом и перед клиентом поливают соевым соусом. При взаимодействии с натрием, который содержится в соевом соусе, нервные окончания даже убитого кальмара начинают реагировать. В результате такой химической реакции моллюск начинает «танцевать» прямо в тарелке.
- 17. Скатол – органическое соединение, которое отвечает за характерный запах фекалий. Интересен тот факт, что в больших дозах данное вещество имеет приятный цветочный аромат, который используют в пищевой промышленности и парфюмерии.
Интересные вопросы по химии. Интеллектуальная игра по химии для 8-х классов: «Эрудиты, вперед!»
Цели мероприятия:
- Расширить кругозор, активизировать опыт учащихся, развить логические и аналитические способности мышления.
- Мотивировать учащихся на успех и индивидуальное и коллективное творчество.
- Формировать и совершенствовать навыки самостоятельной и коллективной творческой работы.
- Формировать умения и навыки, которые носят в современных условиях общенаучный, общеинтеллектуальный характер.
- Воспитывать устойчивый интерес к изучаемому предмету – к химии.
“Просто знать – еще не все, знания нужно использовать”
И.В. Гете
Добрый день, дорогие ребята, уважаемые учителя! Мы рады приветствовать всех, кто собрался сегодня на нашу интеллектуальную игру: зрителей, жюри, и, конечно же, команды. Цель нашей игры – расширить кругозор знаний, полученных на начальном этапе изучения химии, повысить эрудицию, в увлекательной форме провести викторину по предмету. Выступление команд будет оценивать жюри. Пи выступлении команд будет учитываться не только глубина знаний, но и остроумие, находчивость, оригинальность ответов, активность и сплоченность. Пусть этот праздник откроет для каждого что-то новое и интересное, пусть запомнятся улыбки и шутки, крепче станет дружба между вами.
Команды по очереди выбирают себе область знаний и цену вопроса в соответствии с таблицей. Вопрос зачитывает ведущий. На обдумывание дается 5 – 10 с. При правильном ответе команда получает баллы в соответствии с ценой вопроса, при неправильном – такое же количество баллов снимается. Если команда, выбравшая вопрос затрудняется с ответом, то игра переходит в индивидуальную, и каждый участник игры может набирать баллы, подняв сигнальную карточку. Если на данный вопрос нет ответа, то его дает ведущий.
В “Синем” и “Красном” раундах предусмотрены по два вопроса “Кот в мешке”, обозначенные в перечне вопросов звездочкой. Команда, получившая такой вопрос, имеет право передать его другой команде.
Вопросы “Синего раунда”
| Металлы и неметаллы | 10 | 20 | 30 | 40 | 50 |
| Химические загадки | 10 | 20 | 30 | 40 | 50 |
| Закончите фразу | 10 | 20 | 30 | 40 | 50 |
| Верите ли вы, что… | 10 | 20 | 30 | 40 | 50 |
| Первоначальные химические понятия | 10 | 20 | 30 | 40 | 50 |
| Превращение без превращений | 10 | 20 | 30 | 40 | 50 |
| Узнай вещество или элемент | 10 | 20 | 30 | 40 | 50 |
Условия игры “Красный раунд”
Этот раунд проводится аналогично “синему”, но изменяются области знаний и цена вопроса в соответствии с таблицей, а также предусмотрены два вопроса “Своя игра”, обозначенные в перечне вопросов двумя звездочками. Команда, получившая такой вопрос, делает свою ставку, не превышающую суммы заработанных баллов. Другие команды тоже делают свои ставки, но отвечает та команда у которой ставка выше.
Химия вокруг нас интересные факты. Интересные факты о химии

Мы представим интересные факты о химии , понятные всем и каждому. Один из актуальных и полезных вопросов, касается метилового спирта.
Это вещество практически невозможно отличить от этилового спирта, но воздействие первого очень вредно для здоровья человека и его употребление может привести к летальному исходу.
Совсем небольшая доза метанола может лишить человека зрения, а употребление спирта от 30 мл приводит к смерти.
Теперь становится ясно, почему отравляются люди в случае употребления некачественного алкоголя. И что самое поразительное есть противоядие и это этиловый спирт.

Интересные факты о растворах химия. Химия — интересные факты
В 21 веке химия, наряду с математикой и физикой, проникла во все сферы жизни людей. Лекарства, зеркала, покрышки машин… Химические элементы окружают нас повсюду. Даже сам человек состоит из молекул и химических цепочек. Представляем интересные факты о химии.
Удивительное рядом
- Процесс перехода вещества из твёрдого состояния в газообразное в химии называется сублимацией.
- Для изготовления кваса используется реакция брожения.
- Если опустить в пересоленный суп марлю с рисом, блюдо можно спасти, так как за счёт абсорбции соль вытянется.
- В фекалиях содержится скатол, и именно из-за него они неприятно пахнут. Интересно то, что в небольших количествах скатол приятно пахнет, и его добавляют в сигареты и парфюм.
- 100000 – именно столько химических реакций проходят за секунду в мозге человека.
- В состав пластмассы для «Lego» входит сульфат бария. Это вещество совершенно безвредно для человеческого организма.
- 16 сентября – Международный день охраны такого химического элемента, как озон.
- Слезы у человека при нарезании лука вызывает содержащаяся в нём сера.
- Интересные факты о химических элементах. Множество элементов называют в честь стран – Америций, Индий, в честь городов – Иттербий, Берклий, Гольмий, в честь учёных – Бор, Менделевий.
- Дефлогистрированный воздух – принятое в науке название кислорода.
- Американец Чарльз Гудьир случайно открыл процесс вулканизации и создал прочную резину, которая не размягчается в жару и не трескается на холоде. Он просто забыл на горячей плите смесь серы и синтетического каучука.
- Во время стирки белья происходит гидролиз солей.
Источник: https://interesnyefakty.com/novosti/fakty-po-himii-interesnye-fakty-o-himii
Интересные исторические факты о химических элементах. Интересные и занимательные факты о некоторых химических элементах
— занимает первое место в периодической системе Менделеева, невесомый газ, образующий воду при соединении с кислородом.
Литий — это легчайший металл на земле, почти наполовину легче воды, а еще его можно разрезать ножом.
Скандий — используется с целью получения сверхтвёрдых веществ в индустрии.
Титан — не вызывает аллергических реакций и может быть использован в хирургии и для пирсинга.
Медь — губительна для бактерий. Оказывается, медные водопроводные трубы обладают дезинфицирующими качествами, а дверные ручки из этого материала — антибактериальными.
Теллур — токсичный элемент с запахом тухлого чеснока.
Ванадий — если его добавить в сталь или чугун, то сплав получит необычайную прочность.
Галлий — металлический элемент, у которого низкая температура плавления, всего 28 градусов. Если попытаться размешать галлиевой ложкой чай, то она растворится в стакане.
Сурьма — в древние времена использовалась в косметических целях для подводки глаз и бровей, а так же в качестве слабительного. На самом же деле, сурьма чрезвычайно токсична, а в современной промышленности из нее изготавливают сильнейшие кислоты, которыми можно прожечь стекло.
Европий — применяется для защиты от подделок денежных банкнот евро, которые считаются самой защищенной валютой в мире на сегодняшний день.
Азот — главный компонент воздуха, которым мы дышим, но при попадании в легкие в чистом виде способен вызвать летальный исход.
Сера — в чистом виде имеет неприятный запах, но является незаменимым элементом для человеческого организма и замедляет его старение.
Ртуть — единственный металл, который при комнатной температуре находится в жидком состоянии, и один из тяжелейших — 1 литр весит больше 13 кг.
Иридий — назван в честь древнегреческой богини радуги. Он один из наиболее прочных, тяжеловесных и редких металлов на земле. С его помощью смогли определить возраст древних динозавров и других палеонтологических ископаемых.
Осмий — наиболее тяжелое металлическое вещество на планете, которое практически не поддается обработке. Свое название обрел из-за мерзкого амбре, состоящего из смеси хлора и чесночных капель.
Интересные факты о химических элементах в организме человека. Интересные факты о неметаллах человеческого тела
Основа жизни на земле углерод. Именно из него состоят все органические молекулы, а значит и живые организмы, в том числе и тело человека. Неметаллы организма принято разделять на три группы:
- органогенные элементы, из которых состоят все ткани человеческого тела;
- макроэлементы: ежедневно человеку необходимы граммы, десятки граммов серы, фосфора, хлора;
- микроэлементы: их дозировка, нужная для нормальной работы организма, измеряется десятым, сотыми долями грамма или милиграмма.
Необходимых микроэлементов-неметаллов всего четыре: йод, кремний, фтор и селен. Из 24 элементов таблицы Менделеева в организме человека почти половина: одиннадцать неметаллов, без которых невозможна жизнь.
Углерод
Шестой элемент периодической системы входит в состав всех живых молекул. Его способность образовывать длинные цепочки незаменима для создания молекул ДНК, сложных белков. Число отдельных атомов углерода в молекулах доходит до десятков, сотен миллионов.

Человечеству известно несколько десятков миллионов веществ, которые образованы с участием углерода. Это в несколько раз больше, чем количество веществ, образованных всеми остальными элементами таблицы Менделеева. Этому макроэлементу посвящен отдельный раздел химии — органическая.
Источник: https://interesnyefakty.com/novosti/interesnye-fakty-v-razvitii-himii-interesnye-fakty-o-himii
Видео ИНТЕРЕСНЫЕ ФАКТЫ О ХИМИЧЕСКИХ ЭЛЕМЕНТАХ, О КОТОРЫХ ВЫ НЕ ЗНАЛИ!
interesnyefakty.com
Интересные факты химии. Интересные факты о химии
Интересные факты химии. Интересные факты о химии

Мы представим интересные факты о химии , понятные всем и каждому. Один из актуальных и полезных вопросов, касается метилового спирта.
Это вещество практически невозможно отличить от этилового спирта, но воздействие первого очень вредно для здоровья человека и его употребление может привести к летальному исходу.
Совсем небольшая доза метанола может лишить человека зрения, а употребление спирта от 30 мл приводит к смерти.
Теперь становится ясно, почему отравляются люди в случае употребления некачественного алкоголя. И что самое поразительное есть противоядие и это этиловый спирт.

Интересные факты о веществах. Необычные факты о химических элементах

Некоторые науки доступны лишь избранным. Это не тайное знание, просто нужно обладать соответствующим складом ума. Именно поэтому физики или химики выглядят инопланетянами среди офисного персонала или филологов. Вообще, глубокое погружение в какую-то науку вычленяет исследователя из окружающего мира. А ведь в любой научной дисциплине много интересного. Например, химические элементы.
Водород
Жидкий водород (гидроген) считается самым плотным веществом (жидкостью), а в газообразном — самым разреженным. Этого элемента в коре Земли содержится всего 0,15%,в то время как Солнце состоит из него примерно на 50%. Кстати, на планете самое распространенное соединение — монооксид дигидрогена.
Золото
Этот драгоценный металл находится практически везде. В тонне океанической воды можно собрать целых 7 мг. Даже в теле человека в теории находится порядка нескольких десятых миллиграмма. Это трагическая новость для тех, кто стремится обогатиться, но спасает миллионы жизней.
Серебро
Мы привыкли, что это «второй» по стоимости драгоценный металл. Поклонники украшений традиционно делятся на фанатов золота или серебра. А вот бактерицидные свойства серебряных изделий обнаружили случайно в армии Александра Македонского. В одном из походов среди солдат началась эпидемия кишечных болезней. При этом начальство оставалось здоровым, а воду пили одинаковую, потому что полководцы реально заботились о своих солдатах. Ответ был в посуде, из которой ели. Обычные военные ели из оловянных тарелок и поэтому заболели, а вот серебряная посуда нейтрализовала бактерии в пище и воде.
Жидкие металлы
Есть четыре металла, которые находятся в жидком состоянии при «комнатной температуре». То есть их не нужно специально нагревать, чтобы они спокойно переливались. Это ртуть, галлий, франций и цезий.
Платина
Сразу после выделения этого металла его называли «серебришко». Он слишком похож на обычное серебро и стоил в разы меньше. Видимо наши предки настолько привыкли обрабатывать именно серебро, что не стали высоко ценить его «аналог». Цена платины взлетела, когда открылись ее сферы применения (та же электроника или медицина).
А еще чистое железо может находиться в газообразном состоянии. Его нужно будет всего лишь нагреть до 50 000 градусов Цельсия.
Источник: https://interesnyefakty.com/novosti/interesnye-himicheskie-fakty-himiya-interesnye-fakty
Интересные факты о химических элементах в организме человека. Интересные факты о химических элементах
Как вещества, как известно, состоят из атомов. А разные виды атомов называются химическими элементами. В этом посте вы прочитаете множество интересных фактов о химических элементах.
Химических элементов значительно меньше, чем разных веществ. Стабильных элементов (атомы которых не распадаются со временем) всего 80, а также есть ещё несколько радиоактивных, но долгоживущих, которые тоже встречаются в природе. Всё многообразие веществ образуется из-за того, что атомы способны соединяться между собой. Положительно заряженные ядра атомов при сближении притягивают отрицательно заряженные электроны других атомов и из-за этого между атомами образуется устойчивая связь.
Атомы химических элементов отличаются друг от друга числом протонов в ядре атома. Протоны и нейтроны удерживаются в ядре ядерными силами, но электромагнитные силы пытаются отталкивать протоны друг от друга. Чем больше протонов в ядре, тем сильнее отталкивание, поэтому слишком большие ядра не могут долго существовать. Самый последний из химических элементов, атомы которого стабильны — свинец (номер 82), а самый последний, который встречается в природе — уран (номер 92). Все известные элементы с большими номерами получены искусственно в ядерных реакторах или на ускорителях. Самый же тяжёлый на сегодняшний день элемент, который получен искусственно, это унуноктий (номер 118). Его синтезировали российские учёные на ускорителе в Дубне. Все элементы с номером 100 и выше получены в очень малых количествах (иногда лишь в количестве нескольких атомов).
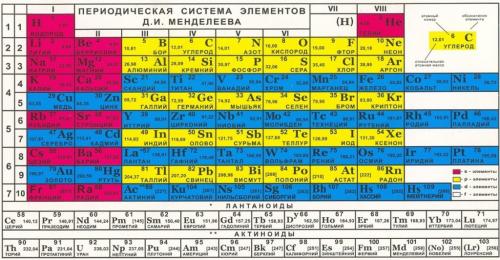
Согласно современным представлениям все элементы тяжелее водорода и гелия образовались в процессе эволюции звёзд. Ядра атомов от водорода до железа способны сливаться друг с другом с выделением энергии и постепенно образуются в течение жизни звезды. А вот все химические элементы, атомы которых тяжелее железа, как считают учёные, образовались при взрывах сверхновых или нейтронных звёзд.
Самый первый химический элемент — водород. Он является самым распространённым во Вселенной, более 90% атомов — это атомы водорода. Но на Земле водорода не так много, а самый распространённый элемент — кислород. В земной коре около 50% кислорода, затем идут кремний (26% по массе) и алюминий (7%).
Даже чистые химические элементы могут существовать в виде разных веществ, т к. атомы в них могут соединяться по-разному. Это явление называется аллотропией.

пример аллотропии — кристаллический бор (слева) и аморфный бор
Химические элементы очень сильно отличаются друг от друга по способности вступать в химические реакции. Самые химически пассивные элементы — инертные газы, особенно гелий. Всё потому, что у них полностью заполнена внешняя электронная оболочка. Гелий и неон вообще не образуют настоящих химических соединений. Также малой химической активностью отличаются т. н. благородные металлы — золото, серебро, платина и металлы платиновой группы.
Самые активные химические элементы — те, которые легко отдают или присоединяют электроны. Самый активный металл — цезий, а самый активный неметалл — фтор.
Цезий настолько активен, что самопроизвольно загорается на воздухе и взрывается в воде.
Фтор настолько активен, что реагирует почти со всеми известными веществами. В этом газе загораются даже такие вещества, как песок и вода. Фтор настолько опасен, что многие химики, пытаясь получить его в чистом виде, погибли во время опытов.
Из всех химических элементов в чистом виде 11 элементов при нормальных условиях — газы, а почти все остальные — твёрдые вещества. Лишь ртуть и бром — жидкости.
По своим свойствам многие химические элементы в чём-то похожи друг на друга. Например, среди них выделяют такие группы, как щелочные металлы, галогены, инертные газы и т. д. В то же время практически любой известный химический элемент в чём-то уникален и в некоторых областях применения незаменим. Например, титан, на основе которого делают сверхпрочные сплавы, незаменим в авиастроении. Кремний незаменим в микроэлектронике. Литий незаменим в производстве компактных аккумуляторов. Цезий незаменим как материал для инфракрасных датчиков. Уран незаменим в атомной промышленности.
Организм человека состоит из более, чем 30 химических элементов, при недостатке которых он не может нормально функционировать. Например, из соединений кальция состоят кости, железо входит в состав гемоглобина крови, йод нужен для синтеза гормонов щитовидной железы и т. д.
Интересные исторические факты о химических элементах. Интересные и занимательные факты о некоторых химических элементах
— занимает первое место в периодической системе Менделеева, невесомый газ, образующий воду при соединении с кислородом.
Литий — это легчайший металл на земле, почти наполовину легче воды, а еще его можно разрезать ножом.
Скандий — используется с целью получения сверхтвёрдых веществ в индустрии.
Титан — не вызывает аллергических реакций и может быть использован в хирургии и для пирсинга.
Медь — губительна для бактерий. Оказывается, медные водопроводные трубы обладают дезинфицирующими качествами, а дверные ручки из этого материала — антибактериальными.
Теллур — токсичный элемент с запахом тухлого чеснока.
Ванадий — если его добавить в сталь или чугун, то сплав получит необычайную прочность.
Галлий — металлический элемент, у которого низкая температура плавления, всего 28 градусов. Если попытаться размешать галлиевой ложкой чай, то она растворится в стакане.
Сурьма — в древние времена использовалась в косметических целях для подводки глаз и бровей, а так же в качестве слабительного. На самом же деле, сурьма чрезвычайно токсична, а в современной промышленности из нее изготавливают сильнейшие кислоты, которыми можно прожечь стекло.
Европий — применяется для защиты от подделок денежных банкнот евро, которые считаются самой защищенной валютой в мире на сегодняшний день.
Азот — главный компонент воздуха, которым мы дышим, но при попадании в легкие в чистом виде способен вызвать летальный исход.
Сера — в чистом виде имеет неприятный запах, но является незаменимым элементом для человеческого организма и замедляет его старение.
Ртуть — единственный металл, который при комнатной температуре находится в жидком состоянии, и один из тяжелейших — 1 литр весит больше 13 кг.
Иридий — назван в честь древнегреческой богини радуги. Он один из наиболее прочных, тяжеловесных и редких металлов на земле. С его помощью смогли определить возраст древних динозавров и других палеонтологических ископаемых.
Осмий — наиболее тяжелое металлическое вещество на планете, которое практически не поддается обработке. Свое название обрел из-за мерзкого амбре, состоящего из смеси хлора и чесночных капель.
Интересные факты и опыты по химии. Химия — интересные факты
В 21 веке химия, наряду с математикой и физикой, проникла во все сферы жизни людей. Лекарства, зеркала, покрышки машин… Химические элементы окружают нас повсюду. Даже сам человек состоит из молекул и химических цепочек. Представляем интересные факты о химии.
Удивительное рядом
- Процесс перехода вещества из твёрдого состояния в газообразное в химии называется сублимацией.
- Для изготовления кваса используется реакция брожения.
- Если опустить в пересоленный суп марлю с рисом, блюдо можно спасти, так как за счёт абсорбции соль вытянется.
- В фекалиях содержится скатол, и именно из-за него они неприятно пахнут. Интересно то, что в небольших количествах скатол приятно пахнет, и его добавляют в сигареты и парфюм.
- 100000 – именно столько химических реакций проходят за секунду в мозге человека.
- В состав пластмассы для «Lego» входит сульфат бария. Это вещество совершенно безвредно для человеческого организма.
- 16 сентября – Международный день охраны такого химического элемента, как озон.
- Слезы у человека при нарезании лука вызывает содержащаяся в нём сера.
- Интересные факты о химических элементах. Множество элементов называют в честь стран – Америций, Индий, в честь городов – Иттербий, Берклий, Гольмий, в честь учёных – Бор, Менделевий.
- Дефлогистрированный воздух – принятое в науке название кислорода.
- Американец Чарльз Гудьир случайно открыл процесс вулканизации и создал прочную резину, которая не размягчается в жару и не трескается на холоде. Он просто забыл на горячей плите смесь серы и синтетического каучука.
- Во время стирки белья происходит гидролиз солей.
Интересные вопросы по химии. Интеллектуальная игра по химии для 8-х классов: «Эрудиты, вперед!»
Цели мероприятия:
- Расширить кругозор, активизировать опыт учащихся, развить логические и аналитические способности мышления.
- Мотивировать учащихся на успех и индивидуальное и коллективное творчество.
- Формировать и совершенствовать навыки самостоятельной и коллективной творческой работы.
- Формировать умения и навыки, которые носят в современных условиях общенаучный, общеинтеллектуальный характер.
- Воспитывать устойчивый интерес к изучаемому предмету – к химии.
“Просто знать – еще не все, знания нужно использовать”
И.В. Гете
Добрый день, дорогие ребята, уважаемые учителя! Мы рады приветствовать всех, кто собрался сегодня на нашу интеллектуальную игру: зрителей, жюри, и, конечно же, команды. Цель нашей игры – расширить кругозор знаний, полученных на начальном этапе изучения химии, повысить эрудицию, в увлекательной форме провести викторину по предмету. Выступление команд будет оценивать жюри. Пи выступлении команд будет учитываться не только глубина знаний, но и остроумие, находчивость, оригинальность ответов, активность и сплоченность. Пусть этот праздник откроет для каждого что-то новое и интересное, пусть запомнятся улыбки и шутки, крепче станет дружба между вами.
Команды по очереди выбирают себе область знаний и цену вопроса в соответствии с таблицей. Вопрос зачитывает ведущий. На обдумывание дается 5 – 10 с. При правильном ответе команда получает баллы в соответствии с ценой вопроса, при неправильном – такое же количество баллов снимается. Если команда, выбравшая вопрос затрудняется с ответом, то игра переходит в индивидуальную, и каждый участник игры может набирать баллы, подняв сигнальную карточку. Если на данный вопрос нет ответа, то его дает ведущий.
В “Синем” и “Красном” раундах предусмотрены по два вопроса “Кот в мешке”, обозначенные в перечне вопросов звездочкой. Команда, получившая такой вопрос, имеет право передать его другой команде.
Вопросы “Синего раунда”
| Металлы и неметаллы | 10 | 20 | 30 | 40 | 50 |
| Химические загадки | 10 | 20 | 30 | 40 | 50 |
| Закончите фразу | 10 | 20 | 30 | 40 | 50 |
| Верите ли вы, что… | 10 | 20 | 30 | 40 | 50 |
| Первоначальные химические понятия | 10 | 20 | 30 | 40 | 50 |
| Превращение без превращений | 10 | 20 | 30 | 40 | 50 |
| Узнай вещество или элемент | 10 | 20 | 30 | 40 | 50 |
Этот раунд проводится аналогично “синему”, но изменяются области знаний и цена вопроса в соответствии с таблицей, а также предусмотрены два вопроса “Своя игра”, обозначенные в перечне вопросов двумя звездочками. Команда, получившая такой вопрос, делает свою ставку, не превышающую суммы заработанных баллов. Другие команды тоже делают свои ставки, но отвечает та команда у которой ставка выше.
interesnyefakty.com
Факты по химии. Интересные факты о химии
Факты по химии. Интересные факты о химии

Мы представим интересные факты о химии , понятные всем и каждому. Один из актуальных и полезных вопросов, касается метилового спирта.
Это вещество практически невозможно отличить от этилового спирта, но воздействие первого очень вредно для здоровья человека и его употребление может привести к летальному исходу.
Совсем небольшая доза метанола может лишить человека зрения, а употребление спирта от 30 мл приводит к смерти.
Теперь становится ясно, почему отравляются люди в случае употребления некачественного алкоголя. И что самое поразительное есть противоядие и это этиловый спирт.

Интересные вопросы по химии. Интеллектуальная игра по химии для 8-х классов: «Эрудиты, вперед!»
Цели мероприятия:
- Расширить кругозор, активизировать опыт учащихся, развить логические и аналитические способности мышления.
- Мотивировать учащихся на успех и индивидуальное и коллективное творчество.
- Формировать и совершенствовать навыки самостоятельной и коллективной творческой работы.
- Формировать умения и навыки, которые носят в современных условиях общенаучный, общеинтеллектуальный характер.
- Воспитывать устойчивый интерес к изучаемому предмету – к химии.
“Просто знать – еще не все, знания нужно использовать”
И.В. Гете
Добрый день, дорогие ребята, уважаемые учителя! Мы рады приветствовать всех, кто собрался сегодня на нашу интеллектуальную игру: зрителей, жюри, и, конечно же, команды. Цель нашей игры – расширить кругозор знаний, полученных на начальном этапе изучения химии, повысить эрудицию, в увлекательной форме провести викторину по предмету. Выступление команд будет оценивать жюри. Пи выступлении команд будет учитываться не только глубина знаний, но и остроумие, находчивость, оригинальность ответов, активность и сплоченность. Пусть этот праздник откроет для каждого что-то новое и интересное, пусть запомнятся улыбки и шутки, крепче станет дружба между вами.
Команды по очереди выбирают себе область знаний и цену вопроса в соответствии с таблицей. Вопрос зачитывает ведущий. На обдумывание дается 5 – 10 с. При правильном ответе команда получает баллы в соответствии с ценой вопроса, при неправильном – такое же количество баллов снимается. Если команда, выбравшая вопрос затрудняется с ответом, то игра переходит в индивидуальную, и каждый участник игры может набирать баллы, подняв сигнальную карточку. Если на данный вопрос нет ответа, то его дает ведущий.
В “Синем” и “Красном” раундах предусмотрены по два вопроса “Кот в мешке”, обозначенные в перечне вопросов звездочкой. Команда, получившая такой вопрос, имеет право передать его другой команде.
Вопросы “Синего раунда”
| Металлы и неметаллы | 10 | 20 | 30 | 40 | 50 |
| Химические загадки | 10 | 20 | 30 | 40 | 50 |
| Закончите фразу | 10 | 20 | 30 | 40 | 50 |
| Верите ли вы, что… | 10 | 20 | 30 | 40 | 50 |
| Первоначальные химические понятия | 10 | 20 | 30 | 40 | 50 |
| Превращение без превращений | 10 | 20 | 30 | 40 | 50 |
| Узнай вещество или элемент | 10 | 20 | 30 | 40 | 50 |
Условия игры “Красный раунд”
Этот раунд проводится аналогично “синему”, но изменяются области знаний и цена вопроса в соответствии с таблицей, а также предусмотрены два вопроса “Своя игра”, обозначенные в перечне вопросов двумя звездочками. Команда, получившая такой вопрос, делает свою ставку, не превышающую суммы заработанных баллов. Другие команды тоже делают свои ставки, но отвечает та команда у которой ставка выше.
Интересные факты о Растворах химия. Факты о Растворах и смесях
Раствор — это жидкость, в которой растворено твердое вещество.

• Водопроводная вода редко бывает чистой, обычно она содержит примеси других веществ. Это делает ее раствором.
• Когда твердое вещество растворяется, его молекулы отделяются друг от друга и полностью перемешиваются с молекулами жидкости.
• Жидкость в растворе называется растворителем.
• Чем больше твердого вещества растворяется в данном объеме жидкости, тем концентрированнее становится раствор, пока твердое вещество не перестанет растворяться.
• Растворы, содержащие предельное количество растворенного вещества, называют насыщенными.
Морская вода — это раствор, содержащий огромное число разных растворенных веществ в малых концентрациях. Среди них поваренная соль (хлорид натрия) и хлорид магния.
• Если насыщенный раствор нагреть, то в нем можно растворить дополнительное количество твердого вещества, т.е. растворимость большинства веществ возрастает с увеличением температуры.
• Если насыщенный раствор охладить или оставить испаряться, то растворенное вещество выпадет в осадок. Молекулы выпадающего в осадок вещества часто объединяются в твердые кристаллы.
Факты о Растворах и смесях
• Раствор — это жидкость, в которой растворено твердое вещество.
• Водопроводная вода редко бывает чистой, обычно она содержит примеси других веществ. Это делает ее раствором.
• Когда твердое вещество растворяется, его молекулы отделяются друг от друга и полностью перемешиваются с молекулами жидкости.
• Жидкость в растворе называется растворителем.
• Чем больше твердого вещества растворяется в данном объеме жидкости, тем концентрированнее становится раствор, пока твердое вещество не перестанет растворяться.
• Растворы, содержащие предельное количество растворенного вещества, называют насыщенными.
Морская вода — это раствор, содержащий огромное число разных растворенных веществ в малых концентрациях. Среди них поваренная соль (хлорид натрия) и хлорид магния.
• Если насыщенный раствор нагреть, то в нем можно растворить дополнительное количество твердого вещества, т.е. растворимость большинства веществ возрастает с увеличением температуры.
• Если насыщенный раствор охладить или оставить испаряться, то растворенное вещество выпадет в осадок. Молекулы выпадающего в осадок вещества часто объединяются в твердые кристаллы.
Химия вокруг нас интересные факты. Химия — интересные факты
В 21 веке химия, наряду с математикой и физикой, проникла во все сферы жизни людей. Лекарства, зеркала, покрышки машин… Химические элементы окружают нас повсюду. Даже сам человек состоит из молекул и химических цепочек. Представляем интересные факты о химии.
Удивительное рядом
- Процесс перехода вещества из твёрдого состояния в газообразное в химии называется сублимацией.
- Для изготовления кваса используется реакция брожения.
- Если опустить в пересоленный суп марлю с рисом, блюдо можно спасти, так как за счёт абсорбции соль вытянется.
- В фекалиях содержится скатол, и именно из-за него они неприятно пахнут. Интересно то, что в небольших количествах скатол приятно пахнет, и его добавляют в сигареты и парфюм.
- 100000 – именно столько химических реакций проходят за секунду в мозге человека.
- В состав пластмассы для «Lego» входит сульфат бария. Это вещество совершенно безвредно для человеческого организма.
- 16 сентября – Международный день охраны такого химического элемента, как озон.
- Слезы у человека при нарезании лука вызывает содержащаяся в нём сера.
- Интересные факты о химических элементах. Множество элементов называют в честь стран – Америций, Индий, в честь городов – Иттербий, Берклий, Гольмий, в честь учёных – Бор, Менделевий.
- Дефлогистрированный воздух – принятое в науке название кислорода.
- Американец Чарльз Гудьир случайно открыл процесс вулканизации и создал прочную резину, которая не размягчается в жару и не трескается на холоде. Он просто забыл на горячей плите смесь серы и синтетического каучука.
- Во время стирки белья происходит гидролиз солей.
Интересные исторические факты о химических элементах. Интересные факты о таблице Менделеева
Благодаря Генеральной Ассамблее ООН 2019 официально стал Международным годом таблицы Менделеева. Расскажем несколько интересных фактов о периодической таблице химических элементов.
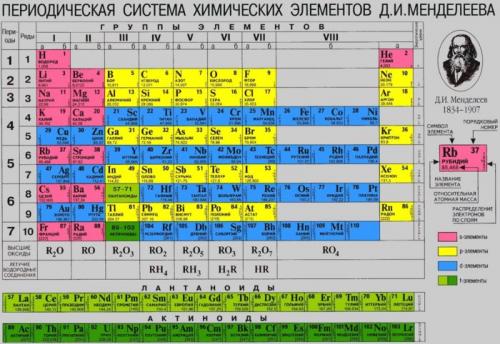
Таблица Менделеева
Родители смогут вспомнить школьную программу, а школьники узнают полезную информацию для расширения кругозора и успехов на уроках и олимпиадах по химии.
Интересные факты об истории таблицы Менделеева
Факт #1. Создателем таблицы считается Дмитрий Менделеев, но до него похожую схему представил научному сообществу Джон Ньюленд. Правда, его не восприняли всерьез.
Факт #2. Российский ученый Дмитрий Иванович впервые опубликовал свой вариант таблицы в 1869 году, окончательный вид с доработками и улучшениями открытие приобрело только в 1871 году.
Факты об элементах таблицы Менделеева
У большинства элементов таблицы Менделеева есть своя увлекательная история открытия и необычные свойства. Опишем некоторые из них.
Факт #1 . Благодаря урану (U) ученый Анри Беккерель получил Нобелевскую премию. Он понял, что вещество радиоактивно, когда случайно положил соли урана на фотопластинку. А еще уран — последний по номеру природный элемент в таблице, остальные вещества можно создать только искусственным путем.
Факт #2 . 200 лет назад исследователи Льюис и Кларк прошли через всю Америку к Тихому океану. Они взяли с собой в путь ртутное слабительное. А современные ученые по следам ртути (Hg), которая со временем не разлагается, смогли узнать точное место лагеря путешественников.
Факт #3 . Галлий (Ga) стал первым пробелом в таблице, заполненным уже после смерти ученого. Металлический галлий известен тем, что он сохраняет твердость при комнатной температуре, но в руках плавится.
Факт #4. Одни наименования химических элементов произошли от латинских слов, связанных со свойствами веществ. Некоторые элементы получили названия в честь ученых. А часть веществ носит имена героев мифов.
Факт #5. Элемент титан (Ti) назвали именем могучих сыновей богини Геи . Это один из самых твердых металлов. А его диаксид переливаетсямвсеми цветами радуги.
Факт #6. Тантал (Ta) носит имя героя древнегреческих мифов , совершившего несколько непростительных преступлений.
Факт #7. Торий (Th) назвали в честь бога грома Тора.
Факт #8. Ванадий (V) отличается соединениями с необычной окраской, поэтому назван именем древнескандинавской богини красоты.
Факт #9. Уран (U), Нептуний (Np) и Плутоний (Pu) также носят имена богов Урана, Нептуна (Посейдона) и Плутона (Аида).
Мифы о таблице Менделеева
Факт #1. Периодическая таблица химических элементов также известна распространенными мифами. Самый популярный гласит, что ученый однажды увидел сразу всю таблицу во сне. Но исследование жизни Менделеева говорит о том, что на самом деле он потратил немало времени и сил на свое открытие.
Факт #2. По другой легенде буквы армянского алфавита связаны с таблицей Менделеева. В разборе армянских названий таких веществ, как золото, серебро, свинец и ртуть, некая связь действительно прослеживается. Но это, скорее, совпадение. Армянские ученые вряд ли могли заранее предугадать открытие всех элементов таблицы.
Открытие Менделеева — огромный вклад в науку. И хороший повод для появления интересных фактов и мифов. А что еще вы знаете о таблице Менделеева? Пишите свои дополнения в комментариях.
Интересные факты о химических элементах в организме человека. Химический состав человека
«Всё- химия»- выражение, которое чаще всего можно услышать от преподавателей химии в школе, тем не менее, оно правильно. Так как, в конечном счёте, абсолютно всё состоит из химических элементов. Наше тело- тоже.
1. Кислород. Он не только существенная часть вдыхаемого нами воздуха и питьевой воды, он так же занимает значимое место в нашем теле. С 65 % общей массы нашего тела, кислород, самый важный химический элемент в составе человеческого организма.
2. Углерод может похвастаться не только самым большим количеством химических соединений в периодической системе, (самые известные из них- уголь и нефть). Он так же занимает почётное второе место в нашем списке.
3. Водород, как и кислород- составной элемент воздуха и питьевой воды. И он также относится к основным компонентам человеческого тела. 10% нашего веса состоят из водорода.
4. Несмотря на то, что азот также содержится в воздухе, он более известен как теплоноситель, в жидкой форме. Всё же, его таинственно испаряющейся газы не должны вводить в заблуждение- 3 % массы нашего тела состоят из азота.
5. Даже если он и составляет всего 1,5 %, кальций- важный металл в нашем организме. Именно он придаёт прочность нашим костям и зубам.
6. Фосфор, как светящееся вещество, известен каждому. Но далеко не каждый знает, что именно благодаря фосфору в организме, происходит образование ДНК, основы человеческой жизни.
7. Калий, со скромными 0,2 %, принимает небольшое участие в процессах организма. Он относится к электролитам, в которых наше тело нуждается, прежде всего, при спорте. Его недостаток может вызвать чувство истощения и судороги.
8. Может ли сера, с её неприятным видом и запахом, быть важной для нашего организма? Да, это именно так. Сера- существенная составная часть аминокислот и коферментов.
9. Сначала сера, теперь хлор. Можно подумать, наш организм состоит из одних ядов. Разумеется, элементарного хлора в нашем теле нет, зато есть хлорид. И он для нас жизненно важен, так как, содержится, например, в плазме крови.
10. Натрий мы потребляем, прежде всего, в форме хлорида натрия, так же известного как поваренная соль. Элемент важен для защиты клеток и движения нервных сигналов.
11. Магний жизненно необходим для всех организмов на земле, естественно, для нас людей, тоже. Вопреки его незначительной части- 0,05 % массы нашего тела, недостаток магния ведет к отчётливо ощутимым последствиям: Нервозность, головные боли, усталость и судороги мышц являются только некоторыми из них.
12. Мужской организм содержит больше железа, чем женский. Одна из причин этому- разница в питании. Другая- женщины теряют железо во время менструации. Поэтому средняя масса этого элемента в человеческом теле варьирует от 2 до 5 грамм.
13. Кобальт- составная часть витамина B12, который необходим для существования человека. Передозировка кобальта ведёт к многочисленным болезням, к раковым опухолям в том числе.
14. Для микроорганизмов медь смертельна даже в незначительных количествах, но человеку она нужна для образования жизненно-важных ферментов. Тяжелый металл составляет 0,05 % массы нашего тела. Мы получаем её через овощи, шоколад и орехи.
15. Цинк относится к элементам, которые нужны всем живым существам на земле. Он важен для обмена веществ и содержится во многих важных ферментах.
16. Йод- составляющая часть гормонов тироксин и трийодтиронин, которые производит щитовидная железа. Недостаток йода может вызвать тяжёлые нарушения в обмене веществ.
17. Селен относится к незаменимым микроэлементам. В тоже время, при передозировке, он сильно токсичен, поэтому его употребление как БАД, вызывает большие дискуссии в кругах учёных.
Видео топ 5 химических фактов. Химия – просто
interesnyefakty.com
Интересная органическая химия. Интересные факты о химии.
В эту самую минуту
Пока Вы читаете данную статью, Ваши глаза используют органическое соединение – ретиналь, который преобразует световую энергию в нервные импульсы. Пока Вы сидите в удобной позе, мышцы спины поддерживают правильную осанку благодаря химическому расщеплению глюкозы с высвобождением требуемой энергии. Как Вы понимаете, пробелы между нервными клетками так же заполнены органическими веществами – медиаторами (или нейространсмиттерами), которые помогают всем нейронам стать одним целым. И данная слаженная система работает без участия Вашего сознания! Так глубоко, как биологи, только химики-органики понимают, насколько филигранно создан человек, как логично устроены внутренние системы органов и их жизненный цикл. Отсюда следует, что изучение органической химии – основа понимания нашей жизни! А качественное изучение – это путь в будущее, ибо новые лекарства создаются прежде всего в химических лабораториях. Наша кафедра желает познакомить Вас поближе с этой прекрасной наукой.
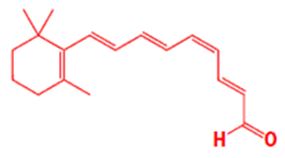 11-цис-ретиналь, поглощает свет
11-цис-ретиналь, поглощает свет
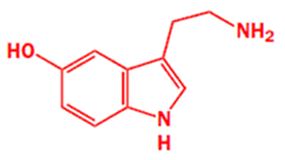 серотонин – нейромедиатор
серотонин – нейромедиатор
Органическая химия как наука
Органическая химия как наука возникла в конце девятнадцатого века. Она возникла на перекрещивании разных сфер жизни – от получения пищи до лечения миллионов людей, не подозревающих о роли химии в их жизни. Химия занимает уникальное место в структуре понимания Вселенной. Это наука о молекулах, но органическая химия является чем-то большим, чем это определение. Органическая химия в буквальном смысле сама себя создает, словно растет. Органическая химия, занимаясь изучением не только природных молекул имеет возможность самой создавать новые вещества, структуры, материи. Данная особенность подарила человечеству полимеры, красители для одежды, новые лекарства, духи. Некоторые считают, что синтетические материалы могут нанести вред человеку, либо быть экологически опасными. Однако, как порой отличить черное от белого, так и установить тонкую грань между «опасностью для человека» и «коммерческой выгодой» очень сложно. В этом вопросе так же поможет кафедра Органического синтеза и нанотехнологий (ОСиНТ).
Органические соединения
Органическая химия формировалась, как наука о жизни, ранее считалось, что она сильно отличается от неорганической химии в лаборатории. Затем ученые полагали, что органическая химия – это химия Углерода, особенно соединений каменного угля. В наше время органическая химия объединяет все соединения Углерода как живой, так и не живой природы.
Доступные для нас органические соединения получаются либо из живых организмов, либо из ископаемых материалов (нефть, уголь). Примером субстанций из природных источников являются эфирные масла – ментол (вкус мяты) и цис-жасмон (аромат цветков жасмина). Эфирные масла получают перегонкой с водяным паром; подробности раскроются при обучении на нашей кафедре.
-

- Ментол
-

- Цис-жасмон
-

- Хинин
Уже в 16 веке был известен алкалоид – хинин, который получают из коры хинного дерева (Южная Америка) и используют против малярии.
Иезуиты, что открыли данное свойство хинина, конечно же не знали его структуры. Тем более в те времена не стоял вопрос о синтетическом получении хинина – что удалось осуществить только в 20 столетии! Ещё любопытная история, связанная с хинином – это открытие фиолетового пигмента мовеина Уильямом Перкиным в 1856 году. Зачем он это сделал и какие результаты его открытия – так же можно узнать на нашей кафедре.
Но вернемся к истории становления органической химии. В 19 веке (времена У. Перкина) основным источником сырья для химической промышленности был уголь. Сухая перегонка угля давала коксовый газ, который использовался для обогрева и приготовления пищи, каменноугольную смолу, богатую на ароматические карбоциклические и гетероциклические соединения (бензол, фенол, анилин, тиофен, пиридин). На нашей кафедре Вам расскажут, чем они отличаются и какое они имеют значение в органическом синтезе.
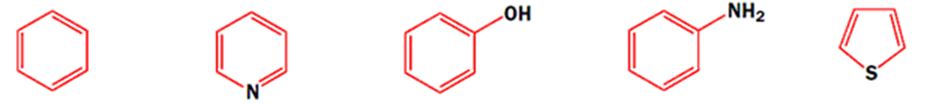
Бензол, пиридин, фенол, анилин, тиофен
Фенол обладает антисептическими свойствами (тривиальное название – карболовая кислота), а анилин стал основой развития красочной промышленности (получение анилиновых красителей). Данные красящие вещества по-прежнему коммерчески доступны, например, Бисмарк-Браун (коричневый) показывает, что большая часть ранних трудов по химии была проведена в Германии:
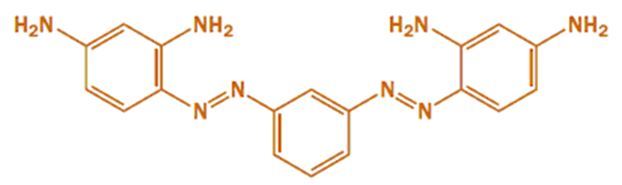
Бисмарк-Браун
Однако в 20 столетии, нефть опередила уголь в качестве основного источника органического сырья и энергии, поэтому газообразные метан (природный газ), этан, пропан стали доступным энергетическим ресурсом.
В тоже время, химическая промышленность разделилась на массовую и тонкую. Первая занимается производством красок, полимеров – веществ, не имеющих сложное строение, однако, производимых в огромном количестве. А тонкая химическая промышленность, правильнее сказать – тонкий органический синтез занимается получением лекарств, ароматов, вкусовых добавок, в гораздо меньших объемах, что, однако более прибыльно. В настоящее время известно около 16 миллионов органических соединений. Сколько ещё возможно? В этой области, органический синтез не имеет ограничений. Представьте себе, что Вы создали самую длинную алкильную цепь, однако Вы можете легко добавить ещё один углеродный атом. Этот процесс бесконечен. Но не следует думать, что все эти миллионы соединений – обычные линейные углеводороды; они охватывают все виды молекул с удивительно разнообразными свойствами.

Алифатические соединения
Свойства органических соединений
Каковы же физические свойства органических соединений?
Они могут быть кристаллическими как сахар, или пластичными как парафин, взрывоопасными как изооктан, летучими как ацетон.
-

- Сахароза
-

- Изооктан (2,3,5-триметилпентан)
Окраска соединений так же может быть самая разнообразная. Человечество уже столько синтезировало красителей, что создается впечатление, что уже не осталось таких цветов, какие нельзя получить с помощью синтетических красителей.
К примеру, можно составить такую таблицу ярко окрашенных веществ:
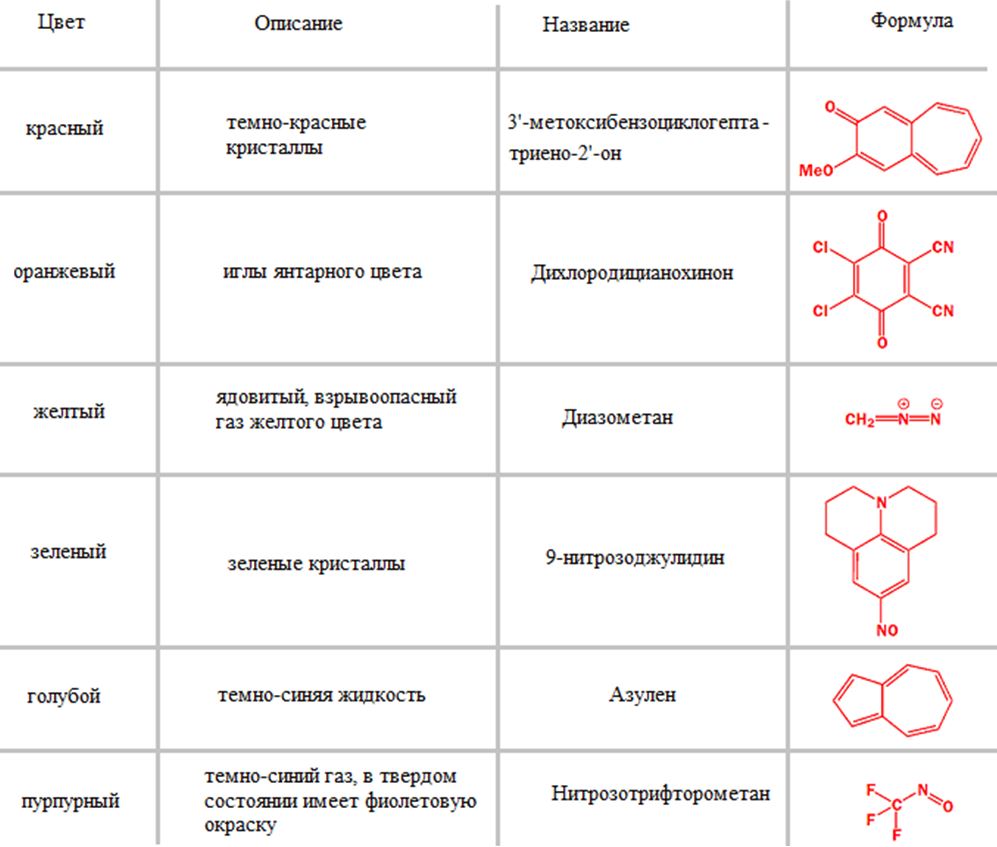
Однако кроме этих характеристик, органические вещества обладают запахом, который помогает их дифференцировать. Любопытный пример – защитная реакция скунсов. Запах секрета скунсов обуславливают сернистые соединения – тиолы:

Компоненты секретов скунсов
Но самый ужасный запах был «унюхан» в городе Фрайбурге (1889), во время попытки синтеза тиоацетона разложением тримера, когда пришлось эвакуировать население города, поскольку «неприятный запах, которых быстро распространился по большой площади в городе, вызывает обмороки, рвоту и тревожные состояния». Лабораторию закрыли.
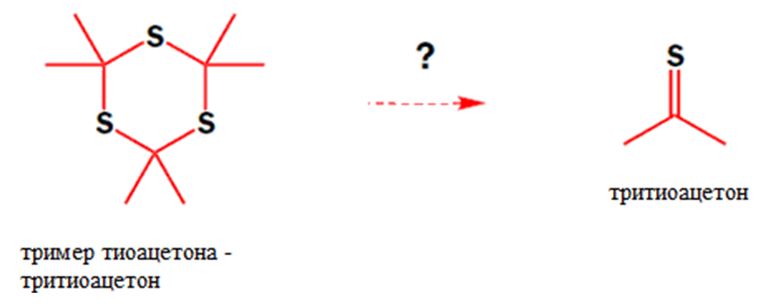
Но этот опыт решили повторить химики научной станции Ессо (Esso) к югу от Оксфорда. Передадим им слово:
«В последнее время, проблемы запаха вышли за пределы наших худших ожиданий. Во времена ранних экспериментов, пробка выскочила из бутылки с отходами и сразу была заменена, а наши колеги из соседней лаборатории (200 ярдов) немедленно почувствовали тошноту и рвоту.
Двое из наших химиков, которые просто изучали крекинг незначительных количеств тритиоацетона нашли себя как объект враждебных взглядов в ресторане и были посрамлены, когда официантка распылила дезодорант вокруг них. Запахи «бросили вызов» ожидаемым эффектам разбавления, поскольку работники лаборатории не считали запахи невыносимыми… и по-настоящему отрицали свою ответственность, так как они работали в закрытых системах. Чтобы убедить их в обратном, они были распределены с другими наблюдателями по всей территории лаборатории на расстояниях до четверти мили. Затем одна капля ацетон гем-дитиола, а позже маточного раствора перекристаллизации тритиоацетона была размещена на часовом стекле в вытяжном шкафу. Запах был обнаружен по ветру в считанные секунды». Т.е. запах этих соединений усиливается при понижении концентрации.
Существует два претендета на эту ужасную вонь – дитиол пропан (вышеуказанный гем-дитиол), либо 4-метил-4сульфанил-пентанон-2:
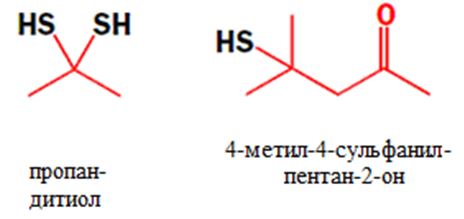
Вряд ли кто-то найдется чтобы определить из них лидера.
Однако, неприятный запах имеет свою область применения. Природный газ, что поступает в наши дома содержит небольшое количество ароматизатора – третбутил тиола. Небольшое количество – это столько, что люди способны почувствовать одну часть тиола в 50 миллиардах частей метана.
Напротив, некоторые другие соединения имеют восхитительные запахи. Чтобы искупить честь сернистых соединений мы должны сослаться на трюфель, который хрюшки могут унюхать через метр почвы и чей вкус и запах настолько восхитительны что они стоят дороже, чем золото. За аромат роз отвечают дамаскеноны. Если Вы имеете возможность понюхать запах одной капли, то Вы, вероятно, будете разочарованы, так как она пахнет как скипидар, или камфора. А на следующее утро Ваша одежда (и Вы в том числе) будете очень сильно благоухать розами. Так же, как и тритиоацетон, этот запах усиливается при разведении.

Компонент аромата трюфелей
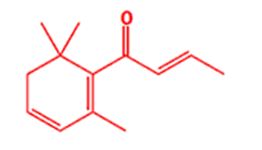
Демаскенон – аромат роз
А как насчет вкуса?
Всем известно, что дети могут попробовать на вкус бытовую химию (средство для чистки ванны, туалета и т.д.). Перед химиками встала задача, чтобы несчастные дети больше не захотели попробовать какую-то химию в яркой упакове. Обратите внимание, что это сложное соединение является солью:
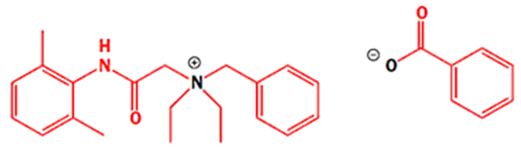
Битрекс денатониум бензоат
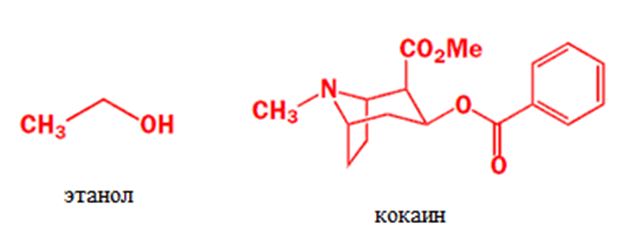
Некоторые другие вещества оказывают «странное» воздействие на человека, вызывая комплексы психических ощущений – галюцинации, эйфорию и т.д. К ним относятся наркотики, этиловый спирт. Они очень опасны, т.к. вызывают зависимость и уничтожают человека как личность.
Давайте не забывать и о других существах. Известно, что кошки любят спать в любое время. Недавно ученые получили из спинномозговой жидкости бедных кошек вещество, позволяющее им быстро засыпать. Оно так же действует и на человека. Это удивительно простое соединение:
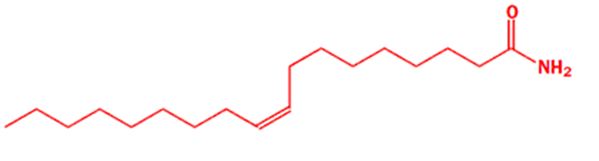
Инициатор сна – цис-9,10-октадеценоамид
Подобная структура, носящая название Коньюгированная Линолевая Кислота (КЛК) обладает противоопухолевыми свойствми:
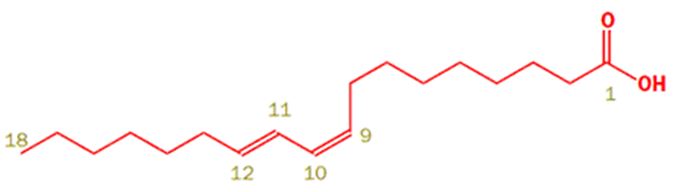
КЛК- противораковое средство цис-9-транс-11 сопряженная линолевая кислота
Ещё одна любопытная молекула – ресвератол, может быть отвечает за благотворное влияние красного вина в профилактике сердечных заболеваний:
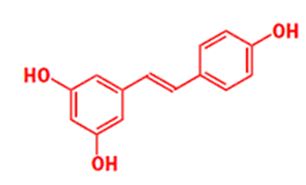
Ресвератол из шкурки виноградинок
В качестве третьего примера «съедобных» молекул (после КЛК и ресвератрола) возьмем витамин С. Моряки дальнего плавания времен эпохи Великих Географических Открытий страдали заболеванием скорбут (цингой), когда происходят дегенеративные процессы мягких тканей, особенно ротовой полости. Нехватка данного витамина и вызывает цингу. Аскорбиновая кислота (тривиальное название витамина С) является универсальным антиоксидантом, она нейтрализует свободные радикалы, защищая людей от рака. Некоторые считают, что большие дозы витамина С защищают нас от простуды, но это ещё не доказано.
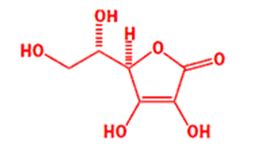
Витамин С
Органическая химия и промышленность
Витами С в больших колличествах получают в Швейцарии, на фармацевтическом заводе Roshe (не путать с РошеноМ). Во всем мире объемы промышленности органического синтеза исчисляются как килограмами (мелкотоннажные производства), так и миллионами тонн (крупнотоннажные производства). Это хорошая новость для студентов-органиков, т.к. дефицита рабочих мест (равно как и переизбытка выпускников) тут нет. Другими словами профессия инженера-химика очень актуальна.
Некоторые простые соединения можно получать как из нефти, так и из растений. Этиловый спирт используют в качестве сырья для получения резины, пластмасс, других органических соединений. Его можно получить каталитической гидратацией этилена (из нефти), либо путем ферментации отходов сахарной промышленности (как в Бразилии, где использование этанола в качестве топлива позволило улучшить экологическую ситуацию).
Стоит отдельно упомянуть полимерную промышленность. Она поглощает наибольшую часть продуктов переработки нефти в виде мономеров (стирол, акрилаты, винилхлорид, этилен). Производство синтетических волокон имеет оборот более чем 25 миллионов тонн в год. В получение поливинилхлорида вовлечено около 50 000 людей с годовым выпуском 20 миллионов тонн.
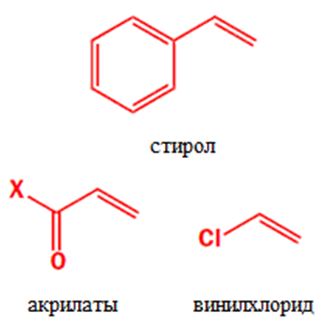
Следует так же упомянуть производство клеев, герметиков, покрытий. Например, известным суперклеем (на основе метил цианоакрилата) Вы можете приклеить почти все.
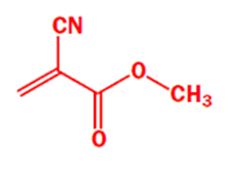
Цианоакрилат – основной компонент суперклея
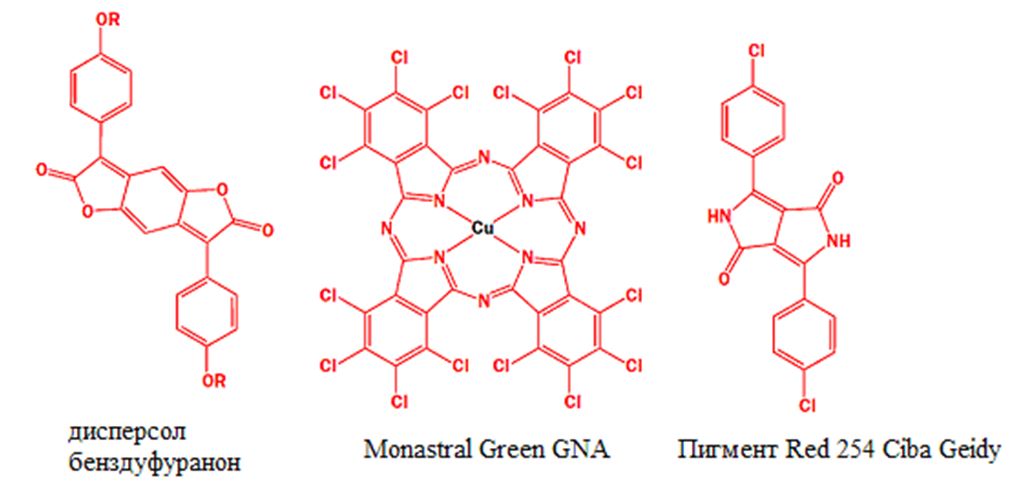
Пожалуй, наиболее известным красителем является индиго, который раньше выделяли из растений, а сейчас получают синтетически. Индиго – это цвет синих джинсов. Для окраски полиэфирных волокон используются, к примеру, бензодифураноны (как дисперсол), которые придают ткани отличный красный цвет. Для окрашивания полимеров используют фталоцианины в виде комплексов с железом, или медью. Они так же находят применение в качестве компонента активного слоя CD, DVD, Blu Ray дисков. Новый класс «высокопроизводительных» красителей на основе DPP (1,4-diketopyrrolo[3,4-c]pyrroles) разработан Ciba-Geidy.
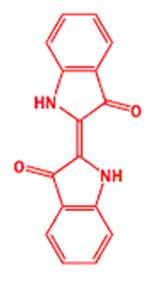
Индиго
Фотография сначала была черно-белой: галоиды серебра взаимодействуя со светом высвобождали атомы металла, которые и воспроизводили изображение. Окрашенные фотографии в цветной пленке марки Кодак возникали как следствие химической реакции между двумя бесцветными реагентами. Один из них, как правило ароматический амин:
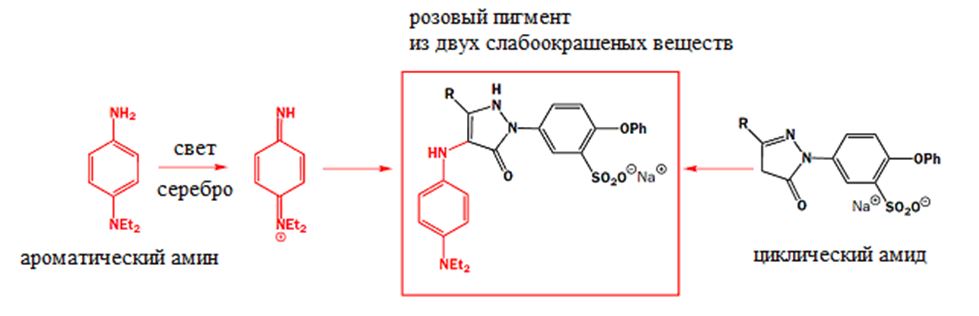
От фотоискусства можно легко перейти в сладкую жизнь.
Подсластители, такие как классический сахар получают в огромных масштабах. Другие подсластители, как аспартам (1965) и сахарин (1879) производятся в аналогичных объемах. Аспартам представляет собой дипептид из двух натуральных аминокислот:
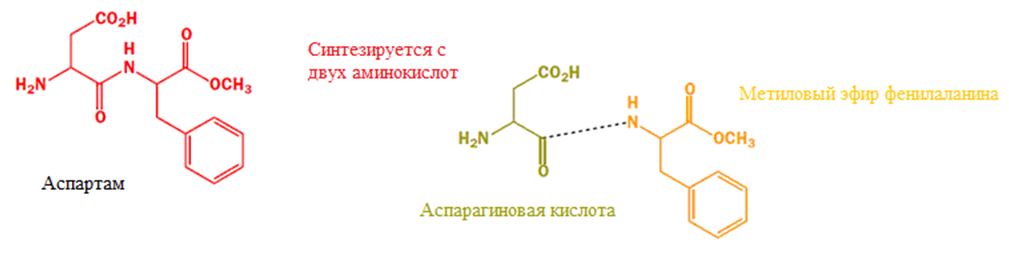
Фармацевтические компании производят лекарственные субстанции от многих болезней. Примером коммерчески успешного, революционного препарата является Ранитидин (от язвенной болезни) и Силденафил (Виагра, надеемся Вы в курсе кому и зачем она нужна).
Успех этих препаратов связан как с лечебной эффективностью, так и прибыльностью:
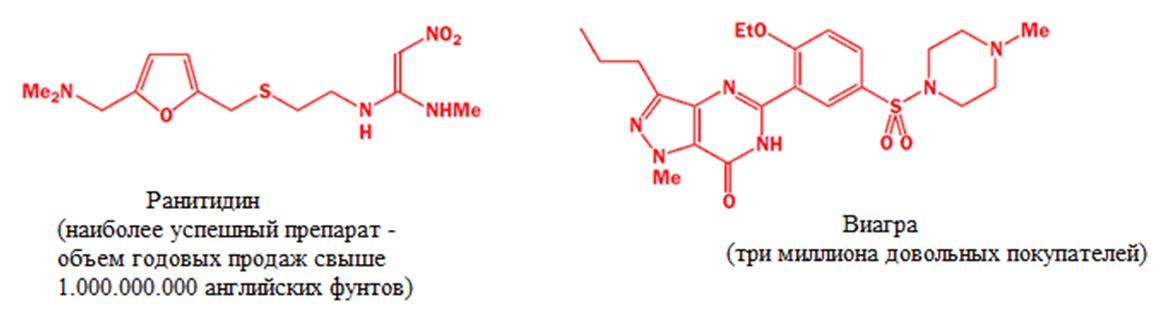
Это еще не всё. Это только начало
Ещё осталось много интересного об органической химии, поэтому обучение на кафедре ОСиНТ является приоритетным не только для любителей химии, но и для абитуриентов, которым интересен окружающий мир, которые желают расширить рамки своего восприятия и раскрыть свой потенциал.
Всё о поступлении на специальность Химические технологии и инженерия
Поступление
на 1 курс
Все самое важное для абитуриента
смотрите здесь
Подробнее
Продолжение обучения
Поступление на 2-4 курс, в магистратуру и аспирантуру. Все формы обучения!
Подробнее
Наши
галереи
Лучше 1 раз увидеть
Чем 100 раз услышать!
Смотрите наши фотографии
Подробнее
Вот несколько последних статей:

Говорили о том какой бывает этиловый спирт из чего его делают, как фальсифицируют и проводят анализы, и чего стоит остерегаться.…

Глицерин применение – пищевые продукты, косметика и взрывчатые вещества Читая этикетки косметических средств, мы зачастую замечаем в их составе глицерин.…

Не так давно Пепси объявила, что они больше не будут использовать подсластитель аспартам, искусственный сахарозаменитель, в диетической Пепси (на территории…

По доброй традиции встреча Нового года у большинства людей не обходится без открытой бутылки шампанского. Напиток в бокале с его…

СОСТАВ КРАСКИ ДЛЯ ВОЛОС КРАСИТЕЛИ И ПИГМЕНТЫ Сегодня, стойкая краска для волос широко используются, либо чтобы прикрыть седые волосы, либо…
Поделиться
web.kpi.kharkov.ua
Химия — Википедия
Хи́мия (от араб. کيمياء, произошедшего, предположительно, от египетского слова km.t (чёрный), откуда возникло также название Египта, чернозёма и свинца — «чёрная земля»[источник не указан 315 дней]; другие возможные варианты: др.-греч. χυμος — «сок», «эссенция», «влага», «вкус», др.-греч. χυμα — «сплав (металлов)», «литьё», «поток», др.-греч. χυμευσις — «смешивание») — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются. Поскольку все вещества состоят из атомов, которые благодаря химическим связям способны формировать молекулы, то химия занимается, прежде всего, рассмотрением перечисленных выше задач на атомно-молекулярном уровне, то есть на уровне химических элементов и их соединений. Химия имеет немало связей с физикой и биологией, по сути граница между ними условна[1], а пограничные области изучаются квантовой химией, химической физикой, физической химией, геохимией, биохимией и другими науками.
Зачатки химии возникли ещё со времён появления человека. Поскольку человек всегда так или иначе имел дело с химическими веществами, его первые эксперименты с огнём, дублением шкур, приготовлением пищи можно назвать зачатками практической химии. Постепенно практические знания накапливались, и в самом начале развития цивилизации люди умели готовить некоторые краски, эмали, яды и лекарства. Вначале человек использовал биологические процессы, такие, как брожение, гниение; позже, с освоением огня, начал использовать процессы горения, спекания, сплавления. Использовались окислительно-восстановительные реакции, не протекающие в живой природе — например, восстановление металлов из их соединений.
Такие ремёсла, как металлургия, гончарство, стеклоделие, крашение, парфюмерия, косметика, достигли значительного развития ещё до начала нашей эры. Например, состав современного бутылочного стекла практически не отличается от состава стекла, применявшегося в 4000 году до н. э. в Египте. Хотя химические знания тщательно скрывались жрецами от непосвящённых, они всё равно медленно проникали в другие страны. К европейцам химическая наука попала главным образом от арабов после завоевания ими Испании в 711 году. Они называли эту науку «алхимией», от них это название распространилось и в Европе.
Известно, что в Египте уже в 3000 году до н. э. умели получать медь из её соединений, используя древесный уголь в качестве восстановителя, а также получали серебро и свинец. Постепенно в Египте и Месопотамии было развито производство бронзы, а в северных странах — железа. Делались также теоретические находки. Например, в Китае с XXII века до н. э. существовала теория об основных элементах (Вода, Огонь, Дерево, Золото, Земля). В Месопотамии возникла идея о противоположностях, из которых построен мир: огонь—вода, тепло—холод, сухость—влажность и т. д.
В V веке до н. э. в Греции Левкипп и Демокрит развили теорию о строении вещества из атомов — атомизм. По аналогии со строением письма они заключили, что как речь делится на слова, а слова состоят из букв, так и все вещества состоят из определённых соединений (молекул), которые в свою очередь состоят из неделимых элементов (атомов).
В V веке до н. э. Эмпедокл предложил считать основными элементами (стихиями) Воду, Огонь, Воздух и Землю. В IV веке до н. э. Платон развил учение Эмпедокла: каждому из этих элементов соответствовал свой цвет и своя правильная пространственная фигура атома, определяющая его свойства: огню — красный цвет и тетраэдр, воде — синий и икосаэдр, земле — зелёный и гексаэдр, воздуху — жёлтый и октаэдр. По мнению Платона, именно из комбинаций этих «кирпичиков» и построен весь материальный мир. Учение о четырёх превращающихся друг в друга было унаследовано Аристотелем.
Алхимия[править | править код]
Слово «алхимия» попало в европейские языки из араб. الخيمياء (’al-kīmiyā’), которое, в свою очередь, было заимствовано из среднегреческого χυμεία «флюид».
Культура Египта обладала хорошо развитыми технологиями, что демонстрируют объекты и сооружения, создание которых возможно только при наличии теоретической и практической базы. Подтверждение развития первичных теоретических знаний в Египте наука получает в последнее время. Тем не менее, на такое происхождение указывает, в большей степени эзотерическую, концептуальную принадлежность имеющие подобия теоретических — традиционные источники алхимии — этого причудливого и цветистого «симбиоза» искусства и, в определённой степени — примата одного из основных разделов естествознания — химии, только формально берущей начало в этом комплексе знаний и опыта. Среди таких источников в первую очередь следует назвать — «Изумрудную скрижаль» (лат. «Tabula smaragdina») Гермеса Трисмегиста, как и ряд других трактатов «Большого алхимического свода».[2][3]
Имел место ещё в IV—III веках до н. э. на Востоке (в Индии, Китае, в арабском мире) ранний «прототип» алхимии. В этот и последующие периоды были найдены новые способы получения таких элементов как ртуть, сера, фосфор, охарактеризованы многие соли, уже были известны и использовались кислота HNO3 и щёлочь NaOH. С раннего Средневековья получает развитие то, что сейчас принято понимать под алхимией, в которой традиционно соединились, наряду с вышеназванными наукообразными компонентами (в смысле современного понимания методологии науки), философские представления эпохи и новые для того времени ремесленные навыки, а также магические и мистические представления; последними, впрочем, и была наделена в отдельных своих проявлениях и особенностях философская мысль той поры. Известными алхимиками того времени были Джабир ибн Хайян (Гебер), Ибн Сина (Авиценна) и Абу Бакр ар-Рази. Ещё в античности, благодаря интенсивному развитию торговли, золото и серебро становятся всеобщим эквивалентом производимых товаров. Трудности, с которыми связано получение этих сравнительно редких металлов, побудили к попыткам практического использования натурфилософских воззрений Аристотеля о преобразовании одних веществ в другие; возникновение учения о «трансмутации», вместе с уже названным Гермесом Трисмегистом, традиция алхимической школы связывала и с его именем. Представления эти претерпели мало изменений вплоть до XIV века.[2][3]
Алхимики в поисках философского камняВ VII веке н. э. алхимия проникла в Европу. В то время, как и на протяжении всей истории, у представителей господствовавших слоёв общества особой «популярностью» пользовались предметы роскоши, в особенности — золото, поскольку именно оно являлось, как уже отмечено, эквивалентом торговой оценки. Алхимиков, в числе прочих вопросов, продолжали интересовать способы получения золота из других металлов, а также проблемы их обработки. Вместе с тем, к тому времени арабская алхимия стала отдаляться от практики и утратила влияние. Из-за особенностей технологий, обусловленных, в числе прочего — системой герметических взглядов, различием знаковых систем, терминологии и сугубо корпоративного распространения знаний «алхимическое действо» развивалось очень медленно. Наиболее известными европейскими алхимиками считаются Никола Фламель, Альберт Великий, Джон Ди, Роджер Бэкон и Раймонд Луллий. Эпоха алхимиков ознаменовала получение многих первичных веществ, разработку способов их получения, выделения и очистки. Только в XVI веке, с развитием различных производств, в том числе металлургии, а также фармацевтики, обусловленным возрастанием её роли в медицине, начали появляться исследователи, чья деятельность выразилась существенными преобразованиями в этой науке, которые приблизили становление хорошо осмысленных и актуальных практических методов этой дисциплины. Среди них, прежде всего, следует назвать Георгия Агриколу и Теофраста Бомбаста Парацельса.[2][3]
Химия как наука[править | править код]
Химия как самостоятельная дисциплина определилась в XVI—XVII веках, после ряда научных открытий, обосновавших механистическую картину мира, развития промышленности, появления буржуазного общества. Однако из-за того, что химия, в отличие от физики, не могла быть выражена количественно, существовали споры, является ли химия количественной воспроизводимой наукой или это некий иной вид познания. В 1661 году Роберт Бойль создал труд «Химик-скептик», в котором объяснил разность свойств различных веществ тем, что они построены из разных частиц (корпускул), которые и отвечают за свойства вещества. Ван Гельмонт, изучая горение, ввёл понятие газ для вещества, которое образуется при нём, открыл углекислый газ. В 1672 году Бойль открыл, что при обжиге металлов их масса увеличивается, и объяснил это захватом «весомых частиц пламени».
М. В. Ломоносов уже в первой известной своей работе, именно к данной области естествознания отношение имеющей — «Элементы математической химии» (1741), в отличие от большинства химиков своего времени, считавших эту сферу деятельности искусством, классифицирует её как науку, начиная свой труд словами[4]:
 | Химия — наука об изменениях, происходящих в смешанном теле, поскольку оно смешанное. …Не сомневаюсь, что найдутся многие, которым это определение покажется неполным, будут сетовать на отсутствие начал разделения, соединения, очищения и других выражений, которыми наполнены почти все химические книги; но те, кто проницательнее, легко усмотрят, что упомянутые выражения, которыми весьма многие писатели по химии имеют обыкновение обременять без надобности свои исследования, могут быть охвачены одним словом: смешанное тело. В самом деле, обладающий знанием смешанного тела может объяснить все возможные изменения его, и в том числе разделение, соединение и т. д. |  |
Тепло и флогистон. Газы[править | править код]
В начале XVIII века Шталь сформулировал теорию флогистона — вещества, удаляющегося из материалов при их горении.
В 1749 году М. В. Ломоносов написал «Размышления о причине теплоты и холода» (замысел работы относится к 1742—1743 годам — см. его же «Заметки по физике и корпускулярной философии»). Высочайшую оценку этому труду дал Л. Эйлер (письмо 21 ноября 1747 года). В 1848 году профессор Д. М. Перевощиков, обстоятельно излагая важнейшие идеи М. В. Ломоносова, подчёркивает, что его теория теплоты опередила науку на полстолетия («Современник», январь 1848, т. VII, кн. 1, отд. II, с. 41—58) — с мнением этим, до того и в дальнейшем, согласуется мнение многих других исследователей.[4]
В 1754 году Блэк открыл углекислый газ, Пристли в 1774 — кислород, а Кавендиш в 1766 — водород.
В период 1740—1790 годов Лавуазье и Ломоносов[4] химически объяснили процессы горения, окисления и дыхания, доказали, что огонь — не вещество, а следствие процесса. Пруст в 1799—1806 годах сформулировал закон постоянства состава. Гей-Люссак в 1808 открыл закон объёмных отношений (закон Авогадро). Дальтон в труде «Новая система химической философии» (1808—1827) доказал существование атомов, ввёл понятие атомный вес, элемент — как совокупность одинаковых атомов.
Реинкарнация атомарной теории вещества[править | править код]
В 1811 году Авогадро выдвинул гипотезу о том, что молекулы элементарных газов состоят из двух одинаковых атомов; позднее на основе этой гипотезы Канниццаро осуществил реформу атомно-молекулярной теории. Эта теория была утверждена на первом международном съезде химиков в Карлсруэ 3-5 сентября 1860 года.
В 1869 году Д. И. Менделеев открыл периодический закон химических элементов и создал периодическую систему химических элементов. Он объяснил понятие химический элемент и показал зависимость свойств элемента от атомной массы. Открытием этого закона он основал химию как количественную науку, а не только как описательную и качественную.
Радиоактивность и спектры[править | править код]
Важную роль в познании структуры вещества сыграли открытия XIX века. Исследование тонкой структуры эмиссионных спектров и спектров поглощения натолкнуло учёных на мысль о их связи со строением атомов веществ. Открытие радиоактивности показало, что некоторые атомы нестабильны (изотопы) и могут самопроизвольно превращаться в новые атомы (радон — «эманация»).
Квантовая химия[править | править код]
- Основная статья: Квантовая химия
Квантовая химия — это направление химии, рассматривающее строение и свойства химических соединений, реакционную способность, кинетику и механизм химических реакций на основе квантовой механики. Разделами квантовой химии являются: квантовая теория строения молекул, квантовая теория химических связей и межмолекулярных взаимодействий, квантовая теория химических реакций и реакционной способности и др.[5] Квантовая химия находится на стыке химии и квантовой физики (квантовой механики). Она занимается рассмотрением химических и физических свойств веществ на атомарном уровне (моделях электронно-ядерного строения и взаимодействий, представленных с точки зрения квантовой механики). Вследствие того, что сложность изучаемых объектов во многих случаях не позволяет находить явные решения уравнений, описывающих процессы в химических системах, применяют приближённые методы расчёта. С квантовой химией неразрывно связана вычислительная химия — дисциплина, использующая математические методы квантовой химии, адаптированные для составления специальных компьютерных программ, используемых для расчёта молекулярных свойств, амплитуды вероятности нахождения электронов в атомах, симуляции молекулярного поведения.
Элементарная частица[править | править код]
- Основная статья: Элементарная частица
Это все частицы, не являющиеся атомными ядрами или атомами (протон — исключение). В узком смысле — частицы, которые нельзя считать состоящими из других частиц (при заданной энергии воздействия/наблюдения). Элементарными частицами также являются электроны (-) и протоны (+).
Атом[править | править код]
- Основная статья: Атом
Наименьшая частица химического элемента, обладающая всеми его свойствами. Атом состоит из ядра и «облака» электронов вокруг него. Ядро состоит из положительно заряженных протонов и нейтральных нейтронов. Взаимодействуя, атомы могут образовывать молекулы.
Атом — предел химического разложения любого вещества. Простое вещество (если оно не является одноатомным, как, например, гелий He) разлагается на атомы одного вида, сложное вещество — на атомы разных видов.
Атомы (точнее, атомные ядра) неделимы химическим путём.
Молекула[править | править код]
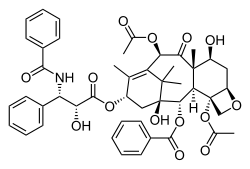 Молекулярная структура изображает связи и относительное положение атомов в молекуле. На иллюстрации показана молекула паклитаксела (номенклатурное название: (2α,4α,5β,7β,10β,13α)-4,10-бис(ацетилокси)-13-{[(2R,3S)- 3-(бензоиламино)-2-гидрокси-3-фенилпропаноил]окси}- 1,7-дигидрокси-9-оксо-5,20-эпокситакс-11-ен-2-ил бензоат)
Молекулярная структура изображает связи и относительное положение атомов в молекуле. На иллюстрации показана молекула паклитаксела (номенклатурное название: (2α,4α,5β,7β,10β,13α)-4,10-бис(ацетилокси)-13-{[(2R,3S)- 3-(бензоиламино)-2-гидрокси-3-фенилпропаноил]окси}- 1,7-дигидрокси-9-оксо-5,20-эпокситакс-11-ен-2-ил бензоат)Частица, состоящая из двух или более атомов, которая может самостоятельно существовать. Имеет постоянный качественный и количественный состав. Свойства молекулы зависят от атомов, входящих в её состав, и от характера связей между ними, от молекулярной структуры и от пространственного расположения (изомеры). Может иметь несколько разных состояний и переходить от одного состояния к другому под действием внешних факторов. Свойства вещества, состоящего из определённых молекул, зависят от состояния молекул и от свойств молекулы.
Вещество[править | править код]
- Основная статья: Вещество
В соответствии с классическими научными воззрениями различаются две физические формы существования материи — вещество и поле. Вещество — это форма материи, обладающая массой (масса не равна нулю). Химия изучает большей частью вещества, организованные в атомы, молекулы, ионы и радикалы. Те, в свою очередь, состоят из элементарных частиц: электронов, протонов, нейтронов и т. д.
Простые и сложные вещества. Химические элементы[править | править код]
Среди чистых веществ принято различать простые (состоящие из атомов одного химического элемента) и сложные (образованы из атомов нескольких химических элементов) вещества.
Простые вещества следует отличать от понятий «атом» и «химический элемент».
Химический элемент — это вид атомов с определённым положительным зарядом ядра. Все химические элементы указаны в Периодической системе элементов Д. И. Менделеева; каждому элементу отвечает свой порядковый (атомный) номер в Периодической системе. Значение порядкового номера элемента и значение заряда ядра атома того же элемента совпадают, то есть химический элемент — это совокупность атомов с одинаковым порядковым номером.
- Основная статья: Химический элемент
Простые вещества представляют собой формы существования химических элементов в свободном виде; каждому элементу соответствует, как правило, несколько простых веществ (аллотропных форм), которые могут различаться по составу, например атомный кислород O, кислород O2 и озон O3, или по кристаллической решётке, например алмаз и графит для элемента углерод C. Очевидно, что простые вещества могут быть одно- и многоатомными.
Сложные вещества иначе называются химическими соединениями. Этот термин означает, что вещества могут быть получены с помощью химических реакций соединения из простых веществ (химического синтеза) или разделены на элементы в свободном виде (простые вещества) с помощью химических реакций разложения (химического анализа).
Простые вещества представляют собой конечные формы химического разложения сложных веществ. Сложные вещества, образующиеся из простых веществ, не сохраняют химические свойства составляющих веществ.
Суммируя всё сказанное выше, можно записать:
E⇄ASC{\displaystyle E{\overset {S}{\underset {A}{\rightleftarrows }}}C}, где
E — простые вещества (элементы в свободном виде),
C — сложные вещества (химические соединения),
S — синтез,
A — анализ.
В настоящее время понятия «синтез» и «анализ» химических веществ используются в более широком смысле. К синтезу относят любой химический процесс, который приводит к получению необходимого вещества и при этом существует возможность его выделения из реакционной смеси. Анализом считается любой химический процесс, позволяющий определить качественный и количественный состав вещества или смеси веществ, то есть установить, из каких элементов составлено данное вещество и каково содержание каждого элемента в этом веществе. Соответственно различают качественный и количественный анализ — две составные части одной из химических наук — аналитической химии.
Металлы и неметаллы[править | править код]
Все химические элементы по их свойствам, то есть свойствам свободных атомов и свойствам образуемых элементами простых и сложных веществ, делят на металлические и неметаллические элементы. Условно к неметаллам относят элементы He, Ne, Ar, Kr, Xe, Rn, F, Cl, Br, I, At, O, S, Se, N, P, C и H. К полуметаллам относят B, Si, Ge, As, Sb, Te, иногда — Po. Остальные элементы считаются металлами.
Чистые вещества и смеси веществ[править | править код]
Индивидуальное чистое вещество обладает определённым набором характеристических свойств. От чистых веществ следует отличать смеси веществ, которые могут состоять из двух или большего числа чистых веществ, сохраняющих присущие им свойства.
Смеси веществ делятся на гомогенные (однородные) и гетерогенные (неоднородные).
| Агрегатное состояние составных частей (до образования смеси) | Гомогенная смесь (гомогенная система) | Гетерогенная смесь (гетерогенная система) |
|---|---|---|
| Твёрдое — твёрдое | Твёрдые растворы, сплавы (например латунь, бронза) | Горные породы (например гранит, минералосодержащие руды и др.) |
| Твёрдое — жидкое | Жидкие растворы (например, водные растворы солей) | Твёрдое в жидком — суспензии или взвеси (например, частицы глины в воде, коллоидные растворы) |
| Жидкое в твёрдом — жидкость в пористых телах (например, почвы, грунты) | ||
| Твёрдое — газообразное | Хемосорбированный водород в платине, палладии, сталях | Твёрдое в газообразном — порошки, аэрозоли, в том числе дым, пыль, смог |
| Газообразное в твёрдом — пористые материалы (например, кирпич, пемза) | ||
| Жидкое — твёрдое | Твёрдые жидкости (например, стекло — твёрдое, но всё же жидкость) | Может принимать разную форму и фиксировать её (например, посуда — разной формы и цвета) |
| Жидкое — жидкое | Жидкие растворы (например, уксус — раствор уксусной кислоты в воде) | Двух- и многослойные жидкие системы, эмульсии (например, молоко — капли жидкого жира в воде) |
| Жидкое — газообразное | Жидкие растворы (например, раствор диоксида углерода в воде) | Жидкое в газообразном — аэрозоли жидкости в газе, в том числе туманы |
| Газообразное в жидком — пены (например, мыльная пена) | ||
| Газообразное — газообразное | Газовые растворы (смеси любых количеств и любого числа газов), напр. воздух. | Гетерогенная система невозможна |
В гомогенных смесях составные части нельзя обнаружить ни визуально, ни с помощью оптических приборов, поскольку вещества находятся в раздробленном состоянии на микроуровне. Гомогенными смесями являются смеси любых газов и истинные растворы, а также смеси некоторых жидкостей и твёрдых веществ, например сплавы.
В гетерогенных смесях либо визуально, либо с помощью оптических приборов можно различить области (агрегаты) разных веществ, разграниченные поверхностью раздела; каждая из этих областей внутри себя гомогенна. Такие области называются фазой.
Гомогенная смесь состоит из одной фазы, гетерогенная смесь состоит из двух или большего числа фаз.
Гетерогенные смеси, в которых одна фаза в виде отдельных частиц распределена в другой, называются дисперсными системами. В таких системах различают дисперсионную среду (распределяющую среду) и дисперсную фазу (раздробленное в дисперсионной среде вещество).
С помощью физических методов разделения можно провести разделение смесей на их составные части, то есть на чистые вещества.
| Агрегатное состояние составных частей смеси | Физическое свойство, используемое для разделения | Метод разделения |
|---|---|---|
| Твёрдое — твёрдое | Плотность | Отстаивание, седиментация |
| Смачиваемость | Флотация, пенная флотация | |
| Размер частиц | Просеивание | |
| Растворимость | Экстракция, выщелачивание | |
| Магнетизм | Магнитная сепарация | |
| Твёрдое — жидкое | Плотность | Седиментация, декантация (сливание жидкости с осадка), центрифугирование |
| Температура кипения жидкости | Выпаривание, дистилляция, осушка | |
| Размер частиц | Фильтрование | |
| Растворимость твёрдого вещества | Кристаллизация | |
| Твёрдое — газообразное | Плотность | Седиментация, центробежная сепарация |
| Размер частиц | Фильтрование | |
| Электрический заряд | Электрофильтрование | |
| Жидкое — жидкое | Плотность | Отстаивание (в делительной воронке, в маслоотделителе), центрифугирование |
| Температура кипения | Дистилляция | |
| Растворимость | Экстракция | |
| Жидкое — газообразное | Плотность | Седиментация, центробежная сепарация |
| Растворимость газа | Отгонка газа (путём повышения температуры), промывание с помощью другой жидкости | |
| Газообразное — газообразное | Температура конденсации | Конденсация |
| Абсорбируемость | Абсорбция (поглощение объёмом сорбента) | |
| Адсорбируемость | Адсорбция (поглощение поверхностью сорбента) | |
| Размер частиц | Диффузия | |
| Масса | Центрифугирование |
Чистыми веществами называются вещества, которые при проведении физических методов не разделяются на два или более других веществ и не изменяют своих физических свойств.
В природе не существует абсолютно чистых веществ. Например, так называемый особо чистый алюминий ещё содержит 0,001 % примесей других веществ. Таким образом, абсолютно чистое вещество — это абстракция. Правда, когда речь идёт о каком-либо веществе, то химия пользуется этой абстракцией, то есть считает, что вещество истинно чистое, хотя практически берётся вещество с некоторым содержанием примесей. Конечно, химик должен стремиться использовать в своей практике по возможности чистые вещества, содержащие минимальное количество примесей. Следует учитывать, что даже незначительное содержание примесей может существенно изменить химические свойства вещества.
| Смесь | Сложное вещество |
|---|---|
| Образуется с помощью физического процесса (смешивание чистых веществ) | Образуется с помощью химической реакции (синтез из простых веществ) |
| Свойства чистых веществ, из которых составлена смесь, остаются неизменными | Свойства простых веществ, из которых получено сложное вещество, в последнем не сохраняются |
| Чистые вещества (простые и сложные) могут находиться в смеси в любом массовом соотношении | Элементы, входящие в состав сложного вещества, всегда находятся в определённом массовом отношении |
| Может быть разделена на составные части (чистые вещества) с помощью физических методов | Может быть разложено на составные части (элементы в виде простых веществ) только с помощью химической реакции (анализ) |
Ион[править | править код]
Основная статья: ИонЭто заряженная частица, атом или молекула, которая имеет неодинаковое количество протонов и электронов. Если у частицы больше электронов, чем протонов, то она заряжена отрицательно и называется анион. Например — Cl−. Если в частице электронов меньше, чем протонов, значит, она заряжена положительно и называется катион. Например — Na+.
Радикал[править | править код]
Это частица (атом или молекула), содержащая один или несколько неспаренных электронов. В большинстве случаев химическая связь образуется при участии двух электронов. Частица, имеющая неспаренный электрон, очень активна и легко образует связи с другими частицами. Поэтому время жизни радикала в среде, как правило, очень мало.
Химическая связь[править | править код]
Удерживает атомы или группы атомов друг около друга. Различают несколько видов химической связи: ионную, ковалентную (полярную и неполярную), металлическую, водородную.
Периодический закон[править | править код]
Открыт Д. И. Менделеевым 1 марта 1869 года. Современная формулировка: Свойства элементов, а также образуемых ими соединений находятся в периодической зависимости от зарядов ядер их атомов.
Химические реакции[править | править код]
Процессы, протекающие в химическом веществе, или в смесях различных веществ, представляют собой химические реакции. При протекании химических реакций всегда образуются новые вещества.
В сущности это процесс изменения структуры молекулы. В результате реакции количество атомов в молекуле может увеличиваться (синтез), уменьшаться (разложение) или оставаться постоянным (изомеризация, перегруппировка). В ходе реакции изменяются связи между атомами и порядок размещения атомов в молекулах.
Химические реакции выявляют и характеризуют химические свойства данного вещества.
Исходные вещества, взятые для проведения химической реакции, называются реагентами, а новые вещества, образующиеся в результате химической реакции, — продуктами реакции. В общем виде химическая реакция изображается так:
Реагенты → Продукты
Химия изучает и описывает эти процессы как в макромасштабе, на уровне макроколичеств веществ, так и в микромасштабе, на атомно-молекулярном уровне. Внешние проявления химических процессов, протекающих в макромасштабе, нельзя непосредственно перенести на микроуровень взаимодействия веществ и однозначно их интерпретировать, однако такие переходы возможны при правильном использовании специальных химических законов, присущих только микрообласти (атомам, молекулам, ионам, взятым в единичных количествах).
Номенклатура[править | править код]
Это свод правил наименования химических соединений. Поскольку общее число известных соединений больше 20 млн, и их число принципиально неограниченно, необходимо пользоваться чёткими правилами при их наименовании, чтобы по названию можно было воспроизвести их структуру. Существует несколько вариантов наименования органических и неорганических соединений, но стандартом считается номенклатура IUPAC.
Современная химия — настолько обширная область естествознания, что многие её разделы по существу представляют собой самостоятельные, хотя и тесно взаимосвязанные научные дисциплины.
По признаку изучаемых объектов (веществ) химию принято делить на неорганическую и органическую. Объяснением сущности химических явлений и установлением их общих закономерностей на основе физических принципов и экспериментальных данных занимается физическая химия, включающая квантовую химию, электрохимию, химическую термодинамику, химическую кинетику. Самостоятельными разделами являются также аналитическая и коллоидная химия (см. ниже перечень разделов).
Технологические основы современных производств излагает химическая технология — наука об экономичных методах и средствах промышленной химической переработки готовых природных материалов и искусственного получения химических продуктов, не встречающихся в окружающей природе.
Сочетание химии с другими смежными естественными науками представляют собой биохимия, биоорганическая химия, геохимия, радиационная химия, фотохимия и др.
Общенаучные основы химических методов разрабатываются в теории познания и методологии науки.
- Агрохимия
- Аналитическая химия занимается изучением веществ с целью получить представление об их химическом составе и структуре, в рамках этой дисциплины ведётся разработка экспериментальных методов химического анализа.
- Биоорганическая химия
- Биохимия изучает химические вещества, их превращения и явления, сопровождающие эти превращения в живых организмах. Тесно связана с органической химией, химией лекарственных средств, нейрохимией, молекулярной биологией и генетикой.
- Вычислительная химия
- Геохимия — наука о химическом составе Земли и планет (космохимия), законах распределения элементов и изотопов, процессах формирования горных пород, почв и природных вод.
- Квантовая химия
- Коллоидная химия
- Компьютерная химия
- Косметическая химия
- Космохимия
- Математическая химия
- Материаловедение
- Медицинская химия
- Металлоорганическая химия
- Нанохимия
- Неорганическая химия изучает свойства и реакции неорганических соединений. Чёткой границы между органической и неорганической химии нет, напротив, существуют дисциплины на стыке этих наук, например, металлоорганическая химия.
- Органическая химия выделяет в качестве предмета изучения вещества, построенные на основе углеродного скелета.
- Нейрохимия своим предметом имеет изучение медиаторов, пептидов, белков, жиров, сахара и нуклеиновых кислот, их взаимодействия и роли, которую они играют в формировании, становлении и изменении нервной системы.
- Нефтехимия
- Общая химия
- Препаративная химия
- Радиохимия
- Супрамолекулярная химия
- Фармацевтика
- Физическая химия изучает физический и фундаментальный базис химических систем и процессов. Важнейшие области исследования включают химическую термодинамику, кинетику, электрохимию, статистическую механику и спектроскопию. Физическая химия имеет много общего с молекулярной физикой. Физическая химия предполагает использование инфинитезимального метода. Физическая химия является отдельной дисциплиной от химической физики.
- Фотохимия
- Химия высокомолекулярных соединений
- Химия одноуглеродных молекул
- Химия полимеров
- Химия почв
- Теоретическая химия своей задачей ставит теоретическое обобщение и обоснование знаний химии через фундаментальные теоретические рассуждения (как правило, в области математики или физики).
- Термохимия
- Токсикологическая химия
- Электрохимия
- Экологическая химия; химия окружающей среды
- Ядерная химия изучает ядерные реакции и химические последствия ядерных реакций.
ru.wikipedia.org
Очень странные вещества, открытые наукой
Еще до зарождения философии в Древней Греции люди были одержимы идеей субстанций, где заканчивается одна материя, и начинается другая, и общими строительными блоками жизни. Но за тысячи лет, в течение которых мы изучали различные материалы, мы получили представление о том, что к чему. С помощью химии и периодической таблицы мы пришли к пониманию и научились предсказывать поведение основных веществ или материалов.У некоторых материалов есть странные абстрактные черты. Нам кажется, что все в природе действует по строгим правилам, кажется предсказуемым и чудесно вписывается в аккуратные небольшие пояснительные инструкции. Это дает нам возможность классифицировать вещи различным способом и понимать их такими, какие они есть. Вот 10 абсолютно странных материалов, которые были открыты учеными за многие годы.
10. Трииодид
Фото: quirkyscience.com
В то время как трииодид является химическим веществом, которое можно смешивать с другими для создания различных химических веществ, сам по себе трииодид, по сути, не очень интересен. Обычно это желтоватое вещество, которое становится красным при получении трииодида азота, который обозначается как NI. Что такого особенного в трииодиде азота? Это его крайняя взрывоопасность.
Большинство взрывчатых веществ становятся таковыми под воздействием химических процессов, таких как взаимодействие с теплом и горение. Но только не трииодид азота, который взрывается при контакте с ним. Именно так. Возьмите грамм этого порошка, поставьте его на стол, прикоснитесь к нему чем угодно и наблюдайте шоу. Все, что требуется для взрыва — простой контакт или трение. Этот материал настолько неустойчив, что к взрыву может привести даже легкое прикосновение к нему.
9. Вантаблэк

Фото: Live Science
Вантаблэк (Vantablack) – это искусственный материал, разработанный компанией Surrey NanoSystems. Этот материал является эквивалентом черной дыры в том, что он поглощает свет настолько, что трехмерные объекты, покрытые материалом, кажутся двумерными, поскольку сильно снижается преломление любого света. Вантаблэк удерживает мировой рекорд как самое темное искусственное вещество и самый темный черный, который вы можете купить. Материал поглощает 99 процентов всего света, с которым вступает в контакт.
В Южной Корее им даже покрыли здание, чтобы создать «самое темное место на Земле», имитируя самые глубокие тайники космоса. Цель состояла в том, чтобы создать опыт погружения в темноту — глубокое темное облако черного. Трехмерные объекты, покрытые вантаблэк, выглядят как тени, которые отбрасывает объект, развернутый в профиль. Это, мягко говоря, очень интересный материал.
8. Супергидрофобный материал

Фото: ultrahydrophobiccoating.com
Супергидрофобный материал – это не то, что мы покупаем, чтобы покрыть кожу или замшу, или нанести на деревянные поверхности, находящиеся снаружи, чтобы защитить их от дождя и другого воздействия. Супергидрофобный материал заставляет воду сворачиваться в сферы, которые выглядят как драгоценные камни.
Он настолько водооталкивающий, что, если вы распылите его на лобовое стекло вашего автомобиля, то сможете ездить под дождем со скоростью до 64 километров в час, и ваше лобовое стекло останется сухим. Прощайте, дворники.
На самом деле, супергидрофобный материал отталкивает почти все жидкости, заставляя их сворачиваться в маленькие шарики, которые вы даже можете катать, как если бы они были настоящими шариками. Этот материал гениален и имеет множество вариантов применения, в том числе и для высокотехнологичных отраслей промышленности. Он очень странный.
7. Ферромагнитная жидкость
Ферромагнитные жидкости представляют собой тип жидкости, которые можно преобразовывать в странные формы, даже не касаясь. Обычно это темная, черная, красноватая, или серая жидкость, которая ведет себя так же, как и обычные жидкости, если нет магнитного поля.
Как только жидкость вступает в контакт с магнитным полем, она становится высоко намагниченной, и начинает принимать разные формы, изгибаясь и вытягиваясь. Она ведет себя как наши обычные твердые магниты, только находится при этом в жидком состоянии.
Эта штука похожа на темный жидкий металл. Ее можно приобрести в интернете или даже сделать с помощью доступной в интернете инструкции. Как и многие другие чудеса физики, ферромагнитная жидкость в действии – удивительное зрелище. Она реагирует на магнитное поле и ведет себя в соответствии с ним. Когда магнитное поле исчезает, жидкость растекается случайным образом.
6. Сверхкритическая жидкость

Фото: Ben Finney, Mark Jacobs
Сверхкритическая жидкость — это материал, созданный при определенных значениях температуры и давления. Она отменяет границы физических свойств, которые мы знаем. Короче говоря, сверхкритическая жидкость — это нечто между жидкостью и газом. Это смесь того и другого, но при этом она не является ни жидкостью, ни газом.
Такое случается, когда жидкость нагревается выше критической температуры и давления. Критическая температура — это точка, в которой вещество было нагрето до такой степени, что вы не можете превратить его в жидкость. Критическое давление — это давление, необходимое для превращения газа в жидкость при высокой температуре.
Сверхкритическая жидкость — газообразное вещество с высокими свойствами жидкости. Если бы вы углубились в атмосферу некоторых планет, таких как Юпитер или Нептун, вы бы погрузились в нее. Это супер-странная версия всех жидкостей… или это газ?
5. Нитинол
Нитинол — это торговое название сплава титана и никеля с чрезвычайно необычными (и важными) свойствами. Нитинол часто используется в медицинской промышленности, но имеет и другие применения. Самое странное в этом металле то, что он похож на жидкий металл, который вы видели в «Терминаторе-2: Судный день», в том, что всегда может вернуться к своей первоначальной форме. Нитинол суперэластичный, или у него есть «память» о своей первоначальной форме.
Поэтому, если вы сделаете объект из нитинола, а затем согнете его, он на ваших глазах автоматически сформирует свою первоначальную форму. Эти свойства памяти формы позволяют использовать его и для развлечения, и для практических целей. Его широко применяют для стентов, поскольку нитинол может сжиматься внутри человеческого тела, если необходимо, обладает прочностью металла, и может возвратиться в свою первоначальную форму каждый раз, когда влияние силы, изменяющей его форму, заканчивается. Свойство нитинола по изменению формы активируется теплом. При некоторых температурах он будет изменять свою первоначальную форму. В других случаях он вернется в исходное состояние.
Эту температурную разницу нужно контролировать в пределах 1 градуса Цельсия. От водорослей, которые помнят освещавший их свет, до нитинола, который всегда помнит свою первоначальную форму и возвращается к ней при правильных условиях, материалы с «памятью», безусловно, удивительные и странные.
4. Галлий

Фото: Live Science
Галлий – это химический элемент, металл, с атомным номером 31, который еще больше напоминает жидкий металл из «Терминатора 2: Судный день». Особенно странной характеристикой галлия является низкая температура, при которой он превращается в жидкость. Она чуть ниже 30 градусов по Цельсию. Во многих местах это близко к комнатной температуре.
Это блестящий металл серебристо-белого цвета. Когда вы имеете дело с галлием, вы имеете дело с жидким металлом. Как с жидкостью, с этим металлом можно играть – он сворачивается и формирует в ваших руках разные формы.
У галлия много сфер практического применения, таких как LED – лампы, производство кабеля и фармацевтика. Это очень мягкий металл, даже в твердом состоянии. На самом деле, он настолько мягкий, что вы можете нарезать его ножом без особых усилий. Если вы сделаете из галлия твердый шар, а затем возьмете его в руки, он растает. Это удивительный металл.
3. Гидрогель

Гидрогели — это увлекательная группа веществ, не хуже сверхкритических жидкостей. Однако вместо того, чтобы находиться где-то между жидкостью и газом, гидрогели находятся где-то между жидкостью и твердым телом. Гидрогель сохраняет свою форму и не растекается, как твердое тело, но он изгибается, как жидкость, и очень податлив. Одним из известных гидрогелей является JELL-O. Это забавный перекус для людей по всему миру. Но есть и другие виды гидрогелей, и другие способы их применения, кроме как в продуктах питания.
Благодаря их гибкости и долговечности, у гидрогелей открываются большие перспективы в мире науки в качестве биоматериалов, которые можно помещать на, или в организм человека. Их способность полностью разжижаться, заполнять пространство, а затем затвердевать и все еще быть гибкими, просто удивительна.
Гидрогели представляют собой серию полимеров, у которых есть определенные химические и физические свойства, и которые плавно изменяют свое состояние с твердого на жидкое. При нагревании белки полимера рассеиваются и перемещаются более свободно. При охлаждении те же самые белки снова затвердевают, но не так сильно, как когда вода превращается в лед. Эти белки делают гидрогель одним из самых необычных чувствительных и внешне интересных веществ.
2. Графеновый аэрогель

Фото: graphene-info.com
Графеновый аэрогель — самый легкий материал на Земле и, безусловно, самый легкий твердый материал, который мы знаем. Его вес составляет всего 0,16 миллиграммов на кубический сантиметр, практически легче, чем воздух. Его плотность даже ниже плотности гелия, хотя немного выше плотности водорода, самого легкого из всех газов.
Графеновый аэрогель был создан из гидрогеля, в котором жидкое содержимое заменили воздухом, в результате объем воздуха в веществе составил 99,98 процента. Вот почему он такой легкий – он пустой. В нем не так много твердых атомов, чтобы он много весил. В результате графеновый аэрогель является наименее плотным из всех известных твердых материалов.
Помимо того, что сегодня графеновый аэрогель используется в разных клеящих веществах, покрытиях и наполнителях, его также используют как легкий материал для трехмерной печати, который позволяет добиться точности. Будущее графенового аэрогеля многообещающее, и это вещество станет основным продуктом будущего для печати таких предметов, как легкие кофейные чашки или даже ювелирные изделия.
1. Темная материя

Фото: Live Science
Темная материя — одна из самых неуловимых субстанций во Вселенной, которая нам известна сегодня, и это делает ее, возможно, одной из самых удивительных. Темная материя составляет около 27% от физической Вселенной. Ее нельзя обнаружить по степени ее освещенности, преломлению света, благодаря которому мы видим обычную материю своими глазами и специальными приборами. Темную материю можно обнаружить только по гравитационному притяжению. Мы знаем, что она где-то там, но не видим ее. Таким образом, мы можем предположить ее наличие только по притяжению, которым она удерживает другие видимые нам объекты.
С появлением первой гипотезы о ее существовании в 1970х годах, присутствием темной материи стало возможным объяснить таинственные движения многих объектов, притягиваемых в ее гравитационное поле – например, галактик, которые каким-то волшебным образом уходят от влияния гравитационного поля более крупных галактик. Гравитационное усиления происходит, когда вещество в пространстве искажает пространственную ткань и искривляет свет. Даже если мы не можем видеть темную материю, мы знаем, что она существует. Она искривляет проходящий свет, а не излучает или поглощает его.
Темная материя составляет около 27 процентов наблюдаемой Вселенной, но наблюдаемая материя составляет только 5 процентов нашей Вселенной. Около 68% Вселенной — это «темная энергия», таинственная, неуловимая энергия. Это означает, что, наблюдая за веществом, можно увидеть около 5 процентов нашей Вселенной. Мы можем воспринимать ее только по тому крошечному кусочку, который можем наблюдать. Это делает темную материю одним из самых странных веществ, обнаруженных современной наукой.
bugaga.ru