Карта сайта
- Шрифт
A
A
A
- Цвет
A
A
A
- Университет
- Сведения об образовательной организации
- Университет сегодня
- Структура
- Ученый совет
- Информационно-библиотечный центр
- Факультеты и кафедры
- Пресс-центр
- Персоналии
- Персональные данные
- Антикоррупционная деятельность
- Противодействие терроризму и экстремизму
- Центр проектной деятельности «POLYGON»
- Образование
- Высшее образование
- Образовательные стандарты
- Второе высшее
- Переподготовка и повышение квалификации
- Учебно-методическое управление
- Образовательные центры
- Школа педагогического мастерства
- ИИ-2021
- Наука
- Управление науки и инноваций
- Диссертационные советы
- Отдел аспирантуры и докторантуры
- Инновационная деятельность
- Инжиниринговый Центр «ПКМиТ»
- Центр коллективного пользования (ЦКП) «Физико-химические методы анализа»
- Научные конференции
- Периодические научные издания
- Научные подразделения
- Конкурс научных кадров
- Развитие
- Перспективы и итоги развития университета
- Программа стратегического академического лидерства «Приоритет 2030»
- Программа развития опорного университета
- Программа трансформации ВолгГТУ
- Цифровая кафедра
- Сотрудничество
- Партнеры университета
- Проекты и программы
- Стажировки
- Международные языковые экзамены
- Подготовка иностранных специалистов
- Программа «Глобальное образование»
- Россотрудничество
- VII Международный Фестиваль русской речи иностранных студентов «Берега»
- Справочник
- Контакты
- Справочник телефонов
- Платежные реквизиты
- Бланки, документы, положения
- Государственные закупки
- Карта сайта
- Абитуриенту
- Личный кабинет абитуриента
- Поступление в вуз онлайн
- Приёмная комиссия
- Учись в политехе
- Выбор специальности
- Подготовка к поступлению
- Прием в политех
- Контакты
- Студенту
- Профсоюзная организация
- Студенческая жизнь
- Расписания
- Рейтинг студента
- Стипендия, общежития, материальная помощь
- Бланки
- Платное образование
- Трудоустройство
- Здоровый образа жизни
- Файловое хранилище
- Аспиранту
- Приём в аспирантуру
- Докторантура
- Перечень научных специальностей
- ФГОС
- Прикрепление для подготовки диссертации
- Прикрепление для сдачи кандидатских экзаменов
- Нормативная база
- Полезные ресурсы
- Результаты промежуточной аттестации
- Расписание занятий
- Портфолио аспирантов
- Сотруднику
- Профсоюзная организация
- Показатели работы ППС университета
- Документы
- Документооборот
- Государственные закупки
- Персональные данные
- Выпускнику
- Ассоциация выпускников ВолгГТУ
Главная / education / Карта сайта
|
Амилоидоз — Список литературы | BMJ Best Practice
Основные статьи
Wechalekar AD, Gillmore JD, Hawkins PN. Systemic amyloidosis. Lancet. 2016 Jun 25;387(10038):2641-54. Аннотация
Systemic amyloidosis. Lancet. 2016 Jun 25;387(10038):2641-54. Аннотация
Merlini G, Dispenzieri A, Sanchorawala V, et al. Systemic immunoglobulin light chain amyloidosis. Nat Rev Dis Primers. 2018 Oct 25;4(1):38. Аннотация
Papa R, Lachmann HJ. Secondary, AA, amyloidosis. Rheum Dis Clin North Am. 2018 Nov;44(4):585-603. Аннотация
Siddiqi OK, Ruberg FL. Cardiac amyloidosis: an update on pathophysiology, diagnosis, and treatment. Trends Cardiovasc Med. 2018 Jan;28(1):10-21. Аннотация
Kapoor M, Rossor AM, Jaunmuktane Z, et al. Diagnosis of amyloid neuropathy. Pract Neurol. 2019 Jun;19(3):250-8. Аннотация
Tuzovic M, Yang EH, Baas AS, et al. Cardiac amyloidosis: diagnosis and treatment strategies. Curr Oncol Rep. 2017 Jul;19(7):46. Аннотация
Palladini G, Kastritis E, Maurer MS, et al. Daratumumab plus CyBorD for patients with newly diagnosed AL amyloidosis: safety run-in results of ANDROMEDA. Blood. 2020 Jul 2;136(1):71-80.Полный текст
Аннотация
Daratumumab plus CyBorD for patients with newly diagnosed AL amyloidosis: safety run-in results of ANDROMEDA. Blood. 2020 Jul 2;136(1):71-80.Полный текст
Аннотация
Adams D, Gonzalez-Duarte A, O’Riordan WD, et al. Patisiran, an RNAi therapeutic, for hereditary transthyretin amyloidosis. N Engl J Med. 2018 Jul 5;379(1):11-21. Аннотация
Benson MD, Waddington-Cruz M, Berk JL, et al. Inotersen treatment for patients with hereditary transthyretin amyloidosis. N Engl J Med. 2018 Jul 5;379(1):22-31. Аннотация
Maurer MS, Schwartz JH, Gundapaneni B, et al. Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med. 2018 Sep 13;379(11):1007-16. Аннотация
Статьи, указанные как источники
1. Gertz MA, Comenzo R, Falk RH, et al. Definition of organ involvement and treatment response in immunoglobulin light chain amyloidosis (AL): a consensus opinion from the 10th International Symposium on Amyloid and Amyloidosis, Tours, France, 18-22 April 2004. Am J Hematol. 2005 Aug;79(4):319-28. Аннотация
Definition of organ involvement and treatment response in immunoglobulin light chain amyloidosis (AL): a consensus opinion from the 10th International Symposium on Amyloid and Amyloidosis, Tours, France, 18-22 April 2004. Am J Hematol. 2005 Aug;79(4):319-28. Аннотация
2. International Myeloma Working Group. Criteria for the classification of monoclonal gammopathies, multiple myeloma and related disorders: a report of the International Myeloma Working Group. Br J Haematol. 2003 Jun;121(5):749-57. Аннотация
3. Benson MD, Buxbaum JN, Eisenberg DS, et al. Amyloid nomenclature 2020: update and recommendations by the International Society of Amyloidosis (ISA) nomenclature committee. Amyloid. 2020 Dec;27(4):217-22.Полный текст Аннотация
4. Quock TP, Yan T, Chang E, et al. Epidemiology of AL amyloidosis: a real-world study using US claims data. Blood Adv. 2018 May 22;2(10):1046-53.Полный текст
Аннотация
Blood Adv. 2018 May 22;2(10):1046-53.Полный текст
Аннотация
5. Bergesio F, Ciciani AM, Santostefano M, et al. Renal involvement in systemic amyloidosis — an Italian retrospective study on epidemiological and clinical data at diagnosis. Nephrol Dial Transplant. 2007 Jun;22(6):1608-18. Аннотация
6. Staron A, Connors LH, Zheng L, et al. Race/ethnicity in systemic AL amyloidosis: perspectives on disease and outcome disparities. Blood Cancer J. 2020 Nov 10;10(11):118.Полный текст Аннотация
7. National Cancer Institute: Surveillance, Epidemiology, and End Results Program. Cancer stat facts: myeloma. 10 Apr 2018 [internet publication].Полный текст
8. Wadhera RK, Rajkumar SV. Prevalence of monoclonal gammopathy of undetermined significance: a systematic review. Mayo Clin Proc. 2010 Oct;85(10):933-42. Аннотация
Mayo Clin Proc. 2010 Oct;85(10):933-42. Аннотация
9. Landgren O, Weiss BM. Patterns of monoclonal gammopathy of undetermined significance and multiple myeloma in various ethnic/racial groups: support for genetic factors in pathogenesis. Leukemia. 2009 Oct;23(10):1691-7.Полный текст Аннотация
10. Hazenberg BP, van Rijswijk MH. Where has secondary amyloid gone? Ann Rheum Dis. 2000 Aug;59(8):577-9.Полный текст Аннотация
11. Lachmann HJ, Goodman HJB, Gilbertson JA, et al. Natural history and outcome in systemic AA amyloidosis. N Engl J Med. 2007;356:2361-2371.Полный текст Аннотация
12. Lane T, Pinney JH, Gilbertson JA, et al. Changing epidemiology of AA amyloidosis: clinical observations over 25 years at a single national referral centre. Amyloid. 2017 Sep;24(3):162-6. Аннотация
Amyloid. 2017 Sep;24(3):162-6. Аннотация
13. Pinney JH, Smith CJ, Taube JB, et al. Systemic amyloidosis in England: an epidemiological study. Br J Haematol. 2013 May;161(4):525-32. Аннотация
14. Wechalekar AD, Gillmore JD, Hawkins PN. Systemic amyloidosis. Lancet. 2016 Jun 25;387(10038):2641-54. Аннотация
15. Rajkumar SV, Gertz MA, Kyle RA. Primary systemic amyloidosis with delayed progression to multiple myeloma. Cancer. 1998 Apr 15;82(8):1501-5. Аннотация
16. Kourelis TV, Kumar SK, Gertz MA, et al. Coexistent multiple myeloma or increased bone marrow plasma cells define equally high-risk populations in patients with immunoglobulin light chain amyloidosis. J Clin Oncol. 2013 Dec 1;31(34):4319-24.Полный текст Аннотация
17. Larsen CP, Ismail W, Kurtin PJ, et al. Leukocyte chemotactic factor 2 amyloidosis (ALECT2) is a common form of renal amyloidosis among Egyptians. Mod Pathol. 2016 Apr;29(4):416-20.Полный текст
Аннотация
Larsen CP, Ismail W, Kurtin PJ, et al. Leukocyte chemotactic factor 2 amyloidosis (ALECT2) is a common form of renal amyloidosis among Egyptians. Mod Pathol. 2016 Apr;29(4):416-20.Полный текст
Аннотация
18. Comenzo RL, Zhou P, Fleisher M, et al. Seeking confidence in the diagnosis of systemic AL (Ig light-chain) amyloidosis: patients can have both monoclonal gammopathies and hereditary amyloid proteins. Blood. 2006 May 1;107(9):3489-91.Полный текст Аннотация
19. Merlini G, Dispenzieri A, Sanchorawala V, et al. Systemic immunoglobulin light chain amyloidosis. Nat Rev Dis Primers. 2018 Oct 25;4(1):38. Аннотация
20. Pozzi C, Locatelli F. Kidney and liver involvement in monoclonal light chain disorders. Semin Nephrol. 2002 Jul;22(4):319-30. Аннотация
Аннотация
21. Gu M, Wilton R, Stevens FJ. Diversity and diversification of light chains in myeloma: the specter of amyloidogenesis by proxy. Contrib Nephrol. 2007;153:156-81. Аннотация
22. Comenzo RL, Zhang Y, Martinez C, et al. The tropism of organ involvement in primary systemic amyloidosis: contributions of Ig V(L) germ line gene use and clonal plasma cell burden. Blood. 2001 Aug 1;98(3):714-20.Полный текст Аннотация
23. Gertz MA, Leung N, Lacy MQ, et al. Clinical outcome of immunoglobulin light chain amyloidosis affecting the kidney. Nephrol Dial Transplant. 2009 Oct;24(10):3132-7.Полный текст Аннотация
24. Merlini G, Pozzi C. Mechanisms of renal damage in plasma cell dyscrasias: an overview. Contrib Nephrol. 2007;153:66-86. Аннотация
Contrib Nephrol. 2007;153:66-86. Аннотация
25. Gertz MA, Lacy MQ, Dispenzieri A, et al. Amyloidosis: diagnosis and management. Clin Lymphoma Myeloma. 2005 Nov;6(3):208-19. Аннотация
26. Shah KB, Inoue Y, Mehra MR. Amyloidosis and the heart: a comprehensive review. Arch Intern Med. 2006 Sep 25;166(17):1805-13.Полный текст Аннотация
27. Muchtar E, Gertz MA, Lacy MQ, et al. Ten-year survivors in AL amyloidosis: characteristics and treatment pattern. Br J Haematol. 2019 Dec;187(5):588-94.Полный текст Аннотация
28. Martinez-Naharro A, Hawkins PN, Fontana M. Cardiac amyloidosis. Clin Med (Lond). 2018 Apr 1;18(suppl 2):s30-s35.Полный текст Аннотация
29. Falk RH, Alexander KM, Liao R, et al. AL (light-chain) cardiac amyloidosis: a review of diagnosis and therapy. J Am Coll Cardiol. 2016 Sep 20;68(12):1323-41.Полный текст
Аннотация
Falk RH, Alexander KM, Liao R, et al. AL (light-chain) cardiac amyloidosis: a review of diagnosis and therapy. J Am Coll Cardiol. 2016 Sep 20;68(12):1323-41.Полный текст
Аннотация
30. Perugini E, Rapezzi C, Reggiani LB, et al. Comparison of ventricular long-axis function in patients with cardiac amyloidosis versus idiopathic restrictive cardiomyopathy. Am J Cardiol. 2005 Jan 1;95(1):146-9. Аннотация
31. Palladini G, Merlini G. What is new in diagnosis and management of light chain amyloidosis? Blood. 2016 Jul 14;128(2):159-68.Полный текст Аннотация
32. Gertz MA, Lacy MQ, Dispenzieri A, et al. Amyloidosis. Best Pract Res Clin Haematol. 2005;18(4):709-27. Аннотация
33. Freeman R. Autonomic peripheral neuropathy. Lancet. 2005 Apr 2-8;365(9466):1259-70. Аннотация
Autonomic peripheral neuropathy. Lancet. 2005 Apr 2-8;365(9466):1259-70. Аннотация
34. Siddiqi OK, Ruberg FL. Cardiac amyloidosis: an update on pathophysiology, diagnosis, and treatment. Trends Cardiovasc Med. 2018 Jan;28(1):10-21. Аннотация
35. Kittleson MM, Maurer MS, Ambardekar AV, et al. Cardiac amyloidosis: evolving diagnosis and management: a scientific statement from the American Heart Association. Circulation. 2020 Jul 7;142(1):e7-e22.Полный текст Аннотация
36. Grogan M, Scott CG, Kyle RA, et al. Natural history of wild-type transthyretin cardiac amyloidosis and risk stratification using a novel staging system. J Am Coll Cardiol. 2016 Sep 6;68(10):1014-20.Полный текст Аннотация
37. Kyle RA, Therneau TM, Rajkumar SV, et al. A long-term study of prognosis in monoclonal gammopathy of undetermined significance. N Engl J Med. 2002 Feb 21;346(8):564-9.Полный текст
Аннотация
Kyle RA, Therneau TM, Rajkumar SV, et al. A long-term study of prognosis in monoclonal gammopathy of undetermined significance. N Engl J Med. 2002 Feb 21;346(8):564-9.Полный текст
Аннотация
38. Papa R, Lachmann HJ. Secondary, AA, amyloidosis. Rheum Dis Clin North Am. 2018 Nov;44(4):585-603. Аннотация
39. Lachmann HJ, Booth DR, Booth SE, et al. Misdiagnosis of hereditary amyloidosis as AL (primary) amyloidosis. N Engl J Med. 2002 Jun 6;346(23):1786-91.Полный текст Аннотация
40. Muchtar E, Gertz MA, Kumar SK, et al. Improved outcomes for newly diagnosed AL amyloidosis between 2000 and 2014: cracking the glass ceiling of early death. Blood. 2017 Apr 13;129(15):2111-9.Полный текст Аннотация
41. Siddiqi OK, Ruberg FL. Cardiac amyloidosis: an update on pathophysiology, diagnosis, and treatment. Trends Cardiovasc Med. 2018 Jan;28(1):10-21. Аннотация
Siddiqi OK, Ruberg FL. Cardiac amyloidosis: an update on pathophysiology, diagnosis, and treatment. Trends Cardiovasc Med. 2018 Jan;28(1):10-21. Аннотация
42. Neben-Wittich MA, Wittich CM, Mueller PS, et al. Obstructive intramural coronary amyloidosis and myocardial ischemia are common in primary amyloidosis. Am J Med. 2005 Nov;118(11):1287. Аннотация
43. Conceição I, González-Duarte A, Obici L, Schmidt HH, Simoneau D, Ong ML, Amass L. «Red-flag» symptom clusters in transthyretin familial amyloid polyneuropathy. J Peripher Nerv Syst. 2016 Mar;21(1):5-9.Полный текст Аннотация
44. Planté-Bordeneuve V, Said G. Familial amyloid polyneuropathy. Lancet Neurol. 2011 Dec;10(12):1086-97. Аннотация
45. Kaku M, Berk JL. Neuropathy associated with systemic amyloidosis. Semin Neurol. 2019 Oct;39(5):578-88. Аннотация
Semin Neurol. 2019 Oct;39(5):578-88. Аннотация
46. Gonzalez-Duarte A, Valdés-Ferrer SI, Cantú-Brito C. Characteristics and natural history of autonomic involvement in hereditary ATTR amyloidosis: a systematic review. Clin Auton Res. 2019 Sep;29(suppl 1):1-9.Полный текст Аннотация
47. Vaxman I, Gertz M. When to suspect a diagnosis of amyloidosis. Acta Haematol. 2020;143(4):304-11.Полный текст Аннотация
48. Kapoor M, Rossor AM, Jaunmuktane Z, et al. Diagnosis of amyloid neuropathy. Pract Neurol. 2019 Jun;19(3):250-8. Аннотация
49. Kyle RA, Gertz MA. Primary systemic amyloidosis: clinical and laboratory features in 474 cases. Semin Hematol. 1995 Jan;32(1):45-59. Аннотация
50. Katzmann JA, Abraham RS, Dispenzieri A, et al. Diagnostic performance of quantitative kappa and lambda free light chain assays in clinical practice. Clin Chem. 2005 May;51(5):878-81.Полный текст
Аннотация
Katzmann JA, Abraham RS, Dispenzieri A, et al. Diagnostic performance of quantitative kappa and lambda free light chain assays in clinical practice. Clin Chem. 2005 May;51(5):878-81.Полный текст
Аннотация
51. Morris KL, Tate JR, Gill D, et al. Diagnostic and prognostic utility of the serum free light chain assay in patients with AL amyloidosis. Intern Med J. 2007 Jul;37(7):456-63. Аннотация
52. National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: systemic light chain amyloidosis. 2021 [internet publication].Полный текст
53. Gertz MA. The classification and typing of amyloid deposits. Am J Clin Pathol. 2004 Jun;121(6):787-9. Аннотация
54. Gillmore JD, Wechalekar A, Bird J, et al. Guidelines on the diagnosis and investigation of AL amyloidosis. Br J Haematol. 2015 Jan;168(2):207-18.Полный текст
Аннотация
Guidelines on the diagnosis and investigation of AL amyloidosis. Br J Haematol. 2015 Jan;168(2):207-18.Полный текст
Аннотация
55. Hawkins PN, Lavender JP, Pepys MB. Evaluation of systemic amyloidosis by scintigraphy with 123I-labeled serum amyloid P component. N Engl J Med. 1990 Aug 23;323(8):508-13.Полный текст Аннотация
56. Maurer MS, Bokhari S, Damy T, et al. Expert consensus recommendations for the suspicion and diagnosis of transthyretin cardiac amyloidosis. Circ Heart Fail. 2019 Sep;12(9):e006075.Полный текст Аннотация
57. Tuzovic M, Yang EH, Baas AS, et al. Cardiac amyloidosis: diagnosis and treatment strategies. Curr Oncol Rep. 2017 Jul;19(7):46. Аннотация
58. Koyama J, Ray-Sequin PA, Falk RH. Longitudinal myocardial function assessed by tissue velocity, strain, and strain rate tissue Doppler echocardiography in patients with AL (primary) cardiac amyloidosis. Circulation. 2003 May 20;107(19):2446-52.Полный текст
Аннотация
Koyama J, Ray-Sequin PA, Falk RH. Longitudinal myocardial function assessed by tissue velocity, strain, and strain rate tissue Doppler echocardiography in patients with AL (primary) cardiac amyloidosis. Circulation. 2003 May 20;107(19):2446-52.Полный текст
Аннотация
59. Weidemann F, Strotmann JM. Use of tissue Doppler imaging to identify and manage systemic diseases. Clin Res Cardiol. 2008 Feb;97(2):65-73. Аннотация
60. Gertz M, Adams D, Ando Y, et al. Avoiding misdiagnosis: expert consensus recommendations for the suspicion and diagnosis of transthyretin amyloidosis for the general practitioner. BMC Fam Pract. 2020 Sep 23;21(1):198.Полный текст Аннотация
61. Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy diagnosis of cardiac transthyretin amyloidosis. Circulation. 2016 Jun 14;133(24):2404-12.Полный текст
Аннотация
Circulation. 2016 Jun 14;133(24):2404-12.Полный текст
Аннотация
62. Castano A, Haq M, Narotsky DL, et al. Multicenter study of planar technetium 99m pyrophosphate cardiac imaging: predicting survival for patients with ATTR cardiac amyloidosis. JAMA Cardiol. 2016 Nov 1;1(8):880-9.Полный текст Аннотация
63. Dispenzieri A, Kyle RA, Gertz MA, et al. Survival in patients with primary systemic amyloidosis and raised serum cardiac troponins. Lancet. 2003 May 24;361(9371):1787-9. Аннотация
64. Palladini G, Campana C, Klersy C, et al. Serum N-terminal pro-brain natriuretic peptide is a sensitive marker of myocardial dysfunction in AL amyloidosis. Circulation. 2003 May 20;107(19):2440-5.Полный текст Аннотация
65. Zerbini CA, Anderson JJ, Kane KA, et al. Beta 2 microglobulin serum levels and prediction of survival in AL amyloidosis. Amyloid. 2002 Dec;9(4):242-6. Аннотация
Zerbini CA, Anderson JJ, Kane KA, et al. Beta 2 microglobulin serum levels and prediction of survival in AL amyloidosis. Amyloid. 2002 Dec;9(4):242-6. Аннотация
66. Palladini G, Russo P, Bosoni T, et al. Identification of amyloidogenic light chains requires the combination of serum-free light chain assay with immunofixation of serum and urine. Clin Chem. 2009 Mar;55(3):499-504.Полный текст Аннотация
67. Dispenzieri A, Gertz MA, Kyle RA, et al. Serum cardiac troponins and N-terminal pro-brain natriuretic peptide: a staging system for primary systemic amyloidosis. J Clin Oncol. 2004 Sep 15;22(18):3751-7. Аннотация
68. Kumar S, Dispenzieri A, Lacy MQ, et al. Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements. J Clin Oncol. 2012 Mar 20;30(9):989-95. Аннотация
J Clin Oncol. 2012 Mar 20;30(9):989-95. Аннотация
69. Wechalekar AD, Schonland SO, Kastritis E, et al. A European collaborative study of treatment outcomes in 346 patients with cardiac stage III AL amyloidosis. Blood. 2013 Apr 25;121(17):3420-7.Полный текст Аннотация
70. Palladini G, Dispenzieri A, Gertz MA, et al. New criteria for response to treatment in immunoglobulin light chain amyloidosis based on free light chain measurement and cardiac biomarkers: impact on survival outcomes. J Clin Oncol. 2012 Dec 20;30(36):4541-9.Полный текст Аннотация
71. Dispenzieri A, Buadi F, Kumar SK, et al. Treatment of immunoglobulin light chain amyloidosis: Mayo stratification of myeloma and risk-adapted therapy (mSMART) consensus statement. Mayo Clin Proc. 2015 Aug;90(8):1054-81.Полный текст
Аннотация
2015 Aug;90(8):1054-81.Полный текст
Аннотация
72. mSMART. Mayo consensus on AL amyloidosis: diagnosis, treatment and prognosis. October 2020 [internet publication].Полный текст
73. Muchtar E, Gertz MA, Lacy MQ, et al. Refining amyloid complete hematological response: Quantitative serum free light chains superior to ratio. Am J Hematol. 2020 Nov;95(11):1280-7. Аннотация
74. Rajkumar SV, Lacy MQ, Kyle RA. Monoclonal gammopathy of undetermined significance and smoldering multiple myeloma. Blood Rev. 2007 Sep;21(5):255-65. Аннотация
75. Vaxman I, Gertz M. Recent advances in the diagnosis, risk stratification, and management of systemic light-chain amyloidosis. Acta Haematol. 2019;141(2):93-106.Полный текст Аннотация
76. Comenzo RL, Gertz MA. Autologous stem cell transplantation for primary systemic amyloidosis. Blood. 2002 Jun 15;99(12):4276-82.Полный текст
Аннотация
Comenzo RL, Gertz MA. Autologous stem cell transplantation for primary systemic amyloidosis. Blood. 2002 Jun 15;99(12):4276-82.Полный текст
Аннотация
77. Sidiqi MH, Aljama MA, Muchtar E, et al. Autologous stem cell transplant for immunoglobulin light chain aAmyloidosis patients aged 70 to 75. Biol Blood Marrow Transplant. 2018 Oct;24(10):2157-9.Полный текст Аннотация
78. Jaccard A, Moreau P, Leblond V, et al. High-dose melphalan versus melphalan plus dexamethasone for AL amyloidosis. N Engl J Med. 2007 Sep 13;357(11):1083-93. Аннотация
79. Mhaskar R, Kumar A, Behera M, et al. Role of high-dose chemotherapy and autologous hematopoietic cell transplantation in primary systemic amyloidosis: a systematic review. Biol Blood Marrow Transplant. 2009 Aug;15(8):893-902. Аннотация
2009 Aug;15(8):893-902. Аннотация
80. D’Souza A, Dispenzieri A, Wirk B, et al. Improved outcomes after autologous hematopoietic cell transplantation for light chain amyloidosis: a Center for International Blood and Marrow Transplant Research study. J Clin Oncol. 2015 Nov 10;33(32):3741-9.Полный текст Аннотация
81. Sidiqi MH, Aljama MA, Buadi FK, et al. Stem cell transplantation for light chain amyloidosis: decreased early mortality over time. J Clin Oncol. 2018 May 1;36(13):1323-9.Полный текст Аннотация
82. Gertz MA. Immunoglobulin light chain amyloidosis: 2020 update on diagnosis, prognosis, and treatment. Am J Hematol. 2020 Jul;95(7):848-60. Аннотация
83. Scott EC, Heitner SB, Dibb W, et al. Induction bortezomib in Al amyloidosis followed by high dose melphalan and autologous stem cell transplantation: a single institution retrospective study. Clin Lymphoma Myeloma Leuk. 2014 Oct;14(5):424-30.e1. Аннотация
Induction bortezomib in Al amyloidosis followed by high dose melphalan and autologous stem cell transplantation: a single institution retrospective study. Clin Lymphoma Myeloma Leuk. 2014 Oct;14(5):424-30.e1. Аннотация
84. Sanchorawala V, Brauneis D, Shelton AC, et al. Induction therapy with bortezomib followed by bortezomib-high dose melphalan and stem cell transplantation for light chain amyloidosis: results of a prospective clinical trial. Biol Blood Marrow Transplant. 2015 Aug;21(8):1445-51.Полный текст Аннотация
85. Afrough A, Saliba RM, Hamdi A, et al. Impact of induction therapy on the outcome of immunoglobulin light chain amyloidosis after autologous hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2018 Nov;24(11):2197-203.Полный текст Аннотация
86. Cornell RF, Zhong X, Arce-Lara C, et al. Bortezomib-based induction for transplant ineligible AL amyloidosis and feasibility of later transplantation. Bone Marrow Transplant. 2015 Jul;50(7):914-7.Полный текст
Аннотация
Cornell RF, Zhong X, Arce-Lara C, et al. Bortezomib-based induction for transplant ineligible AL amyloidosis and feasibility of later transplantation. Bone Marrow Transplant. 2015 Jul;50(7):914-7.Полный текст
Аннотация
87. Huang X, Wang Q, Chen W, et al. Induction therapy with bortezomib and dexamethasone followed by autologous stem cell transplantation versus autologous stem cell transplantation alone in the treatment of renal AL amyloidosis: a randomized controlled trial. BMC Med. 2014 Jan 6;12:2.Полный текст Аннотация
88. Cohen AD, Zhou P, Chou J, et al. Risk-adapted autologous stem cell transplantation with adjuvant dexamethasone ± thalidomide for systemic light-chain amyloidosis: results of a phase II trial. Br J Haematol. 2007 Oct;139(2):224-33.Полный текст Аннотация
89. Landau H, Hassoun H, Rosenzweig MA, et al. Bortezomib and dexamethasone consolidation following risk-adapted melphalan and stem cell transplantation for patients with newly diagnosed light-chain amyloidosis. Leukemia. 2013 Apr;27(4):823-8.Полный текст
Аннотация
Landau H, Hassoun H, Rosenzweig MA, et al. Bortezomib and dexamethasone consolidation following risk-adapted melphalan and stem cell transplantation for patients with newly diagnosed light-chain amyloidosis. Leukemia. 2013 Apr;27(4):823-8.Полный текст
Аннотация
90. Milani P, Basset M, Nuvolone M, et al. Indicators of profound hematologic response in AL amyloidosis: complete response remains the goal of therapy. Blood Cancer J. 2020 Sep 1;10(8):90.Полный текст Аннотация
91. Tandon N, Sidana S, Dispenzieri A, et al. Impact of involved free light chain (FLC) levels in patients achieving normal FLC ratio after initial therapy in light chain amyloidosis (AL). Am J Hematol. 2018 Jan;93(1):17-22.Полный текст Аннотация
92. Muchtar E, Dispenzieri A, Leung N, et al. Optimizing deep response assessment for AL amyloidosis using involved free light chain level at end of therapy: failure of the serum free light chain ratio. Leukemia. 2019 Feb;33(2):527-31. Аннотация
Muchtar E, Dispenzieri A, Leung N, et al. Optimizing deep response assessment for AL amyloidosis using involved free light chain level at end of therapy: failure of the serum free light chain ratio. Leukemia. 2019 Feb;33(2):527-31. Аннотация
93. Al Saleh AS, Sidiqi MH, Sidana S, et al. Impact of consolidation therapy post autologous stem cell transplant in patients with light chain amyloidosis. Am J Hematol. 2019 Oct;94(10):1066-71.Полный текст Аннотация
94. Sanchorawala V, Wright DG, Rosenzweig M, et al. Lenalidomide and dexamethasone in the treatment of AL amyloidosis: results of a phase 2 trial. Blood. 2007 Jan 15;109(2):492-6.Полный текст Аннотация
95. Specter R, Sanchorawala V, Seldin DC, et al. Kidney dysfunction during lenalidomide treatment for AL amyloidosis. Nephrol Dial Transplant. 2011 Mar;26(3):881-6.Полный текст
Аннотация
Nephrol Dial Transplant. 2011 Mar;26(3):881-6.Полный текст
Аннотация
96. Sitia R, Palladini G, Merlini G. Bortezomib in the treatment of AL amyloidosis: targeted therapy? Haematologica. 2007 Oct;92(10):1302-7.Полный текст Аннотация
97. Kastritis E, Anagnostopoulos A, Roussou M, et al. Treatment of light chain (AL) amyloidosis with the combination of bortezomib and dexamethasone. Haematologica. 2007 Oct;92(10):1351-8. Аннотация
98. Gavriatopoulou M, Musto P, Caers J, et al. European myeloma network recommendations on diagnosis and management of patients with rare plasma cell dyscrasias. Leukemia. 2018 Sep;32(9):1883-98. Аннотация
99. Gertz MA. Immunoglobulin light chain amyloidosis: 2020 update on diagnosis, prognosis, and treatment. Am J Hematol. 2020 Jul;95(7):848-60. Аннотация
Am J Hematol. 2020 Jul;95(7):848-60. Аннотация
100. Kastritis E, Leleu X, Arnulf B, et al. Bortezomib, melphalan, and dexamethasone for light-chain amyloidosis. J Clin Oncol. 2020 Oct 1;38(28):3252-60.Полный текст Аннотация
101. Palladini G, Kastritis E, Maurer MS, et al. Daratumumab plus CyBorD for patients with newly diagnosed AL amyloidosis: safety run-in results of ANDROMEDA. Blood. 2020 Jul 2;136(1):71-80.Полный текст Аннотация
102. Palladini G, Russo P, Nuvolone M, et al. Treatment with oral melphalan plus dexamethasone produces long-term remissions in AL amyloidosis. Blood. 2007 Jul 15;110(2):787-8. Аннотация
103. Mikhael JR, Schuster SR, Jimenez-Zepeda VH, et al. Cyclophosphamide-bortezomib-dexamethasone (CyBorD) produces rapid and complete hematologic response in patients with AL amyloidosis. Blood. 2012 May 10;119(19):4391-4.Полный текст
Аннотация
Cyclophosphamide-bortezomib-dexamethasone (CyBorD) produces rapid and complete hematologic response in patients with AL amyloidosis. Blood. 2012 May 10;119(19):4391-4.Полный текст
Аннотация
104. Venner CP, Lane T, Foard D, et al. Cyclophosphamide, bortezomib, and dexamethasone therapy in AL amyloidosis is associated with high clonal response rates and prolonged progression-free survival. Blood. 2012 May 10;119(19):4387-90.Полный текст Аннотация
105. Jaccard A, Comenzo RL, Hari P, et al. Efficacy of bortezomib, cyclophosphamide and dexamethasone in treatment-naïve patients with high-risk cardiac AL amyloidosis (Mayo Clinic stage III). Haematologica. 2014 Sep;99(9):1479-85.Полный текст Аннотация
106. Palladini G, Sachchithanantham S, Milani P, et al. A European collaborative study of cyclophosphamide, bortezomib, and dexamethasone in upfront treatment of systemic AL amyloidosis. Blood. 2015 Jul 30;126(5):612-5.Полный текст
Аннотация
Palladini G, Sachchithanantham S, Milani P, et al. A European collaborative study of cyclophosphamide, bortezomib, and dexamethasone in upfront treatment of systemic AL amyloidosis. Blood. 2015 Jul 30;126(5):612-5.Полный текст
Аннотация
107. Manwani R, Cohen O, Sharpley F, et al. A prospective observational study of 915 patients with systemic AL amyloidosis treated with upfront bortezomib. Blood. 2019 Dec 19;134(25):2271-80.Полный текст Аннотация
108. Dispenzieri A, Lacy MQ, Zeldenrust SR, et al. The activity of lenalidomide with or without dexamethasone in patients with primary systemic amyloidosis. Blood. 2007 Jan 15;109(2):465-70. Аннотация
109. Moreau P, Jaccard A, Benboubker L, et al. Lenalidomide in combination with melphalan and dexamethasone in patients with newly diagnosed AL amyloidosis: a multicenter phase 1/2 dose-escalation study. Blood. 2010 Dec 2;116(23):4777-82.Полный текст
Аннотация
Blood. 2010 Dec 2;116(23):4777-82.Полный текст
Аннотация
110. Sanchorawala V, Patel JM, Sloan JM, et al. Melphalan, lenalidomide and dexamethasone for the treatment of immunoglobulin light chain amyloidosis: results of a phase II trial. Haematologica. 2013 May;98(5):789-92.Полный текст Аннотация
111. Hegenbart U, Bochtler T, Benner A, et al. Lenalidomide/melphalan/dexamethasone in newly diagnosed patients with immunoglobulin light chain amyloidosis: results of a prospective phase 2 study with long-term follow up. Haematologica. 2017 Aug;102(8):1424-31.Полный текст Аннотация
112. Kastritis E, Dialoupi I, Gavriatopoulou M, et al. Primary treatment of light-chain amyloidosis with bortezomib, lenalidomide, and dexamethasone. Blood Adv. 2019 Oct 22;3(20):3002-9.Полный текст
Аннотация
Blood Adv. 2019 Oct 22;3(20):3002-9.Полный текст
Аннотация
113. Seldin DC, Choufani EB, Dember LM, et al. Tolerability and efficacy of thalidomide for the treatment of patients with light chain-associated (AL) amyloidosis. Clin Lymphoma. 2003 Mar;3(4):241-6. Аннотация
114. Wechalekar AD, Goodman HJ, Lachmann HJ, et al. Safety and efficacy of risk-adapted cyclophosphamide, thalidomide, and dexamethasone in systemic AL amyloidosis. Blood. 2007 Jan 15;109(2):457-64. Аннотация
115. Venner CP, Gillmore JD, Sachchithanantham S, et al. A matched comparison of cyclophosphamide, bortezomib and dexamethasone (CVD) versus risk-adapted cyclophosphamide, thalidomide and dexamethasone (CTD) in AL amyloidosis. Leukemia. 2014 Dec;28(12):2304-10.Полный текст Аннотация
116. Liu B, Wang Y, Ning X, et al. A comparative study of cyclophosphamide, thalidomide and dexamethasone (CTD) versus bortezomib and dexamethasone (BDex) in light-chain amyloidosis. Curr Probl Cancer. 2021 Apr;45(2):100669.Полный текст
Аннотация
Liu B, Wang Y, Ning X, et al. A comparative study of cyclophosphamide, thalidomide and dexamethasone (CTD) versus bortezomib and dexamethasone (BDex) in light-chain amyloidosis. Curr Probl Cancer. 2021 Apr;45(2):100669.Полный текст
Аннотация
117. Gertz MA, Lacy MQ, Lust JA, et al. Phase II trial of high-dose dexamethasone for untreated patients with primary systemic amyloidosis. Med Oncol. 1999 Jul;16(2):104-9. Аннотация
118. Mahmood S, Venner CP, Sachchithanantham S, et al. Lenalidomide and dexamethasone for systemic AL amyloidosis following prior treatment with thalidomide or bortezomib regimens. Br J Haematol. 2014 Sep;166(6):842-8.Полный текст Аннотация
119. Palladini G, Milani P, Foli A, et al. A phase 2 trial of pomalidomide and dexamethasone rescue treatment in patients with AL amyloidosis. Blood. 2017 Apr 13;129(15):2120-23.Полный текст
Аннотация
Blood. 2017 Apr 13;129(15):2120-23.Полный текст
Аннотация
120. ter Haar NM, Oswald M, Jeyaratnam J, et al. Recommendations for the management of autoinflammatory diseases. Ann Rheum Dis. 2015 Sep;74(9):1636-44.Полный текст Аннотация
121. Okuda Y, Ohnishi M, Matoba K, et al. Comparison of the clinical utility of tocilizumab and anti-TNF therapy in AA amyloidosis complicating rheumatic diseases. Mod Rheumatol. 2014 Jan;24(1):137-43. Аннотация
122. Lane T, Wechalekar AD, Gillmore JD, et al. Safety and efficacy of empirical interleukin-1 inhibition using anakinra in AA amyloidosis of uncertain aetiology. Amyloid. 2017 Sep;24(3):189-93. Аннотация
123. Lachmann HJ, Gilbertson JA, Gillmore JD, et al. Unicentric Castleman’s disease complicated by systemic AA amyloidosis: a curable disease. QJM. 2002 Apr;95(4):211-8.Полный текст
Аннотация
Unicentric Castleman’s disease complicated by systemic AA amyloidosis: a curable disease. QJM. 2002 Apr;95(4):211-8.Полный текст
Аннотация
124. Lidar M, Livneh A. Familial Mediterranean fever: clinical, molecular and management advancements. Neth J Med. 2007 Oct;65(9):318-24.Полный текст Аннотация
125. Wu B, Xu T, Li Y, et al. Interventions for reducing inflammation in familial Mediterranean fever. Cochrane Database Syst Rev. 2018 Oct 19;10:CD010893.Полный текст Аннотация
126. Hoffman HM, Throne ML, Amar NJ, et al. Efficacy and safety of rilonacept (interleukin-1 Trap) in patients with cryopyrin-associated periodic syndromes: results from two sequential placebo-controlled studies. Arthritis Rheum. 2008 Aug;58(8):2443-52.Полный текст
Аннотация
2008 Aug;58(8):2443-52.Полный текст
Аннотация
127. Hoffman HM, Throne ML, Amar NJ, et al. Long-term efficacy and safety profile of rilonacept in the treatment of cryopryin-associated periodic syndromes: results of a 72-week open-label extension study. Clin Ther. 2012 Oct;34(10):2091-103.Полный текст Аннотация
128. van der Hilst JCh, Moutschen M, Messiaen PE, et al. Efficacy of anti-IL-1 treatment in familial Mediterranean fever: a systematic review of the literature. Biologics. 2016 Apr 4;10:75-80. Аннотация
129. Yilmaz S, Cinar M, Simsek I, et al. Tocilizumab in the treatment of patients with AA amyloidosis secondary to familial Mediterranean fever. Rheumatology (Oxford). 2015 Mar;54(3):564-5. Аннотация
130. Hashkes PJ, Spalding SJ, Giannini EH, et al. Rilonacept for colchicine-resistant or -intolerant familial Mediterranean fever: a randomized trial. Ann Intern Med. 2012 Oct 16;157(8):533-41. Аннотация
Hashkes PJ, Spalding SJ, Giannini EH, et al. Rilonacept for colchicine-resistant or -intolerant familial Mediterranean fever: a randomized trial. Ann Intern Med. 2012 Oct 16;157(8):533-41. Аннотация
131. Ben-Zvi I, Kukuy O, Giat E, et al. Anakinra for colchicine-resistant familial mediterranean fever: a randomized, double-blind, placebo-controlled trial. Arthritis Rheumatol. 2017 Apr;69(4):854-62. Аннотация
132. De Benedetti F, Gattorno M, Anton J, et al. Canakinumab for the treatment of autoinflammatory recurrent fever syndromes. N Engl J Med. 2018 May 17;378(20):1908-19.Полный текст Аннотация
133. Ozen S, Ben-Cherit E, Foeldvari I, et al. Long-term efficacy and safety of canakinumab in patients with colchicine-resistant familial Mediterranean fever: results from the randomised phase III CLUSTER trial. Ann Rheum Dis. 2020 Oct;79(10):1362-9.Полный текст
Аннотация
Ann Rheum Dis. 2020 Oct;79(10):1362-9.Полный текст
Аннотация
134. Kacar M, Savic S, van der Hilst JCH. The efficacy, safety and tolerability of canakinumab in the treatment of familial mediterranean fever: a systematic review of the literature. J Inflamm Res. 2020;13:141-9. Аннотация
135. Adams D, Suhr OB, Hund E, et al. First European consensus for diagnosis, management, and treatment of transthyretin familial amyloid polyneuropathy. Curr Opin Neurol. 2016 Feb;29(suppl 1):S14-26.Полный текст Аннотация
136. Ando Y, Coelho T, Berk JL, et al. Guideline of transthyretin-related hereditary amyloidosis for clinicians. Orphanet J Rare Dis. 2013 Feb 20;8:31.Полный текст Аннотация
137. Tsuchiya A, Yazaki M, Kametani F, et al. Marked regression of abdominal fat amyloid in patients with familial amyloid polyneuropathy during long-term follow-up after liver transplantation. Liver Transpl. 2008 Apr;14(4):563-70.Полный текст
Аннотация
Tsuchiya A, Yazaki M, Kametani F, et al. Marked regression of abdominal fat amyloid in patients with familial amyloid polyneuropathy during long-term follow-up after liver transplantation. Liver Transpl. 2008 Apr;14(4):563-70.Полный текст
Аннотация
138. Ericzon BG, Wilczek HE, Larsson M, et al. Liver transplantation for hereditary transthyretin amyloidosis: after 20 years still the best therapeutic alternative? Transplantation. 2015 Sep;99(9):1847-54.Полный текст Аннотация
139. Okumura K, Yamashita T, Masuda T, et al. Long-term outcome of patients with hereditary transthyretin V30M amyloidosis with polyneuropathy after liver transplantation. Amyloid. 2016;23(1):39-45. Аннотация
140. Cristóbal Gutiérrez H, Pelayo-Negro AL, Gómez Gómez D, et al. Overview of treatments used in transthyretin-related hereditary amyloidosis: a systematic review. Eur J Hosp Pharm. 2020 Jul;27(4):194-201.s Аннотация
Overview of treatments used in transthyretin-related hereditary amyloidosis: a systematic review. Eur J Hosp Pharm. 2020 Jul;27(4):194-201.s Аннотация
141. Milani P, Mussinelli R, Perlini S, et al. An evaluation of patisiran: a viable treatment option for transthyretin-related hereditary amyloidosis. Expert Opin Pharmacother. 2019 Dec;20(18):2223-8. Аннотация
142. Adams D, Gonzalez-Duarte A, O’Riordan WD, et al. Patisiran, an RNAi therapeutic, for hereditary transthyretin amyloidosis. N Engl J Med. 2018 Jul 5;379(1):11-21. Аннотация
143. Adams D, Polydefkis M, González-Duarte A, et al. Long-term safety and efficacy of patisiran for hereditary transthyretin-mediated amyloidosis with polyneuropathy: 12-month results of an open-label extension study. Lancet Neurol. 2021 Jan;20(1):49-59. Аннотация
144. Benson MD, Waddington-Cruz M, Berk JL, et al. Inotersen treatment for patients with hereditary transthyretin amyloidosis. N Engl J Med. 2018 Jul 5;379(1):22-31. Аннотация
Benson MD, Waddington-Cruz M, Berk JL, et al. Inotersen treatment for patients with hereditary transthyretin amyloidosis. N Engl J Med. 2018 Jul 5;379(1):22-31. Аннотация
145. Brannagan TH, Wang AK, Coelho T, et al. Early data on long-term efficacy and safety of inotersen in patients with hereditary transthyretin amyloidosis: a 2-year update from the open-label extension of the NEURO-TTR trial. Eur J Neurol. 2020 Aug;27(8):1374-81.Полный текст Аннотация
146. Coelho T, Maia LF, Martins da Silva A, et al. Tafamidis for transthyretin familial amyloid polyneuropathy: a randomized, controlled trial. Neurology. 2012 Aug 21;79(8):785-92.Полный текст Аннотация
147. Barroso FA, Judge DP, Ebede B, et al. Long-term safety and efficacy of tafamidis for the treatment of hereditary transthyretin amyloid polyneuropathy: results up to 6 years. Amyloid. 2017 Sep;24(3):194-204.Полный текст
Аннотация
Amyloid. 2017 Sep;24(3):194-204.Полный текст
Аннотация
148. Greene MJ, Klimtchuk ES, Seldin DC, et al. Cooperative stabilization of transthyretin by clusterin and diflunisal. Biochemistry. 2015 Jan 20;54(2):268-78.Полный текст Аннотация
149. Berk JL, Suhr OB, Obici L, et al. Repurposing diflunisal for familial amyloid polyneuropathy: a randomized clinical trial. JAMA. 2013 Dec 25;310(24):2658-67.Полный текст Аннотация
150. Dubrey SW, Davidoff R, Skinner M, et al. Progression of ventricular wall thickening after liver transplantation for familial amyloidosis. Transplantation. 1997 Jul 15;64(1):74-80. Аннотация
151. Herlenius G, Wilczek HE, Larsson M, et al. Ten years of international experience with liver transplantation for familial amyloidotic polyneuropathy: results from the Familial Amyloidotic Polyneuropathy World Transplant Registry. Transplantation. 2004 Jan 15;77(1):64-71. Аннотация
Ten years of international experience with liver transplantation for familial amyloidotic polyneuropathy: results from the Familial Amyloidotic Polyneuropathy World Transplant Registry. Transplantation. 2004 Jan 15;77(1):64-71. Аннотация
152. Maurer MS, Schwartz JH, Gundapaneni B, et al. Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med. 2018 Sep 13;379(11):1007-16. Аннотация
153. Damy T, Garcia-Pavia P, Hanna M, et al. Efficacy and safety of tafamidis doses in the Tafamidis in Transthyretin Cardiomyopathy Clinical Trial (ATTR-ACT) and long-term extension study. Eur J Heart Fail. 2020 Oct 18 [Epub ahead of print].Полный текст Аннотация
154. Rapezzi C, Elliott P, Damy T, et al. Efficacy of tafamidis in patients with hereditary and wild-type transthyretin amyloid cardiomyopathy: further analyses from ATTR-ACT. JACC Heart Fail. 2021 Feb;9(2):115-23.Полный текст
Аннотация
JACC Heart Fail. 2021 Feb;9(2):115-23.Полный текст
Аннотация
155. Gertz MA, Lacy MQ, Dispenzieri A, et al. Transplantation for amyloidosis. Curr Opin Oncol. 2007 Mar;19(2):136-41. Аннотация
156. Gertz MA. Immunoglobulin light chain amyloidosis: 2014 update on diagnosis, prognosis, and treatment. Am J Hematol. 2014 Dec;89(12):1132-40. Аннотация
157. Kaufman GP, Schrier SL, Lafayette RA, et al. Daratumumab yields rapid and deep hematologic responses in patients with heavily pretreated AL amyloidosis. Blood. 2017 Aug 17;130(7):900-2.Полный текст Аннотация
158. Schwotzer R, Manz MG, Pederiva S, et al. Daratumumab for relapsed or refractory AL amyloidosis with high plasma cell burden. Hematol Oncol. 2019 Dec;37(5):595-600. Аннотация
Hematol Oncol. 2019 Dec;37(5):595-600. Аннотация
159. Sanchorawala V, Sarosiek S, Schulman A, et al. Safety, tolerability, and response rates of daratumumab in relapsed AL amyloidosis: results of a phase 2 study. Blood. 2020 Apr 30;135(18):1541-7. Аннотация
160. Kimmich CR, Terzer T, Benner A, et al. Daratumumab for systemic AL amyloidosis: prognostic factors and adverse outcome with nephrotic-range albuminuria. Blood. 2020 Apr 30;135(18):1517-30. Аннотация
161. Lecumberri R, Krsnik I, Askari E, et al. Treatment with daratumumab in patients with relapsed/refractory AL amyloidosis: a multicentric retrospective study and review of the literature. Amyloid. 2020 Sep;27(3):163-7. Аннотация
162. Kastritis E, Roussakis P, Kostopoulos IV, et al. Short daratumumab consolidation in patients with AL amyloidosis or LCCD improves complete response rates and modifies bone marrow microenvironment. Blood. 2020;136(supp 1):25.Полный текст
Blood. 2020;136(supp 1):25.Полный текст
163. Solomon A, Weiss DT, Wall JS. Therapeutic potential of chimeric amyloid-reactive monoclonal antibody 11-1F4. Clin Cancer Res. 2003 Sep 1;9(10 Pt 2):s3831-8.Полный текст Аннотация
164. Solomon A, Weiss DT, Wall JS. Immunotherapy in systemic primary (AL) amyloidosis using amyloid-reactive monoclonal antibodies. Cancer Biother Radiopharm. 2003 Dec;18(6):853-60. Аннотация
165. Edwards CV, Gould J, Langer AL, et al. Analysis of the phase 1a/b study of chimeric fibril-reactive monoclonal antibody 11-1F4 in patients with relapsed or refractory AL amyloidosis. Amyloid. 2017 Mar;24(sup1):58-9.Полный текст Аннотация
166. Valent J, Silowsky J, Kurman MR, et al. CAEL-101 is well-tolerated in AL amyloidosis patients receiving concomitant cyclophosphamide-bortezomib-dexamethasone (CyborD): a phase 2 dose-finding study (NCT04304144). Blood. 2020;136 (suppl 1):26-7.Полный текст
CAEL-101 is well-tolerated in AL amyloidosis patients receiving concomitant cyclophosphamide-bortezomib-dexamethasone (CyborD): a phase 2 dose-finding study (NCT04304144). Blood. 2020;136 (suppl 1):26-7.Полный текст
167. Parker TL, Rosenthal A, Sanchorawala V, et al. A phase II study of isatuximab (SAR650984) (NSC-795145) for patients with previously treated AL amyloidosis (SWOG S1702; NCT#03499808). Blood. 2020;136(supp 1):20–21.Полный текст Аннотация
168. Gertz MA, Lacy MQ, Dispenzieri A, et al. Effect of hematologic response on outcome of patients undergoing transplantation for primary amyloidosis: importance of achieving a complete response. Haematologica. 2007 Oct;92(10):1415-8. Аннотация
169. Dittrich T, Benner A, Kimmich C, et al. Performance analysis of AL amyloidosis cardiac biomarker staging systems with special focus on renal failure and atrial arrhythmia. Haematologica. 2019 Jul;104(7):1451-9.Полный текст
Аннотация
Haematologica. 2019 Jul;104(7):1451-9.Полный текст
Аннотация
170. Muchtar E, Therneau TM, Larson DR, et al. Comparative analysis of staging systems in AL amyloidosis. Leukemia. 2019 Mar;33(3):811-4. Аннотация
МГУ ВМК Языки программирования
← →
Denis__ ©
(2008-08-27 10:56) [0]
Какие изучаются? Кто-то ж должен знать:)
← →
oldman ©
(2008-08-27 11:00) [1]
Наверное, как везде.
Pascal, С, ASM, Sql
← →
Ega23 ©
(2008-08-27 11:02) [2]
> Какие изучаются?
Гм. .. Я всю жизнь считал, что в университете ты не какой-то конкретный язык программирования изучаешь, а методологию…
.. Я всю жизнь считал, что в университете ты не какой-то конкретный язык программирования изучаешь, а методологию…
← →
oldman ©
(2008-08-27 11:03) [3]
> Ega23 © (27.08.08 11:02) [2]
Для разных методов примеры изучаются на разных языках
Не будешь же ты работу с БД на ассемблере писать
← →
Denis__ ©
(2008-08-27 11:05) [4]
> Я всю жизнь считал, что в университете ты не какой-то конкретный
> язык программирования изучаешь, а методологию…
Я вообще ещё не имею такого мнения:) Ибо только первый курс, а сейчас ещё даже не 1 сентября.
> Pascal, С, ASM, Sql
С, С++, С# ?
← →
Skyle ©
(2008-08-27 11:07) [5]
Java?
← →
clickmaker ©
(2008-08-27 11:07) [6]
> в университете ты не какой-то конкретный язык программирования
> изучаешь
мы изучали плюсы
на другом факе люди изучали паскаль
собственно методологии, если под ней понимать всякие там ООД, паттерны, UML, не было
← →
oldman ©
(2008-08-27 11:09) [7]
> Denis__ © (27. 08.08 11:05) [4]
08.08 11:05) [4]
Вряд ли будут такие тонкости с синтаксисом. Просто основы дают.
pascal (object pascal, ессно) — ооп
c — системное программирование
asm — работа с регистрами напрямую
sql — базы данных
← →
Denis__ ©
(2008-08-27 11:11) [8]
> pascal (object pascal, ессно) — ооп
Delphi?
или под дос?
← →
data ©
(2008-08-27 11:18) [9]
нв вмк очень хорошо учат метологии программирования (как уже отмечалось выше). Какой язык уже после этого не важно.
Программирование лекции и семинары идет на первых двух курсах одинаковое для всего курса, тогда и учат методологии. После распределения по кафедрам программированию уже не учат, а есть только практикум по направлению кафедры. Если пойдешь, например, на кафедру АЯ (алгоритм. языки), то будешь изучать подробно не только сами языки, а более глобальные вещи: теорию трансляции, грамматики и пр.
Если пойдешь, например, на кафедру АЯ (алгоритм. языки), то будешь изучать подробно не только сами языки, а более глобальные вещи: теорию трансляции, грамматики и пр.
← →
oldman ©
(2008-08-27 11:18) [10]
> Denis__ © (27.08.08 11:11) [8]
У нас был и под dos (лабы), и delphi (курсач, диплом)
← →
Ega23 ©
(2008-08-27 11:19) [11]
> Delphi?
> или под дос?
>
А какая тебе разница, на чём написать функцию, которая проверяет правильность расставления скобок в строке???
← →
data ©
(2008-08-27 11:20) [12]
> У нас был и под dos (лабы), и delphi (курсач, диплом)
у нас был паскаль дос, асм (на первых двух курсах) и фортран (практикум на кафедре, кафедра ИО). Но это давно было.
Но это давно было.
← →
Denis__ ©
(2008-08-27 11:22) [13]
> теорию трансляции,
Это то, о чём тут иногда появляются ветки?:) «Люди, пгите, сам я в сях не шарю, как это будет на делфи»
oldman, data спасибо. Теперь буду знать чего ожидать.
← →
Ega23 ©
(2008-08-27 11:24) [14]
> Это то, о чём тут иногда появляются ветки?:) «Люди, пгите,
> сам я в сях не шарю, как это будет на делфи»
нет, это несколько другое.
← →
Denis__ ©
(2008-08-27 11:25) [15]
> нет, это несколько другое.
🙂 Насколько другое?
← →
Ega23 ©
(2008-08-27 11:26) [16]
> 🙂 Насколько другое?
У тебя гугл не работает?
← →
Denis__ ©
(2008-08-27 11:31) [17]
Работает. Ладно, пошло-поехало. Понятно всё. Учат не языкам, а метологии. Языки без тонкостей синтаксиса. Всем спасибо.
← →
TUser ©
(2008-08-27 12:03) [18]
кого знаю оттуда, — пишут на всем
есть правда разные отделения
← →
@!!ex ©
(2008-08-27 12:10) [19]
>
> [8] Denis__ © (27. 08.08 11:11)
08.08 11:11)
>
> > pascal (object pascal, ессно) — ооп
>
> Delphi?
> или под дос?
Других компиляторов под Винду кроме Дельфи не знаем?
← →
Ega23 ©
(2008-08-27 12:16) [20]
> Других компиляторов под Винду кроме Дельфи не знаем?
Не, ну сайт-то всё-таки о delphi… 🙂
← →
@!!ex ©
(2008-08-27 12:25) [21]
> [20] Ega23 © (27.08.08 12:16)
Не только. Здесь есть форум по FreePascal
← →
Petr V. Abramov ©
(2008-08-27 13:01) [22]
там думать учат, а не языкам программирования.
← →
Tricky
(2008-08-27 14:23) [23]
Интересно универы закупают ПО (тот же MVC) или по старинке — кряками?
Когда я учился (5 лет назад) — все По было хакнутое. А как сейчас?
← →
Как — то так
(2008-08-27 14:29) [24]
сейчас закупают. По образовательным программмам ВУЗам это очень дешево получается.
← →
@!!ex ©
(2008-08-27 14:33) [25]
Покупают и используют свободные варианты.
FreePascal, MSVC Express
← →
TUser ©
(2008-08-27 16:00) [26]
Винда и МС-ские компиляторы стоят буквально копейки для ВУЗов.
← →
ketmar ©
(2008-08-27 17:33) [27]
>[7] oldman © (2008-08-27 11:09:00)
>pascal (object pascal, ессно) — ооп
за что, кстати, надо бить урановым ломом по черепу.
>[22] Petr V. Abramov © (2008-08-27 13:01:00)
>там думать учат, а не языкам программирования.
фигня. нигде думать не учат. «дают возможость самом научится, предоставляют материалы» — это да.
—
Understanding is not required. Only obedience.
← →
ketmar ©
(2008-08-27 17:34) [28]
>[26] TUser © (2008-08-27 16:00:00)
>Винда и МС-ские компиляторы стоят буквально копейки для ВУЗов.
а GNU/Linux, g++ и Qt вообще бесплатно. %-)
—
Do what thou wilt shall be the whole of the Law.
← →
Anatoly Podgoretsky ©
(2008-08-27 20:44) [29]
> Ega23 (27.08.2008 11:02:02) [2]
Ты когда последний раз в университете учился?
← →
Nic ©
(2008-08-27 21:11) [30]
В моём ВУЗе на 12000 студентов лицензионного софта — единичные лицензии. В основном, всё палёное.
← →
Юрий Зотов ©
(2008-08-27 21:22) [31]
> ketmar © (27.08.08 17:33) [27]
> фигня. нигде думать не учат. «дают возможость самом научится,
> предоставляют материалы»
Откуда знаешь?
← →
ketmar ©
(2008-08-27 23:22) [32]
>[31] Юрий Зотов © (2008-08-27 21:22:00)
>Откуда знаешь?
из универа. для того, чтобы учить думать — надо заниматься индивидуально. а на потоке можно дать инфу, методы, некоторые примеры использования — а дальше сам. кто-то учится решать задачи («думать»), а кто-то — применять типовые решения (и зависает в нестандартных ситуациях).
для того, чтобы учить думать — надо заниматься индивидуально. а на потоке можно дать инфу, методы, некоторые примеры использования — а дальше сам. кто-то учится решать задачи («думать»), а кто-то — применять типовые решения (и зависает в нестандартных ситуациях).
—
All Your Base Are Belong to Us
← →
Юрий Зотов ©
(2008-08-27 23:42) [33]
> ketmar © (27.08.08 23:22) [32]
Нас учили думать. Вряд ли Преподы кончились.
← →
ketmar ©
(2008-08-27 23:59) [34]
>[33] Юрий Зотов © (2008-08-27 23:42:00)
значит, тебе повезло. по опыту меня и знакомых — кончились. ты ж вот тоже не преподаешь, так? %-)
—
Understanding is not required. Only obedience.
← →
+koha
(2008-08-28 01:38) [35]
> Юрий Зотов © (27.08.08 23:42) [33]
> > ketmar © (27.08.08 23:22) [32]Нас учили думать. Вряд
> ли Преподы кончились.
Преподы не кончились — их прикончили мелкие зарплаты…
← →
Германн ©
(2008-08-28 02:04) [36]
> Ega23 © (27.08.08 11:02) [2]
>
>
> > Какие изучаются?
>
>
> Гм… Я всю жизнь считал, что в университете ты не какой-
> то конкретный язык программирования изучаешь, а методологию.
> ..
>
Есть некая разница между тем чему учили и тем что хочешь изучить. Надеюсь (и уверен), что ты это понимаешь.
> Юрий Зотов © (27.08.08 23:42) [33]
>
> > ketmar © (27.08.08 23:22) [32]
>
> Нас учили думать. Вряд ли Преподы кончились.
>
Не. Не кончились. Есть ещё. Есть!
← →
Ega23 ©
(2008-08-28 09:43) [37]
> Ты когда последний раз в университете учился?
Самый последний — 5 лет назад… 🙂
← →
Пробежал…
(2008-08-28 11:30) [38]
> А какая тебе разница, на чём написать функцию, которая проверяет
> правильность расставления скобок в строке???
ну ка напиши это на SQL-92
← →
Ega23 ©
(2008-08-28 11:50) [39]
> ну ка напиши это на SQL-92
А в SQL-92 есть понятие функция? 🙂
← →
Denis__ ©
(2008-08-28 12:01) [40]
> кого знаю оттуда, — пишут на всем
O_0 И как пишут?
← →
Ega23 ©
(2008-08-28 12:06) [41]
> И как пишут?
Правильно пишут.
← →
Denis__ ©
(2008-08-28 12:27) [42]
> Правильно пишут.
🙂
← →
Пробежал…
(2008-08-28 12:44) [43]
> А в SQL-92 есть понятие функция? 🙂
эк какой хитрый попался 😉
ну ладно, напиши выражение, которое будет делать обозначенное 😉 Если все равно на чем писать 😉
Клинические рекомендации по диагностике и лечению системного амилоидоза. Клиническая фармакология и терапия
Клинические рекомендации
Л.В. Лысенко (Козловская),
В.В. Рамеев,
С.В. Моисеев,
О.В. Благова,
Э.И. Богданов,
Г.Е. Гендлин,
Д. А. Гришина,
А.Я. Гудкова,
Е.В. Захарова,
О.Е. Зиновьева,
О.М. Моисеева,
С.С. Никитин,
В.А. Парфенов,
Н.А. Супонева,
С.Н. Терещенко
А. Гришина,
А.Я. Гудкова,
Е.В. Захарова,
О.Е. Зиновьева,
О.М. Моисеева,
С.С. Никитин,
В.А. Парфенов,
Н.А. Супонева,
С.Н. Терещенко
- DOI
- 10.32756/ 0869-5490-2020-1-13-24
- Количество просмотров
- 21286
Скачать статью в PDF
В клинических рекомендациях, подготовленных специалистами различного профиля, рассматриваются методы диагностики и лечениясистемного амилоидоза, в том числе АА (вто-ричный амилоидоз при хронических воспалительных заболеваниях, включая ревматоидныйартрит, анкилозирующий спондилит, аутовоспалительные заболевания, хроническиенагноения, злокачественные опухоли и др.), AL (амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема) иATTR (транстиретиновый; семейные формыполиневропатического, кардиопатического идругого амилоидоза, системный старческийамилоидоз). Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
Метки статьи
Определение, классификация, группы риска и принципы диагностики
Амилоидоз – группа заболеваний, отличительным признаком которых является отложение в тканях и органах
фибриллярного гликопротеида амилоида. Специфическое свойство амилоида, отличающее его от других фибриллярных
белков стромы, – способность к двойному лучепреломлению, что проявляется свечением в поляризованном свете
предварительно окрашенных конгокрасным препаратов амилоида с изменением красного цвета конгофильных амилоидных
отложений на яблочно-зеленый (дихроизм).
Специфическое свойство амилоида, отличающее его от других фибриллярных
белков стромы, – способность к двойному лучепреломлению, что проявляется свечением в поляризованном свете
предварительно окрашенных конгокрасным препаратов амилоида с изменением красного цвета конгофильных амилоидных
отложений на яблочно-зеленый (дихроизм).
В основе амилоидогенеза лежит синтез большого количества нестабильных белковпредшественников, которые
агрегируются с образованием амилоидной фибриллы. Клю чевое значение имеет амилоидогенность основного
белка-предшественника амилоида, специфичного для каждой формы амилоидоза (в настоящее время известно более 30
таких белков), обозначение которого положено в основу современной классификации заболевания (ВОЗ, 2016 г.).
Названия типов амилоида включают в себя букву А, означающую “амилоид», и обозначение конкретного фибриллярного
белка амилоида – А (амилоидный А-протеин), L (легкие цепи иммуноглобулинов), TTR (транстиретин), β2М
(β2-микроглобулин), В (В-протеин), IAPP (островковый амилоидный полипептид). Используют также
производные наименования – иммуноглобулиновый амилоидоз (AL), транстиретиновый (ATTR) и др. (табл. 1) [1-3].
Следует отметить, что Международная классификация болезней (МКБ) 10-го пересмотра базируется на клиническом
принципе, не учитывает особенности патогенеза различных форм амилоидоза и не позволяет обосновать адекватное
лечение.
Используют также
производные наименования – иммуноглобулиновый амилоидоз (AL), транстиретиновый (ATTR) и др. (табл. 1) [1-3].
Следует отметить, что Международная классификация болезней (МКБ) 10-го пересмотра базируется на клиническом
принципе, не учитывает особенности патогенеза различных форм амилоидоза и не позволяет обосновать адекватное
лечение.
| Белок амилоида | Белок-Белок-предшественник | Клиническая форма амилоидоза |
|---|---|---|
| АА | SSA-белок | Вторичный амилоидоз при хронических воспалительных заболеваниях, в том числе периодической болезни и синдроме Макла-Уэллса |
| AL | λ, κ-легкие цепи иммуноглобулинов | Амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема |
| ATTR | Транстиретин | Семейные формы полиневропатического, кардиопатического и др. амилоидоза, системный старческий
амилоидоз амилоидоза, системный старческий
амилоидоз |
| Аβ2М | β2-микроглобулин | Диализный амилоидоз |
| AGel | Гелсолин | Финская семейная амилоидная полиневропатия |
| AApoAI | Аполипопротеин А-I | Амилоидная полиневропатия (III тип по van Allen, 1956 г.) |
| AFib | Фибриноген | Амилоидная нефропатия |
| Aβ2 | β-белок | Болезнь Альцгеймера, синдром Дауна, наследственные кровоизлияния в мозг с амилоидозом |
| APrPScr | Прионовый белок | Болезнь Крейтцфельда-Якоба, болезнь Герстманна-Штраусслера-Шейнкера |
| AANF | Предсердный натрийуретический фактор | Изолированный амилоидоз предсердий |
| AIAPP | Амилин | Изолированный амилоидоз в островках Лангерганса при сахарном диабете 2 типа, инсулиноме |
| ACal | Прокальцитонин | При медуллярном раке щитовидной железы |
| ACys | Цистатин С | Наследственные кровоизлияния в мозг с амилоидозом (Исландия) |
АА-амилоидоз чаще всего развивается при ревматоидном артрите, серонегативных спондилоартропатиях,
аутовоспалительных наследственных периодических лихорадках, в том числе периодической болезни (семейной
средиземноморской лихорадке), а также при хронических нагноениях, туберкулезе. АА-амилоид образуется из
сывороточного предшественника SAA (serum amyloid A) – острофазового белка, продуцируемого в значительных
количествах в ответ на воспаление. По этой причине АА-амилоидоз называют также реактивным или вторичным.
АА-амилоид образуется из
сывороточного предшественника SAA (serum amyloid A) – острофазового белка, продуцируемого в значительных
количествах в ответ на воспаление. По этой причине АА-амилоидоз называют также реактивным или вторичным.
Клинические формы AL-амилоидоза обусловлены единым этиологическим фактором – В-лимфоцитарной дискразией,
характеризующейся формированием аномального клона плазматических или В-клеток в костном мозге, которые
продуцируют аномальные иммуноглобулины, обладающие амилоидогенностью (легкие цепи моноклонального
иммуноглобулина, чаще λ, реже κ-типа). При первичном AL-амилоидозе плазмоклеточная дискразия относительно более
доброкачественная, в то время как при В-гемобластозах (множественной миеломе, болезни Вальденстрема и др.) она
обладает признаками злокачественной опухоли. Аномальный амилоидогенный клон плазматических клеток может
формироваться также из плазмоцитов, локализующихся вне костного мозга, что может привести к развитию локального
амилоидоза. Наиболее распространенные локальные формы AL-амилоидоза – амилоидоз трахеи, бронхов и гортани,
мочевого пузыря. Выявление плазмоклеточной дискразии необходимо для диагностики AL-амилоидоза, а также для
оценки его риска и дифференциального диагноза.
Наиболее распространенные локальные формы AL-амилоидоза – амилоидоз трахеи, бронхов и гортани,
мочевого пузыря. Выявление плазмоклеточной дискразии необходимо для диагностики AL-амилоидоза, а также для
оценки его риска и дифференциального диагноза.
ATTR-амилоидоз является необратимо прогрессирующим заболеванием с высокой степенью инвалидизации вследствие тяжелого поражения сердца, периферической и/или автономной полиневропатии. Пациенты обычно умирают в течение 10-12 лет от первых проявлений. Развитие ATTR-амилоидоза обусловлено мутациями в молекуле транстиретина или возрастным нарушением секреции тетрамеров транстиретина печенью. В обоих случаях происходит распад тетрамеров транстиретина до мономеров, обладающих выраженной конформационной нестабильностью.
Рекомендации:
- Скрининг АА-амилоидоза следует проводить в следующих группах риска: серопозитивные и серонегативные
хронические полиартриты (ревматоидный артрит, анкилозирующий спондилоартрит, ювенильный хронический артрит,
псориатический артрит, синдром Рейтера и др.
 ), воспалительные заболевания кишечника (болезнь Крона, язвенный
колит), аутовоспалительные заболевания (подагра тяжелого рецидивирующего течения, семейные периодические
лихорадки – периодическая болезнь, криопиринопатии, TRAPS, гипериммуно глобулинемия D), хронические
нагноения (туберкулез, бронхоэктатическая болезнь, остеомиелит и др.), злокачественные солидные опухоли
[1,2,4-6].
), воспалительные заболевания кишечника (болезнь Крона, язвенный
колит), аутовоспалительные заболевания (подагра тяжелого рецидивирующего течения, семейные периодические
лихорадки – периодическая болезнь, криопиринопатии, TRAPS, гипериммуно глобулинемия D), хронические
нагноения (туберкулез, бронхоэктатическая болезнь, остеомиелит и др.), злокачественные солидные опухоли
[1,2,4-6]. - Риск АА-амилоидоза у больных с хроническими воспалительными заболеваниями повышается при персистирующем
увеличении уровней маркеров острой фазы воспаления (С-реактивный белок, SAA), наличии анемии хронических
заболеваний (с повышением уровня ферритина крови), особенно в сочетании с суставным синдромом (синовитом)
[4,6-12]. Дина мический контроль за уровнем этих показателей необходим также при мониторировании течения
диагностированного АА-амилоидоза. Для оценки риска развития или прогрессирования АА-амилоидоза в условиях
преимущественного аутовоспаления или с целью выявления субклинической активации воспаления можно определять
сывороточный маркер нейтрофильной активности S100A12 (кальгранулин) [4,13-15].

- Диагностика аутовоспалительных заболеваний предполагает, в первую очередь, проведение генетического исследования на мутации генов MEFV (пирин), NLRP3 (криопирин), TRAPS (рецептор к фактору некроза опухоли альфа), мевалонаткиназы [4,16-25].
- Высокая частота олигосекреторных моноклональных гаммапатий у лиц старше 50 лет требует скринингового обследования этой группы лиц на предмет моноклональных гаммапатий. Наиболее чувствительным и недорогим турбидиметрическим методом для скрининговой диагностики являет Freelite-метод количественной оценки уровня свободных легких цепей иммуноглобулинов. Все больные с плазмоклеточными дискразиями и лимфопролиферативными заболеваниями входят в группу риска AL-амилоидоза [26-34].
- У пациентов с морфологически подтвержденным амилоидозом диагностика AL-амилоидоза предполагает проведение
иммунохимического исследования с применением высокочувствительных методов – иммунофиксации сыворотки и
суточной мочи, количественного определения свободных легких цепей иммуноглобулинов (Freelite) [26-35].

- Помимо выявления моноклональной гаммапатии, диагностика плазмоклеточной дискразии предполагает выявление и оценку количества плазмоцитов костного мозга, а также их структурных особенностей. Применение цитогенетического исследования и иммунофенотипирования плазмоцитов важно для уточнения клональности и злокачественности аберрантного клона плазматических клеток, в особенности в редких случаях неинформативности иммунохимического исследования крови и суточной мочи [26,33-34,36,37].
- Важное значение в диагностике плазмоклеточных дискразий имеют также иммуногистохимические методы выявления патологического клона плазматических клеток. Это особенно важно для диагностики, типирования и лечения локального варианта ALамилоидоза [35].
- ATTR-амилоидоз следует подозревать у пациентов с полиневропатией, необъяснимым чередованием запоров и
диареи, синдромом карпального канала, особенно при наличии полиневропатии, синдрома карпального канала,
кардиомиопатии у родственников.
 Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].
Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47]. - Диагностика амилоидоза основывается на результатах морфологического исследования [1-2,39,48].
- При системном амилоидозе для диагностики амилоидного поражения органа нет необходимости проводить его биопсию у больных с ранее верифицированным диагнозом амилоидоза по результатам биопсии другого органа. Однако точная диагностика возможна только с помощью морфологического исследования [1,48].
- С целью выявления амилоида необходимо окрашивание препаратов ткани красителем конго-красный с последующей
микроскопией в поляризованном свете. Окончательный диагноз амилоидоза устанавливают при выявлении
конгофильных масс, обладающих способностью к яблочно-зеленому или желтоватому свечению в поляризованном
свете [1,39,48]. Для более точной диагностики амилоидоза применяют также метод окраски тиофлафином Т,
который дает светло-зеленое свечение амилоида [1,2].

- При системном амилоидозе информативна биопсия прямой или двенадцатиперстной кишки (с захватом подслизистого слоя). ATTR-амилоид отличается слабой конгофилией. По этой причине выявить этот тип амилоида нередко удается только при повторных биопсиях из разных органов – аспирационной биопсии подкожной жировой клетчатки, биопсии слюнных желез губ и др. Наиболее эффективна биопсия пораженного органа [1-2,39,48]. У пациентов с синдромом запястного канала исследованию на амилоид необходимо подвергать ткань, удаленную при оперативной декомпрессии запястного канала.
- Не рекомендуется проводить биопсию подкожной жировой клетчатки у больных инсулинозависимым сахарным диабетом, так как в местах иньекций инсулин может агрегировать и формировать амилоидные депозиты [48].
- Для дифференциальной диагностики АА-амилоидоза от AL- и ATTR-амилоидоза используют окрасочные методы при
тщательном учете клинических предпосылок разных типов амилоидоза [48,49].

- Наиболее эффективным методом типирования является иммуногистохимическое исследование. Поскольку некоторые антисыворотки могут давать перекрестные реакции с разными типами амилоида, исследование целесообразно проводить с панелью антисывороток. Для неспециализированных терапевтических и нефрологических стационаров рекомендуется применение панели антисывороток к SAA, разным типам тяжелых цепей иммуноглобулинов, легким цепям иммуноглобулинов λ и κ, транстиретину. Важно также использовать антисыворотки к фибриногену [36,50].
- Для диагностики ATTR-амилоидоза необходимо генетическое исследование на наличие мутации гена транстиретина [39].
Клинические проявления
Для вторичного АА-амилоидоза характерно более раннее начало, чем для AL-амилоидоза (средний возраст больных
составляет около 40 и 65 лет, соответственно). ATTR-амилоидоз, несмотря на наследственную природу,
характеризуется низкой пенетрантностью и также проявляется обычно после 35 лет.
Поражение почек – ведущий клинический признак АА- и AL-амилоидоза, наблюдающийся практически у всех больных. Поражение почек встречается и у больных с многими формами семейного амилоидоза (AFib, ALys, AGel и др.). При ATTR-амилоидозе нефропатия отмечается лишь у 20-23% больных. Клинически амилоидная нефропатия характеризуется неуклонно прогрессирующим течением с последовательной сменой стадий: протеинурия, нефротический синдром, хроническая почечная недостаточность (ХПН). Иногда возможно развитие ХПН без предшествующего нефротического синдрома.
Поражение сердца развивается у подавляющего большинства больных AL-амилоидозом и у 50-60% пациентов с
АTTR-амилоидозом, но не характерно для АА-амилоидоза (рис. 1). При эхокардиографии у больных амилоидозом сердца
наблюдается утолщение межжелудочковой перегородки и стенки левого желудочка (чаще симметричное), которое не
сопровождается электрокардиографическими признаками гипертрофии миокарда. У части больных отмечается снижение
вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение
диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности,
которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме
того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
У части больных отмечается снижение
вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение
диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности,
которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме
того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
При AL-амилоидозе и особенно ATTR-амилоидозе часто встречается ортостатическая артериальная гипотензия – вариант
сосудистой недостаточности, при которой сосуды теряют способность поддерживать нормальное артериальное давление
в условиях ортостатических нагрузок. Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в
сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз
нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к
развитию острого нарушения мозгового кровообращения.
Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в
сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз
нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к
развитию острого нарушения мозгового кровообращения.
Поражение желудочно-кишечного тракта может проявляться, особенно при AL-амилоидозе, тяжелой диареей или динамической непроходимостью, которые чаще связаны с нарушениями моторики кишечника вследствие дисфункции автономных нервных сплетений. Иногда выявляют изъязвления или перфорацию стенок с возможным кровотечением. При поражении пищевода возможна дисфагия.
Поражение печени при АА- и AL-типах амилоидоза наблюдают практически в 100% случаев. Функция печени чаще остается сохранной, редким признаком амилоидоза печени является внутрипеченочная портальная гипертензия. При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
Увеличение селезенки, обусловленное амилоидным поражением, отмечается у большинства больных и обычно сопутствует увеличению печени.
Поражение нервной системы, представленное симптомами периферической соматической и автономной невропатии, отмечают у 17-35% больных AL-амилоидозом и практически у всех пациентов с наследственной амилоидной полиневропатией разных типов (ATTR, AApoA1 и др.). В большинстве случаев развивается дистальная симметричная полиневропатия с неуклонно прогрессирующим течением, различные дисфункции автономной нервной системы. Реже выявляют двусторонний синдром запястного канала, обусловленный сдавлением срединного нерва депозитами амилоида.
Поражение кожи наблюдают почти у 40% больных AL-амилоидозом. Помимо параорбитальных геморрагий описаны также
папулы, бляшки, узелки, пузырьковые высыпания, склеродермоподобная индурация кожи.
Амилоидные отложения в мышцах чаще встречаются при AL-амилоидозе. Макроглоссия – патогномоничный симптом AL-амилоидоза, развивающийся примерно у 20% пациентов.
Редким проявлением амилоидоза, описанным при AL- и, в особенности, АTTR-типах, бывает поражение глаз (сухой кератоконъюнктивит, вторичная глаукома, помутнение стекловидного тела, дисфункции зрачка).
Клиническая картина других типов амилоидоза варьируется в зависимости от основной локализации и распространенности амилоидных депозитов, которые иногда могут быть значительными и напоминать проявления AL-амилоидоза.
Рекомендации:
- Наиболее типичное проявление амилоидоза почек – изолированная протеинурия более 0,5 г/сут, чаще
нефротического уровня. Иногда при множественной миеломе важное значение приобретает иммунохимическое
электрофоретическое исследование мочи для отличия альбуминурии в рамках амилоидоза и протеинурии
переполнения (наличие в моче белка БенсДжонса, реакция термопреципитации белка Бенс-Джонса не обладает
достаточной информативностью).
 Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56]. - На амилоидоз сердца указывает утолщение межжелудочковой перегородки и/или задней стенки левого желудочка более 12 мм при эхокардиографии, особенно в сочетании с низкоамплитудной ЭКГ. Дифференциальный диагноз проводят с гипертрофией левого желудочка, которая может быть следствием артериальной гипертонии, аортальных пороков, гипертрофической кардиомиопатии и других причин [29,37-39,42,48,51-53,57-62].
- Характерное проявление амилоидоза сердца – низкая амплитуда желудочковых комплексов на ЭКГ (менее 5 мм в
отведениях от конечностей). Пато логические Q-зубцы у больных амилоидозом нередко являются псевдоинфарктными
(вследствие электрически нейтральных отложений амилоида, имитирующих рубцовые изменения), однако при
амилоидозе коронарных артерий возможно развитие и истинного инфаркта миокарда [29,37-39,42,48,51-53,56-62].

- При амилоидозе сердца наблюдается рестриктивное нарушение диастолической функции левого желудочка, фракция выброса часто остается нормальной, или степень ее снижения не соответствует тяжести сердечной недостаточности [29,37-39,42,48,51-53,5662].
- Всем больным с амилоидозом сердца необходимо проведение стандартной эхокардиографии с допплерометрической оценкой трансмитрального крово тока, при наличии технической возможности оправдано также проведение тканевой допплерометрии миокарда для более точной оценки внутрисердечной гемодинамики. В стандарт обследования больных амилоидозом сердца входят также ЭКГ и суточное мониторирование АД и ЭКГ [1,2,29,37-39,42,48,5153,56-62].
- Магнитно-резонансная томография (МРТ) с контрастированием гадолинием с высокой вероятностью выявляет
инфильтративный характер поражения миокарда и имеет особое диагностическое значение при “изолированном»
поражении сердца [48,56,6062].

- Амилоидную инфильтрацию сердца позволяет выявить также сцинтиграфия миокарда с пирофосфатом технеция, особенно при наличии трудностей в морфологической диагностике ATTR-амилоидоза, для которого характерна слабая конгофилия пораженных тканей. Интенсивное накопление радиоактивного препарата в миокарде (2+/3+) в сочетании с утолщением миокарда неясной этиологии указывает на высоко вероятный ATTR-амилоидоз, если у пациента исключен диагноз AL-амилоидоза (рис. 1) [39,42,58-59,62].
- Диагноз амилоидоза сердца может быть подтвержден при биопсии миокарда. Однако проведение этого исследования обычно не требуется при наличии типичных эхокардиографических изменений у пациентов с амилоидозом, установленным при биопсии другого органа, например, почки или слизистой оболочки прямой или двенадцатиперстной кишки.
- Диагностика периферической амилоидной полиневропатии основывается на клинической оценке неврологических
проявлений: обычно выявляют различные нарушения чувствительности, в частности температурной и болевой.
 Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
- Электромиография наряду с другими нейрофизиологическими методами (количественное сенсорное тестирование,
конфокальная микроскопия нервов роговицы, оценка состояния интраэпидермальных нервных волокон в биоптате
кожи) может использоваться для оценки характера (признаки аксонального и/или аксонально-демиелинизирующего
типа поражения двигательных и чувствительных волокон нервов конечностей) и тяжести неврологических
нарушений. Электромиография в сочетании с ультразвуковым исследованием периферических нервов позволяет
объективизировать их повреждение в анатомически узких каналах (туннельные невропатии) [38,39].

- Признаками I стадии амилоидной полиневропатии являются незначительные нарушения чувствительности по полиневропатическому типу, более выраженные в ногах, пациент сохраняет способность к самостоятельной ходьбе. При II стадии полиневропатии из-за нарастания чувствительных и присоединения двигательных нарушений в виде нижнего периферического преимущественно дистального парапареза походка пациента нарушается, требуется опора на трость или костыли. На III стадии тяжелые двигательные нарушения приковывают пациента к постели, передвижение возможно только на инвалидной коляске [38,39,46].
- Поражение вегетативной нервной системы чаще всего проявляется ортостатической гипотензией разной степени
тяжести. Однако систолическое артериальное давление менее 90 мм рт. ст. может быть обусловлено низким
сердечным выбросом у больных с сердечной недостаточностью или гиповолемией при тяжелом нефротическом
синдроме.
 Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].
Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39]. - Двусторонний синдром запястного канала наиболее характерен для ATTR-, β2М- и AL-амилоидоза и проявляется интенсивными болями и парестезиями в IIII пальцах кистей с постепенной атрофией мышц тенара [38,39].
- МРТ головного мозга с контрастным усилением проводят при наличии клинических признаков поражения центральной нервной системы [38,39].
- Основным признаком амилоидоза печени является ее увеличение, наиболее специфична гепатомегалия более 15 см
по данным компьютерной томографии. У больных амилоидозом печени обычно выявляют также холестаз (повышение
активности щелочной фосфатазы и/или g-глютамилтранспептидазы в 1,5 раза по сравнению с верхней границей
нормы).
 Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51].
Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51]. - Для выявления амилоидоза печени, селезенки и почек всем пациентам проводят ультразвуковое исследование этих органов, в некоторых случаях необходимо проведение компьютерной томографии брюшной полости [2,48].
- Диарея вследствие инфильтрации амилоидом стенки желудочно-кишечного тракта возникает редко, такую диарею трудно дифференцировать от моторной диареи в рамках поражения вегетативной нервной системы. Наиболее надежно вовлечение желудочнокишечного тракта при амилоидозе устанавливают по результатам морфологического исследования. Одна ко обнаружение амилоида только в стенках сосудов желудочно-кишечного тракте не является критерием его поражения, необходимо обнаружение амилоидных депозитов в интерстиции подслизистого слоя кишечника [1-2,5,48,52].
- Нодулярный легочный и трахеобронхиальный амилоидоз за редким исключением – это проявление локального
AL-амилоидоза.
 Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48]. - На амилоидоз плевры указывает рецидивирующий плевральный выпот, который не зависит от эффективности лечения
отечного синдрома, обусловленного сердечной недостаточностью или нефротическим синдромом. При амилоидном
поражении плевры жидкость, полученная во время пункции плевральной полости, нередко содержит примесь крови.
При амилоидозе плевры эвакуация плеврального выпота, как правило, малоэффективна из-за быстрого его
накопления [1,2,48].

- Поражение мягких тканей характерно для AL-амилоидоза. Макроглоссия с инфильтрацией дна ротовой полости и периорбитальная пурпура (и кожные геморрагии на теле) патогномоничны для этого типа амилоидоза. Возможны также псевдогипертрофия скелетных мышц с развитием мышечной слабости, лимфаденопатия, амилоидоз височной артерии [1,2,39,48,52].
- Признаками прогрессирования амилоидоза сердца являются дальнейшее утолщение миокарда (на 2 мм и более),
увеличение функционального класса сердечной недостаточности, снижение фракции выброса левого желудочка на
10% и более. Показатели тяжести амилоидоза сердца – увеличение уровня NTproBNP (особенно более 1800 нг/л) и
тропонинов (тропонин Т более 0,025 нг/мл). Критериями прогрессирования амилоидоза почек считают увеличение
протеинурии (на 50% от исходного уровня, как правило на 1 г/сут и более) и сывороточного уровня креатинина
(на 25% и более от исходного). Информативным критерием прогрессирования амилоидоза печени является
увеличение активности щелочной фосфатазы на 50% от исходной.
 Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Лечение системного амилоидоза
Целью терапии любого типа амилоидоза служит уменьшение количества (или, если возможно, удаление)
белков-предшественников для того, чтобы замедлить или приостановить прогрессирование болезни. Неблаго приятный
прогноз при естественном течении амилоидоза оправдывает применение агрессивных методов лечения. Клиническое
улучшение, достигаемое с помощью лечения, включает стабилизацию или восстановление функции жизненно важных
органов, а также предотвращение функциональных нарушений с увеличением продолжительности жизни больных. Лечение
амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной
недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение
амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной
недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение АА-амилоидоза
Цель терапии АА-амилоидоза – подавление продукции белка-предшественника SAA (вплоть до устойчивой нормализации), что достигается активным лечением хронического воспаления (в том числе субклинического). Это позволяет уменьшить клинические проявления и предотвратить прогрессирование амилоидной нефропатии и существенно улучшить прогноз.
Рекомендации:
- Основной стратегией лечения АА-амилоидоза является эффективное подавление воспаления. Лечение должно
проводиться вне зависимости от клинической активности воспалительного заболевания до нормализации уровня
маркеров острой фазы воспаления – С-реактивного белка (предпочтительно применение высокочувствительного
метода измерения) и/или SAA [10-13,63,66-77].

- Больным ревматоидным артритом и серонегативными спондилоартропатиями необходима постоянная пожизненная базисная терапия. Предпочтение отдают генно-инженерным биологическим препаратам, в том числе ингибиторам фактора некроза опухоли-α, интерлейкина-6, ритуксимабу. После оценки эффективности и безопасности базисной терапии оправдано присоединение терапии колхицином в дозе 2 мг/сут [10-13,63,66-77].
- Препаратом выбора при периодической болезни и тяжелой рецидивирующей подагре является колхицин в дозе 2
мг/сут. Начальная доза препарата составляет 0,5 мг/сут, затем ее постепенно увеличивают до целевой под
контролем клинического анализа крови и сывороточного уровня креатинина. Для предупреждения осмотической
диареи, обусловленной колхицином, возможно временное назначение ферментных препаратов. Дозу колхицина
снижают до 1 мг/сут у больных с хронической болезнью почек 4-5 стадии [1,2,4,69]. При неэффективности
колхицина показано назначение ингибиторов интерлейкина-1, в частности канакинумаба.

- При криопиринопатиях, TRAPS препаратами выбора являются ингибиторы интерлейкина-1, к которым присоединяют колхицин [18,19,74-77].
- При хронических нагноениях важное значение имеет хирургическое лечение. В дальнейшем или одновременно проводят лечение димексидом (5-10 г/сут в разведении большим количеством соков – томатного, гранатового и др.). Препарат предпочтителен при легочных нагноениях [1-2,4,6,31].
Лечение АL-амилоидоза
При AL-амилоидозе, как и при множественной миеломе, целью лечения служит подавление пролиферации клона
плазматических клеток для уменьшения продукции легких цепей иммуноглобулинов. В отличие от множественной
миеломы, принципиальной задачей лечения AL-амилоидоза является по возможности полная элиминация патологического
клона. В связи с быстрым прогрессированием заболевания важное значение имеет применение быстродействующих схем
лечения на основе бортезомиба. По мере достижения ремиссии у некоторых больных применяют высокодозную
химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением
противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза
сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц
старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не
рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также
лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
По мере достижения ремиссии у некоторых больных применяют высокодозную
химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением
противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза
сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц
старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не
рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также
лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
Рекомендации:
- Основной стратегией лечения АL-амилоидоза является элиминация амилоидогенного клона плазматических клеток
костного мозга. После достижения гематологической ремиссии проводят противорецидивное лечение в течение не
менее 12 месяцев.
 В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79].
В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79]. - Полный гематологический ответ диагностируют на основании исчезновения моноклональных амилоидогенных иммуноглобулинов по данным иммунофиксации крови и суточной мочи, количественного определения свободных легких цепей иммуноглобулинов методом Freelite (нормальный уровень легких цепей κ – менее 19,4 мг/л, λ – менее 26,3 мг/л, нормальное соотношение легких цепей в пределах 0,261,65). При снижении уровня свободных легких цепей на 50% от исходного диагностируют частичный ответ, критерием очень хорошего частичного ответа является разница между содержанием двух типов легких цепей иммуноглобулинов менее 40 мг/л [37,60,61,64].
- Клинический эффект терапии в первую очередь оценивают по динамике кардиологических и ренальных показателей.
 Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
- Учитывая возможность достижения быстрого гематологического ответа, терапией первой линии, особенно у больных
с высоким риском быстрого прогрессирования, считают комбинированные схемы на основе бортезомиба, например,
трехкомпонентная схема: бортезомиб 1,3 мг/м2 внутривенно или подкожно (1, 5, 8 и 11-й дни цикла), мелфалан
0,15 мг/кг внутрь (с 1-го по 4-й день) и дексаметазон 20 мг/сут внутрь (1, 5, 8 и 11-й дни). Для большей
безопасности предпочтительно подкожное введение бортезомиба. Если в дальнейшем планируется высокодозная
химиотерапия с поддержкой аутологичными стволовыми клетками мелфалан в составе трехкомпонентной схемы
заменяют на циклофосфамид (400 мг внутривенно капельно в 1, 8, 12-й дни), который не вызывает истощение пула
стволовых клеток в костном мозге. Курсы химиотерапии на основе бортезомиба проводят каждые 4 недели (всего 8
курсов). Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при
применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты,
ацикловир [65,78,79].

- Не менее эффективна схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й день) и дексаметазоном (внутрь 20 мг/сут в дни 1-4, 9-12 и 17-21) каждые 4-6 недель. Основным недостатком этой схемы является медленное формирование гематологического ответа, что делает ее менее перспективной у больных с высоким риском быстрого прогрессирования амилоидоза. Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты, ацикловир [1,2,37,56,57,65,78,79].
- У тяжелых больных с декомпенсированной сердечной недостаточностью может применяться схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й дни) и преднизолоном (0,8 мг/кг с 1-го по 7-й день). Однако эффективность этой схемы ограничена [1,2,56,57,65,78,79].
Лечение ATTR-амилоидоза
До недавнего времени единственным методом лечения ATTR-амилоидоза была трансплантация печени, секретирующей
нормальный транстиретин. Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло
прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование
ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже
имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе
нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями
ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного
транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял
на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию
периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение
тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и
частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81].
Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло
прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование
ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже
имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе
нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями
ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного
транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял
на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию
периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение
тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и
частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81].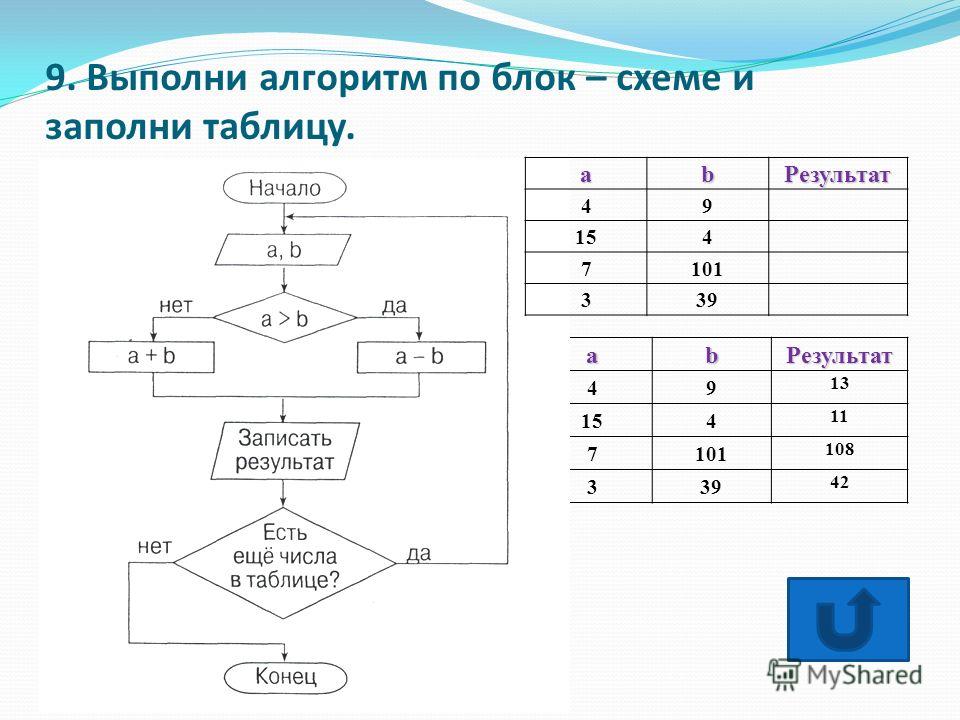 В
Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической
полиневропатией.
В
Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической
полиневропатией.
В качестве стабилизатора транстиретина изучается также дифлюнизал из группы нестероидных противовоспалительных препаратов, однако его эффективность показана только в экспериментальных условиях.
Рекомендации:
- Трансплантация печени остается одним из методов лечения ATTR-амилоидоза. Наилучших показателей выживаемости удается достичь у больных моложе 50 лет с небольшой длительностью заболевания, нормальным индексом массы тела и мутацией Val30Met. Эффективность трансплантации печени существенно ниже у больных с III стадией полиневропатии, ортостатической гипотензией, хронической сердечной недостаточностью, удлинением комплекса QRS бо лее 120 мс и утолщением межжелудочковой перегородки [2,38-40,43-46].
- Больным ATTR-амилоидозом с периферической невропатией рекомендуется пожизненный прием тафамидиса в дозе 20
мг/сут внутрь, который обладает хорошим профилем безопасности [38-40,43-46,80].

Заместительная почечная терапия
Рекомендации:
- Поскольку ХПН служит одной из основных причин смерти больных системным амилоидозом, проведение гемодиализа
или постоянного амбулаторного перитонеального диализа позволяет улучшить прогноз этих пациентов.
Выживаемость больных амилоидозом при проведении гемодиализа, независимо от его типа, сопоставима с
выживаемостью больных другими системными заболеваниями и сахарным диабетом. При этом хорошую и
удовлетворительную реабилитацию отмечают у 60% пациентов с АА- и AL-типами амилоидоза. Основной причиной
смерти больных амилоидозом при проведении гемодиализа являются сердечно-сосудистые осложнения. Амбула торный
перитонеальный диализ имеет некоторые преимущества перед гемодиализом, учитывая отсутствие необходимости в
постоянном сосудистом доступе и меньший риск артериальной гипотензии во время процедуры диализа. У больных
AL-амилоидозом во время процедуры возможно удаление легких цепей иммуноглобулинов [1-4,6,28,48].

- Трансплантация почки эффективна при системном амилоидозе: 5-летняя выживаемость больных и трансплантата составляет 65% и 62%, соответственно, и сопоставима с таковыми в других группах больных с ХПН. Трансплантация почки показана больным с медленным прогрессированием амилоидоза без поражения сердца и желудочно-кишечного тракта. Амилоидоз в трансплантированной почке возникает, по разным данным, примерно у 30% больных, однако он служит причиной потери трансплантата всего у 2-3% пациентов [1-4,6,28,48].
Симптоматическая терапия
Рекомендации:
- Больным амилоидозом противопоказаны сердечные гликозиды и недигидропиридиновые антагонисты кальция
(верапамил, дилтиазем), которые могут накапливаться в амилоиде, в то время как β-адреноблокаторы и
ингибиторы АПФ следует применять осторожно. Основа лечения застойной сердечной недостаточности при
амилоидозе сердца – петлевые диуретики, хотя ортостатическая гипотензия может ограничивать применение этих
препаратов, как и β-адреноблокаторов и ингибиторов АПФ [1,2,31,45,49,52,58].

- При наличии желудочковых тахиаритмий, сопровождавющихся высоким риском внезапной сердечной смерти, показана установка искусственного кардиовертера-дефибриллятора, а при синдроме слабости синусового узла и атрио-вентрикулярной блокаде – имплантация искусственного водителя ритма [2,38,39,45,52,53,58].
- Для лечения ортостатической гипотензии могут быть использованы минералокортикостероиды или глюкокортикостероиды, хотя их применение может привести к декомпенсации сердечной недостаточности. Возможно назначение α-адреномиметика мидодрина (Гутрон), однако его применение требует осторожности [1,2,39,42,45,52,58].
- Для контроля кишечной моторики высокую эффективность показали пролонгированные препараты соматостатина (октреотид-лонг 20 мг один раз в месяц) [1,2,38,39,49].
- При деструкции стекловидного тела у больных ATTR-амилоидозом может потребоваться витрэктомия. При наличии
неконтролируемой глаукомы проводят трабекулэктомию [39].

- Для купирования невропатической боли у пациентов с амилоидной невропатией рекомендовано использование адъювантных анальгетиков (антиконвульсанты и антидепрессанты) [39].
Используемые источники
- Козловская Л.В., Рамеев В.В., Саркисова И.А. Амилоидоз у пожилых.Клиническая медицина 2005;6:12-20. [Kozlovskaya LV, Rameev VV, SarkisovaIA. Amyloidosis in the elderlies. Klinicheskaya medicina 2005;6:12-20 (In Russ.)].
- Рамеев В.В., Козловская Л.В., Саркисова И.А. Лечение амилоидоза. Врач2007;6:38-41 [Rameev VV, Kozlovskaya LV, Sarkisova IA. Treatment of amyloi-dosis. Vrach 2007;6:38-41 (In Russ.)].
- Sipe JD, Benson MD, Buxbaum JN, et al. Amyloid fibril proteins and amyloido-sis: chemical identification and clinical classification International Society ofAmyloidosis 2016 Nomenclature Guidelines. Amyloid 2016;23(4):209-13.
- Рамеев В.В., Козловская Л.
 В., Рамеева А.С., Тао П.П. Оптимизация страте-гии ведения больных вторичным АА-амилоидозом. Врач 2019;30(5):3-11[Rameev VV, Kozlovskaya LV, Rameeva AS, Tao PP. Optimization of the man-agement strategy for patients with secondary AA-amyloidosis. Vrach 2019;30(5):3-11 (In Russ.)].
В., Рамеева А.С., Тао П.П. Оптимизация страте-гии ведения больных вторичным АА-амилоидозом. Врач 2019;30(5):3-11[Rameev VV, Kozlovskaya LV, Rameeva AS, Tao PP. Optimization of the man-agement strategy for patients with secondary AA-amyloidosis. Vrach 2019;30(5):3-11 (In Russ.)]. - Gertz MA, Kyle RA. Secondary systemic amyloidosis: response and survival in 64patients. Medicine (Baltimore) 1991;70(4):246-56.
- Lachmann HJ, Goodman HJB, Gilbertson JA, et al. Natural history and outcomein systemic AA amyloidosis. N Engl J Med 2007;356(23):2361–71.
- Kravitz MS, Pitashny M, Shoenfeld Y. Protective molecules – C-reactive protein(CRP), serum amyloid P (SAP), pentraxin3 (PTX3), mannose-binding lectin(MBL), and apolipoprotein A1 (Apo A1), and their autoantibodies: prevalenceand clinical significance in autoimmunity. J Clin Immunol 2005;25(6):582–91.
- Szalai AJ. C-reactive protein (CRP) and autoimmune disease: facts and conjec-tures. Clin Dev Immunol 2004;11(3-4):221–6.

- Volanakis JE. Human C-reactive protein: expression, structure, and function. MolImmunol 2001;38(2-3):189–97.
- Korkmaz C, Ozdogan H, Kasapçopur O, Yazici H. Acute phase response in famil-ial Mediterranean fever. Ann Rheum Dis 2002;61(1):79–81.
- Duzova A, Bakkaloglu A, Besbas N, et al. Role of A-SAA in monitoring subclin-ical inflammation and in colchicine dosage in familial Mediterranean fever. ClinExp Rheumatol 2003;21(4):509–14.
- Lachmann HJ, Sengül B, Yavuzşen TU, et al. Clinical and subclinical inflamma-tion in patients with familial Mediterranean fever and in heterozygous carriers ofMEFV mutations. Rheumatology (Oxford) 2006;45(6):746–50.
- Wittkowski H, Frosch M, Wulffraat N, et al. S100A12 is a novel molecular mark-er differentiating systemic-onset juvenile idiopathic arthritis from other causes offever of unknown origin. Arthritis Rheum 2008;58(12):3924–31.
- Foell D, Wittkowski H, Hammerschmidt I, et al.
 Monitoring neutrophil activationin juvenile rheumatoid arthritis by S100A12 serum concentrations. ArthritisRheum 2004;50(4):1286–95.
Monitoring neutrophil activationin juvenile rheumatoid arthritis by S100A12 serum concentrations. ArthritisRheum 2004;50(4):1286–95. - Kallinich T, Wittkowski H, Keitzer R, et al. Neutrophil-derived S100A12 as novelbiomarker of inflammation in familial Mediterranean fever. Ann Rheum Dis2010;69(4):677–82.
- Benson MD, Liepnieks JJ, Yazaki M, et al. A new human hereditary amyloidosis:the result of a stop-codon mutation in the apolipoprotein AII gene. Genomics2001;72:272–7.
- Almeida de Jesus A, Goldbach-Mansky R. Monogenic autoinflammatory diseases:concept and clinical manifestations. Clin Immunol Orlando Fla 2013;147(3):155–74.
- Aksentijevich I, Nowak M, Mallah M, et al. De novo CIAS1 mutations, cytokineactivation, and evidence for genetic heterogeneity in patients with neonatal-onsetmultisystem inflammatory disease (NOMID): a new member of the expandingfamily of pyrin-associated autoinflammatory diseases. Arthritis Rheum 2002;46(12):3340–8.

- Goldbach-Mansky R, Dailey NJ, Canna SW, et al. Neonatal-onset multisysteminflammatory disease responsive to interleukin-1beta inhibition. N Engl J Med2006;355(6):581–92.
- Touitou I, Lesage S, McDermott M, et al. Infevers: an evolving mutation databasefor auto-inflammatory syndromes. Hum Mutat 2004;24(3):194–8.
- Houten SM, Kuis W, Duran M, et al. Mutations in MVK, encoding mevalonatekinase, cause hyperimmunoglobulinaemia D and periodic fever syndrome. NatGenet 1999;22(2):175–7.
- Haas D, Hoffmann GF. Mevalonate kinase deficiencies: from mevalonic aciduriato hyperimmunoglobulinemia D syndrome. Orphanet J Rare Dis 2006;1:13.
- Ruiz Gomez A, Couce ML, Garcia-Villoria J, et al. Clinical, genetic, and thera-peutic diversity in 2 patients with severe mevalonate kinase deficiency. Pediatrics2012;129(2):535-9.
- Bader-Meunier B, Florkin B, Sibilia J, et al. Mevalonate kinase deficiency: a sur-vey of 50 patients. Pediatrics 2011;128(1):152-9.

- Gershoni-Baruch R, Brik R, Zacks N, et al. The contribution of genotypes at theMEFV and SAA1 loci to amyloidosis and disease severity in patients with familialMediterranean fever. Arthritis Rheum 2003;48(4):1149–55.
- Мрыхин Н.Н., Лысенко Л.В., Чеботарева Н.В. и др. Частота выявления иварианты моноклональной гаммапатии у больных многопрофильного тера-певтического стационара. Врач 2019;30(2):54-60 [Mrykhin NN, Lysenko LV,Chebotareva NV, et al. Frequency of detection and variants of monoclonalgammapathy in patients of a multidisciplinary therapeutic hospital. Vrach3019;30(2):54-60 (In Russ.)].
- Тао П.П., Рамеев В.В., Рамеева А.С. и др. Проблемы диагностики и лечениялокального AL-амилоидоза. Клин фармакол тер 2019;28(3):26-33 [Tao PP,Rameev VV, Rameeva AS, et al. Problems of diagnosis and treatment of local AL-amyloidosis. Klinicheskaya farmakologiya i terapiya = Clin Pharmacol Ther 2019;29(3):26-33. (In Russ.)].
- Gillmore JD, Hawkins PN, Pepys MB.
 Amyloidosis: a review of recent diagnosticand therapeutic developments. Br J Haematol 1997;99:245-56.
Amyloidosis: a review of recent diagnosticand therapeutic developments. Br J Haematol 1997;99:245-56. - Leung N, Glavey SV, Kumar S, et al. A detailed evaluation of the current renalresponse criteria in AL amyloidosis: is it time for a revision? Haematologica2013;98(6):988-92
- Bradwell AR. Serum free light chain analysis. 4th edition The Binding Site Ltd.2006;285 p.
- Kyle RA. Amyloidosis: a convoluted story. Br J Haematol 2001;114:529–38.
- Kyle RA. Monoclonal gammopathy of undetermined significance: natural historyin 241 cases. Am J Med 1978;64:814-26.
- Gertz MA, Rajkumar SV. Multiple Myeloma. Diagnosis and Treatment. NewYork:Springer 2014;311 p.
- Fonseca R, Bergsagel PL, Drach J, et al. International Myeloma Working Groupmolecular classification of multiple myeloma: spotlight review. Leukemia 2009;23(12):2210–21.
- Owen-Casey MP, Sim R, Cook HT, et al. Value of antibodies to free light chainsin immunoperoxidase studies of renal biopsies.
 J Clin Pathol 2014;67:661–6.
J Clin Pathol 2014;67:661–6. - Lachmann HJ, Booth DR, Booth SE, et al. Misdiagnosis of hereditary amyloido-sis as AL (primary) amyloidosis. N Engl J Med 2002;346:1786-91.
- Muchtar E, Buadi F, Dispenzieri A, Gertz M. Immunoglobulin light-chain amy-loidosis: from basics to new developments in diagnosis, prognosis and therapy.Acta Haematol 2016;135:172-90.
- Рамеев В.В., Мясников Р.П., Виноградов П.П. и др. Системный ATTR-ами-лоидоз, редкая форма поражения внутренних органов. Рациональная фар-макотерапия в кардиологии 2019;15(3):349-58. [Rameev VV, Myasnikov RP,Vinogradov PP, et al. Systemic ATTR-amyloidosis, a rare form of internal organdamage. Rational pharmacotherapy in cardiology 2019;15(3):349-58 (In Russ.)].
- Adams D, Suhr O, Hund E, et al. First European consensus for diagnosis,manegement, and treatment of transthyretin familial amyloid polyneuropathy/ Curr Opin Neurol 2016;29(suppl 1):14-26.
- Гудкова А.
 Я., Полякова А.А., Амелин А.В. и др. Не VAL30MET-транстире-тиновая амилоидная кардиомиопатия. Обзор сведений литературы и кли-ническое наблюдение. Российский кардиологический журнал 2018;2(154):121-128 [Gudkova AJ, Polyakova AA, et al. Non-Val30Met-trans thyretin amyloidcardiomyopathy. Review of literature, data and clinical case. Rossijskij kardio-logicheskij zhurnal 2018;2(154):121-8 (In Russ.)].
Я., Полякова А.А., Амелин А.В. и др. Не VAL30MET-транстире-тиновая амилоидная кардиомиопатия. Обзор сведений литературы и кли-ническое наблюдение. Российский кардиологический журнал 2018;2(154):121-128 [Gudkova AJ, Polyakova AA, et al. Non-Val30Met-trans thyretin amyloidcardiomyopathy. Review of literature, data and clinical case. Rossijskij kardio-logicheskij zhurnal 2018;2(154):121-8 (In Russ.)]. - Hemminki K, Li X, Försti A, et al. Incidence of hereditary amyloidosis andautoinflammatory diseases in Sweden: endemic and imported diseases. BMC MedGenet 2013;14:88.
- González-López E, Gallego-Delgado M, Guzzo-Merello G, et al. Wild-typetransthyretin amyloidosis as a cause of heart failure with preserved ejection frac-tion. Eur Heart J 2015;36:2585–94.
- Adams D, Théaudin M, Cauquil C, et al. FAP neuropathy and emerging treat-ments. Curr Neurol Neurosci Rep 2014;14(3):435.
- Sekijima Y. Transthyretin (ATTR) amyloidosis: clinical spectrum, molecularpathogenesis and disease-modifying treatments.
 J Neurol Neurosurg Psychiatry2015;86(9):1036-43.
J Neurol Neurosurg Psychiatry2015;86(9):1036-43. - Ando Y, Coelho T, Berk JL, et al. Guideline of transthyretin-related hereditaryamyloidosis for clinicians. Orphanet J Rare Dis 2013;20(8):31.
- Adams D, Cauquil C, Theaudin M, et al. Current and future treatment of amyloidneuropathies. Expert Rev Neurother 2014;14(12):1437-51.
- Koike H, Tanaka F, Hashimoto R, et al. Natural history of transthyretinVal30Met familial amyloid polyneuropathy: analysis of late-onset cases from non-endemic areas. J Neurol Neurosurg Psychiatry 2012;83(2):152-8.
- Gertz MA, Comenzo R, Falk RH, et al. Definition of organ involvement andtreatment response in immunoglobulin light chain amyloidosis (AL): a consensusopinion from the 10th International Symposium on Amyloid and Amyloidosis,Tours, France, 18-22 April 2004. Am J Hematol 2005;79(4):319-28.
- Hans LA, Nienhuis JB, Hazenberg BPC. The prevalence and management of sys-temic amyloidosis in western countries.
 Kidney Dis 2016;2:10-9.
Kidney Dis 2016;2:10-9. - Benson MD, Liepnieks J, Uemichi T, et al. Hereditary renal amyloidosis associ-ated with a mutant fibrinogen alpha-chain. Nature Gen 1993;3:252–6.
- Rameeva A, Vedanova K, Rameev V, et al. The critical role of chronic kidney dis-ease in the progression of AL-amyloid cardiopathy. Amyloid 2019;26(S1):109-10
- Kyle RA, Gertz MA. Primary systemic amyloidosis: clinical and laboratory fea-tures in 474 cases. Semin Hematol 1995;32(1):45-59.
- Kyle RA, Linos A, Beard CM, et al. Incidence and natural history of primary sys-temic amyloidosis in Olmsted County, Minnesota, 1950 through 1989. Blood1992;79:1817–22.
- Pinney JH, Smith CJ, Taube JB, et al. Systemic amyloidosis in England: an epi-demiological study. Br J Haematol 2013;161:525–32.
- Mor A, Shinar Y, Zaks N, et al. Evaluation of disease severity in familialMediterranean fever. Semin Arthritis Rheum 2005;35(1):57–64.
- Rezk T, Lachmann HJ, Fontana M, et al.
 Prolonged renal survival in light chainamyloidosis: speed and magnitude of light chain reduction is the crucial factor.Kidney Int 2017;92(6):1476-83.
Prolonged renal survival in light chainamyloidosis: speed and magnitude of light chain reduction is the crucial factor.Kidney Int 2017;92(6):1476-83. - Рамеев В.В., Козловская Л.В., Рамеева А.С. и др. Особенности эволюции ипрогностическое значение поражения сердца у больных системным AL-амилоидозом. Клин фармакол тер 2019;29(2):49-57 [Rameev VV, KozlovskayaLV, Rameeva AS, et al. Evolution and prognostic value of heart disease in patientswith systemic AL-amyloidosis. Klinicheskaya farmakologiya i terapiya = ClinPharmacol Ther 2019;29(3):26-33 (In Russ.)].
- Cacoub P, Axler O, De Zuttere D, et al. Amyloidosis and cardiac involvement.Ann Med Interne (Paris) 2000;151: 611-617.
- Dubrey SW, Hawkins PN, Falk RH. Amyloid diseases of the heart: assessment,diagnosis, and referral. Heart 2011;97(1):75-84.
- Palladini G, Dispenzieri A, Gertz MA, et al. New criteria for response to treat-ment in immunoglobulin light chain amyloidosis based on free light chain mea-surement and cardiac biomarkers: impact on survival outcomes.
 J Clin Oncol2012;30:4541–9.
J Clin Oncol2012;30:4541–9. - Kumar S, Dispenzieri A, Lacy MQ, et al. Revised prognostic staging system forlight chain amyloidosis incorporating cardiac biomarkers and serum free lightchain measurements. J Clin Oncol 2012;30:989–95.
- Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy diagnosis of cardiactransthyretin amyloidosis. Circulation 2016;133(24):2404-12.
- Merlini G, Bellotti V. Molecular mechanisms of amyloidosis. N Engl J Med 2003;349:583-96.
- Gertz MA, Kyle RA, Greipp PR. Response rates and survival in primary systemicamyloidosis. Blood 1991;77:257-62.
- Merlini G. CyBorD: stellar response rates in AL amyloidosis. Blood 2012;119:4343-5.
- Benditt EP, Eriksen N. Amyloid protein SAA is associated with high densitylipoprotein from human serum. Proc Natl Acad Sci USA 1977;74:4025–8.
- Cantarini L, Rigante D, Brizi MG, et al. Clinical and biochemical landmarks insystemic autoinflammatory diseases.
 Ann Med 2012;44(7):664–73.
Ann Med 2012;44(7):664–73. - Hawkins PN, Lachmann HJ, Aganna E, McDermott MF. Spectrum of clinicalfeatures in Muckle-Wells syndrome and response to anakinra. Arthritis Rheum2004;50(2):607–12.
- Goldfinger SE. Colchicine for familial Mediterranean fever. N Engl J Med 1972;287(25):1302.
- Gattorno M, Sormani MP, D’Osualdo A, et al. A diagnostic score for molecularanalysis of hereditary autoinflammatory syndromes with periodic fever in children.Arthritis Rheum 2008;58(6):1823–32.
- Martinon F, Pétrilli V, Mayor A, et al. Gout-associated uric acid crystals activatethe NALP3 inflammasome. Nature 2006;440(7081):237–41.
- So A, De Smedt T, Revaz S, Tschopp J.A pilot study of IL-1 inhibition byanakinra in acute gout. Arthritis Res Ther 2007;9(2):R28.
- McGonagle D, Tan AL, Shankaranarayana S, et al. Management of treatmentresistant inflammation of acute on chronic tophaceous gout with anakinra. AnnRheum Dis 2007;66(12):1683–1684.

- Burger D, Dayer JM, Palmer G, Gabay C. Is IL-1 a good therapeutic target in thetreatment of arthritis? Best Pract Res Clin Rheumatol 2006;20(5):879–96.
- Tunca M, Kirkali G, Soytürk M, et al. Acute phase response and evolution offamilial Mediterranean fever. Lancet 1999;353(9162):1415.
- Mansfield E, Chae JJ, Komarow HD, et al. The familial Mediterranean fever pro-tein, pyrin, associates with microtubules and colocalizes with actin filaments.Blood 2001;98(3):851–59.
- Kuemmerle-Deschner JB, Tyrrell PN, Koetter I, et al. Efficacy and safety ofanakinra therapy in pediatric and adult patients with the autoinflammatoryMuckle-Wells syndrome. Arthritis Rheum 2011;63(3):840–9.
- Comenzo RL, Vosburgh E, Simms RW, et al. Dose-intensive melphalan withblood stem cell support for the treatment of AL amyloidosis: one-year follow-upin five patients. Blood 1996;88:2801-6.
- Dispenzieri A, Kyle RA, Lacy MQ, et al.
 Superior survival in primary systemicamyloidosis patients undergoing peripheral blood stem cell transplantation: a case-control study. Blood 2004;103(10):3960-3.
Superior survival in primary systemicamyloidosis patients undergoing peripheral blood stem cell transplantation: a case-control study. Blood 2004;103(10):3960-3. - Gundapanenia BK, Sultanb MB, Keohaneb DJ, Schwartz JH. Tafamidis delaysneurological progression comparably across Val30Met and non-Val30Met geno-types in transthyretin familial amyloid polyneuropathy. Eur J Neur 2018;25:464-8.
- Maurer MS, Schwartz JH, Gundapaneni B, et al. Tafamidis treatment for patientswith transthyretin amyloid cardiomyopathy. N Engl J Med 2018;379(11):1007-16.
Версия на английском языке
КЛИНИЧЕСКАЯ ГАСТРОЭНТЕРОЛОГИЯ
- ФГБУН «ФИЦ питания и биотехнологии» (Москва, Россия)
Ключевые слова: дыхательный тест с лактулозой, СИБР метаногенной флоры, СИБР водородпродуцирующей флоры, фактическое питание
Резюме:Цель: Оценить особенности рационов пациентов с различными вариантами СИБР для разработки диетологических методов профилактики рецидивов СИБР. Материалы и методы: У 889 пациентов, выполнивших водородно-метановый дыхательный тест с лактулозой, выполнен анализ по данным фактического питания полученных методом суточного воспроизведения. Результаты: Было установлено, что для лиц с СИБР метаногенной флоры характерно более высокое потребление фруктов (0,63 ± 0,7 относительно нормы потребления против 0,37 ± 0,41 в группе Н2, 0,39 ± 0,45, в группе Н2+СН4) и белковых блюд (1,61 ± 0,88 против 1,25 ± 0,91 в группе Н2+СН4, 1,37±0,84 в группе Н2), для лиц с СИБР водородпродуцирующей флорой характерно более высокое потребление жира (1,20 ± 0,35 против 1,14 ± 0,28 в группе нормы, 1,15 ± 0,31 в группе Н2+СН4), в отношении белковых блюд лица с выявленным СИБР отличались достоверно меньшим потреблением красного мяса (0,53 ± 0,66 у пациентов без СИБР против 0,31 ± 0,53 в группе Н2, против 0,37 ± 0,50 в группе СН4), при этом пациенты с СИБР метаногенной флоры употребляли больше рыбной продукции (0,49 ± 0,73 против 0,21 ± 0,41 в группе Н2, против 0,24 ± 0,77 в группе Н2+СН4), а для лиц с избытком водородпродуцирующей флоры характерно более высокое потребление мяса птицы (0,57 ± 0,64 против 0,37 ± 0,50 в группе СН4, против 0,45±0,52 в группе Н2+СН4, против 0,37±0,45 у пациентов без СИБР).
Материалы и методы: У 889 пациентов, выполнивших водородно-метановый дыхательный тест с лактулозой, выполнен анализ по данным фактического питания полученных методом суточного воспроизведения. Результаты: Было установлено, что для лиц с СИБР метаногенной флоры характерно более высокое потребление фруктов (0,63 ± 0,7 относительно нормы потребления против 0,37 ± 0,41 в группе Н2, 0,39 ± 0,45, в группе Н2+СН4) и белковых блюд (1,61 ± 0,88 против 1,25 ± 0,91 в группе Н2+СН4, 1,37±0,84 в группе Н2), для лиц с СИБР водородпродуцирующей флорой характерно более высокое потребление жира (1,20 ± 0,35 против 1,14 ± 0,28 в группе нормы, 1,15 ± 0,31 в группе Н2+СН4), в отношении белковых блюд лица с выявленным СИБР отличались достоверно меньшим потреблением красного мяса (0,53 ± 0,66 у пациентов без СИБР против 0,31 ± 0,53 в группе Н2, против 0,37 ± 0,50 в группе СН4), при этом пациенты с СИБР метаногенной флоры употребляли больше рыбной продукции (0,49 ± 0,73 против 0,21 ± 0,41 в группе Н2, против 0,24 ± 0,77 в группе Н2+СН4), а для лиц с избытком водородпродуцирующей флоры характерно более высокое потребление мяса птицы (0,57 ± 0,64 против 0,37 ± 0,50 в группе СН4, против 0,45±0,52 в группе Н2+СН4, против 0,37±0,45 у пациентов без СИБР). В подгруппе без признаков СИБР выявлено достоверно большее потребление пищевых волокон (21,4 г/сут±10,0 против 19,0±9,5 у группы СИБР Н2 и 19,1±8,9 у группы СИБР Н2/СН4). Заключение: Выявленные особенности питания пациентов с разными вариантами СИБР позволят разработать меры диетологической коррекции рационов пациентов способствующие профилактике рецидивов СИБР.
В подгруппе без признаков СИБР выявлено достоверно большее потребление пищевых волокон (21,4 г/сут±10,0 против 19,0±9,5 у группы СИБР Н2 и 19,1±8,9 у группы СИБР Н2/СН4). Заключение: Выявленные особенности питания пациентов с разными вариантами СИБР позволят разработать меры диетологической коррекции рационов пациентов способствующие профилактике рецидивов СИБР.
- Литература всего 37 ⇓ :: .
- Hawrelak J. A., Myers S. P. Th e Causes of Intestinal Dysbiosis: A Review // Altern Med Rev.-2004.-9(2).-180–197.
- Dominguez-Bello M. G., Blaster M. J. Do you have a probiotic in your future? // Microbes and Infection. – 2008. – 10. – 1072–1076.
- Macfarlane S, Macfarlane GT. Proteolysis and amino acid fermentation. In: Gibson GR, Macfarlane GT, eds. Human Colonic Bacteria: Role in Nutrition, Physiology, and Pathology. – Boca Raton, FL: CRC Press; 1995.-75–100
- Yao C. K., Muir J. G., Gibson P.
 R. Review article: insights into colonic protein fermentation, its modulation and potential health implications // Aliment Pharmacol Th er. – 2016.-43(2). – 1–16
R. Review article: insights into colonic protein fermentation, its modulation and potential health implications // Aliment Pharmacol Th er. – 2016.-43(2). – 1–16 - Ponziani F. R., Gerardi V., Gasbarrini A. Diagnosis and treatment of small intestinal overgrowth // Expert review of gastroenterology & hepatology. – 2016. – 10(2).-215–227.
- Rutherford S. T. and Bassler B. L. Bacterial Quorum Sensing: Its Role in Virulence and Possibilities for Its Control // Cold Spring Harb Perspect Med.-2012. – 2(11). – a012427
- Li Z., Nair S. K. Quorum sensing: How bacteria can coordinate activity and synchronize their response to external signals? // Protein Science. – 2012. – 21. – 1403–1417
- Spiegel B. M. R. Questioning the Bacterial Overgrowth Hypothesis of Irritable Bowel Syndrome: An Epidemiologic and Evolutionary Perspective // Clinical gastroenterology and hepatology. – 2011.-9. – 461–469.
- Gabrielli M., D’angelo G., Di Rienzo T.
 et al. Diagnosis of small intestinal bacterial overgrowth in the clinical practice // European Review for Medical and Pharmacological Sciences. – 2013.-17(Suppl 2). – 30–35.
et al. Diagnosis of small intestinal bacterial overgrowth in the clinical practice // European Review for Medical and Pharmacological Sciences. – 2013.-17(Suppl 2). – 30–35. - Giamarellos-Bourboulis E. J., Tzivras M. Small Intestinal Bacterial Overgrowth: Novel Insight in the Pathogenesis and Treatment of Irritable Bowel Syndrome // Annals Of Gastroenterology. – 2009. – 22 (2). – 77–81.
- Milani C., Ferrario C., Turroni et al. Тhe human gut microbiota and its interactive connections to diet. // J Hum Nutr Diet. – 2016. – 29. – 539–546.
- Wang J., Linnenbrink M., Künzel S. et al. Dietary history contributes to enterotype-like clustering and functional metagenomic content in the intestinal microbiome of wild mice. // Proceedings of the National Academy of Sciences. – 2014. – 111 (26). – E2703-E2710.
- Wu G. D., Chen J., Hoff mann C. et al. Linking Long-Term Dietary Patterns with Gut Microbial Enterotypes // Science. – 2011. – 334. – 105–108.

- Spiegel BMRN, Mayer E, Bolus R, et al. Development and initial validation of a concise point-of-care IBS severity index: the 4-item “BEST” questionnaire. // Gastroenterology. – 2006.-130.-S1040.
- Preparation and use of food-based dietary guidelines // Joint FAO/WHO Consultation (WHO Technical Report Series 880). – 1998. – 108р
- Пилипенко В. И., Исаков В. А., Зейгарник М. В. Метод оценки рационов питания сопоставлением пищевого паттерна // Вопросы диетологии 2016. – том 6, № 3. – 72–76
- Потребление продуктов питания в домашних хозяйствах в 2011 году (по итогам выборочного обследования бюджетов домашних хозяйств) – М.: Федеральная служба государственной статистики, 2012.
- Helman M. L., Greenway F. L. A healthy gastrointestinal microbiome is dependent on dietary diversity // Molecular metabolism. – 2016. – Vol 5. – 317–320.
- Jeff ery I. B., O’Toole P. W. Diet-microbiota interactions and their implications for healthy living // Nutrients.
 – 2013. – Vol 5. – 234–252.
– 2013. – Vol 5. – 234–252. - Jang H. B., Choi M. K., Kang J. H. et al. Association of dietary patterns with the fecal microbiota in Korean adolescents. // BMC Nutrition. – 2017. – 3.-20.
- Shefl in A. M., Melby C. L., Carbonero F. et al. Linking dietary patterns with gut microbial composition and function. // Gut Microbes. – 2017.-8(2).-113–129.
- Porter N. T., Martens E. C. Th e critical roles of polysaccharides in gut microbial ecology and physiology // Annu. Rev. Microbiol. – 2017. – Vol 71. – 349–369.
- Flint H. J., Duncan S. H., Louis P. Th e impact of nutrition on intestinal bacterial communities // Current opinion in Microbiology. – 2017. – 38. – 59–65.
- Pallister T., Spector T. D. Food a new form of personalized (gut microbiome) medicine for chronic diseases? //(9). – 331–336.
- Weiss G. A., Hennet T. Mechanisms and consequencts of intestinal dysbiosis. // Cell. Mol. Life Sci. – 2017. – 74(16).2959–2977.
- Singh R.
 K., Chang H. W., Yan D. et al. Infl uence of diet on the gut microbiome and implications for human health // J Transl Med. – 2017. – 15(1).-73.
K., Chang H. W., Yan D. et al. Infl uence of diet on the gut microbiome and implications for human health // J Transl Med. – 2017. – 15(1).-73. - Martinez K. B., Pierre J. F., Chang E. B. Th e gut microbiota Th e gateway to improved metabolism. // Gastroenterol Clin N Am. – 2016. – 45. – 601–614.
- Myles I. A. Fast food fever: reviewing the impacts of the Western diet on immunity // Nutrition Journal. – 2014. – 13.-61.
- Ohlad C. L., Jobin C. Microbial activities and intestinal homeostasis: a delicate balance between health and disease // Cell MolGastroenterolHepatol. – 2015.-1. – 28–40.
- Cani P. D., Everard A. Talking microbes: When gut bacteria interact with diet and host organs // Mol. Nutr. Food Res. – 2016. – 60. – 58–66.
- Brown K., DeCoff e D., Molcan E., Gibson D. L. Diet-Induced Dysbiosis of the Intestinal Microbiota and the Eff ects on Immunity and Disease // Nutrients. – 2012. – 4. – 1095–1119.
- Pokusaeva K, Fitzgerald GF & van Sinderen D.
 Carbohydrate metabolism in Bifi dobacteria. // Genes Nutr. – 2011. – 6. – 285–306.
Carbohydrate metabolism in Bifi dobacteria. // Genes Nutr. – 2011. – 6. – 285–306. - Rosa D., Dias M. M. S., et al. Milk kefi r: nutritional, microbiological and health benefi ts // Nutrition Research Review. – 2017. – 30(1). – 82–96.
- Gomg L., Cao W., Chi H. et al. Whole cereal grains and potential health eff ects: involvement of the gut microbiota. // Food research international. – 2018. – 103. – 84–102.
- Lekshmi M., Ammini P., Kumar S. et al. Th e food production environment and the development of antimicrobial resisance in human pathogens of animal origin. // Microorganisms. – 2017. – 5. – 11 doi: 10/3390/microorganisms5010011
- Гофман В. Р. Экологические и социальные аспекты безопасности продовольственного сырья и продуктов питания: Учебное пособие. – Челябинск: Изд. ЮУрГУ, 2004. – 551 с.
- Kadokar S., Mutlu E. A. Diet as a therapeutic option for adult infl ammatory bowel disease. // Gasroenterol Clin N Am. – 2017. – 46.
 – p. 745–767.
– p. 745–767.
Для цитирования :
Пилипенко В. И., Балмашнова А. В. Особенности рационов больных с различными вариантами синдрома избыточного бактериального роста в тонкой кишке. Экспериментальная и клиническая гастроэнтерология. 2018;158(10): 34–42. DOI: 10.31146/1682-8658-ecg-158-10-34-42
Загрузить полный текст
Таблицы ODE · Документация разработчика SciML
Явные методы Рунге-Кутты
-
конструктЭулер— метод Эйлера 1-го порядка. -
structHuen()Метод Huen порядка 2. -
structRalston()— Метод Ральстона порядка 2. -
structSSPRK22()— Явный метод SSP 2-го порядка, использующий 2 этапа. -
конструктКутта3— классический метод Кутты 3-го порядка. -
конструкцияSSSPRK33()— Явный метод SSP 3-го порядка с использованием 3-х этапов. -
structSSPRK43()— Явный метод SSP порядка 3 с использованием 4 этапов.
-
конструктRK4— Классический метод Рунге-Кутта 4-го порядка. -
конструктRK438Правило— Классический метод 4-го порядка «Правило 3/8». -
structSSPRK104()— явный метод SSP 4-го порядка с использованием 10 этапов. -
buildBogakiShampine3()— метод 2/3 Богакаи-Шампайна. -
конструктRKF4()— Рунге-Кутта-Фельберг 3/4. -
конструктRKF5()— Рунге-Кутта-Фельберг 4/5. -
structRungeFirst5()— Первый метод Рунге 5-го порядка. -
structCassity5()— Метод Кэссити 5-го порядка. -
structLawson5()— Метод Лоусона 5-го порядка. -
конструкция Лютера-Конена5— первый метод Лютера-Конена 5-го порядка. -
конструкцияЛютерКонен52()— Второй метод 5-го порядка Лютера-Конена. -
structLutherKonen53()— Третий метод Лютера-Конена 5-го порядка.
-
buildPapakostasPapaGeorgiou5()— Papakostas и PapaGeorgiou более стабильный метод порядка 5. -
buildPapakostasPapaGeorgiou52()— Papakostas и PapaGeorgiou более эффективный метод порядка 5. -
конструктЦитурас5()— Метод Цитураса порядка 5. -
конструкцияBogakiShampine5()— Метод Богаки и Ордена Шампина 5. -
structSharpSmart5()— метод Sharp and Smart Order 5. -
конструктCashKarp()— Метод Кэша-Карпа 4/5. -
построить ДормандПринц()— Дорманд-Принц 4/5. -
structButcher6()— Метод Мясника первого порядка 6. -
structButcher62()— Метод Мясника второго порядка 6. -
structButcher63()— Метод Мясника третьего порядка 6. -
buildDormandPrince6()— метод Дорманд-Принса 5/6. -
structSharpVerner6()Метод Шарпа-Вернера 5/6.
-
structVerner916()— более эффективный метод Вернера порядка 6 (1991). -
structVerner9162()— Второй более эффективный метод Вернера порядка 6 (1991). -
structVernerRobust6()— «самый надежный» метод Вернера порядка 6. -
конструкция VernerEfficient6()— «Самый эффективный» метод Вернера порядка 6. -
buildPapakostas6()— метод порядка 6 Папакостаса. -
structLawson6()— Метод порядка 6 Лоусона. -
конструкт Цитоурас Папакостас6()— Метод порядка 6 Цитураса и Папакостаса. -
buildDormandLockyerMcCorriganPrince6()— метод порядка 6 Дорманда-Локьера-МакКорригана-Принса. -
конструкция ТанакаКасугаЯмаситаЯдзаки6А()— Танака-Касуга-Ямасита-Ядзаки порядок 6 метод А. -
ConstructtanakaSugayamashitayazaki6b ()-Танака-касуга-ямашита-язаки. Касуга-Ямасита-Ядзаки, метод порядка 6 D.
-
, buildMikkawyEisa()— Метод Миккави и Эйсы порядка 6. -
structChummund6()— Метод Чаммунда первого порядка 6. -
structChummund62()— Метод Чаммунда второго порядка 6. -
structHuta6()— метод Huta первого порядка 6. -
конструктHuta62()— второй метод Хуты 6 порядка. -
structVerner6()— Старый метод порядка 6, приписываемый Вернеру. -
structDverk()— Классический алгоритм DVERK, приписываемый Вернеру. -
structClassicVerner6()— Классический алгоритм Вернера порядка 6 (1978). -
structButcher7()— Алгоритм Мясника порядка 7. -
structClassicVerner7()— классический алгоритм Вернера порядка 7 (1978). -
structVernerRobust7()— «наиболее надежный» алгоритм Вернера порядка 7. -
конструироватьTanakaYamashitaStable7()— Танака-Ямашита более стабильный алгоритм порядка 7.
-
конструироватьTanakaYamashitaEfficient7()— Танака-Ямасита более эффективный алгоритм порядка 7. -
buildSharpSmart7()— алгоритм Sharp-Smart порядка 7. -
structSharpVerner7()— Алгоритм Шарпа-Вернера порядка 7. -
structVerner7()— «самый эффективный» алгоритм Вернера порядка 7. -
structVernerEfficient7()— «самый эффективный» алгоритм Вернера порядка 7. -
structClassicVerner8()— классический алгоритм Вернера порядка 8 (1978). -
конструкцияCooperVerner8()— Алгоритм Купера-Вернера первого порядка 8. -
structCooperVerner82()— Алгоритм Купера-Вернера второго порядка 8. -
конструироватьЦитураса-Папакостаса8()— Алгоритм Цитураса-Папакостаса 8-го порядка. -
builtdverk78()— Классический алгоритм DVERK 8-го порядка. -
structEnrightVerner8()— Алгоритм Энрайта-Вернера порядка 8.
-
structCurtis8()— Алгоритм Кертиса порядка 8. -
structVerner8()— «самый эффективный» алгоритм Вернера порядка 8. -
конструктRKF8()— Метод Рунге-Кутта-Фельберга Порядок 7/8. -
convertDormandPrice8()— Метод Дорманд-Принц Орден 7/8. -
buildDormandPrince8_64bit()— метод Приказа Дорманд-Принца 7/8. Коэффициенты — это рациональные приближения, подходящие для 64-битной системы. -
structVernerRobust9()— «самый надежный» метод Вернера порядка 9. -
structVernerEfficient9()— «самый эффективный» метод Вернера порядка 9. -
structSharp9()— метод Sharp порядка 9. -
конструктЦитурас9()— Метод Цитураса первого порядка 9. -
конструктЦитурас92()— Метод Цитураса второго порядка 9. -
structCurtis10()— Метод Кертиса порядка 10. -
конструироватьOno10()— Метод порядка 10 Оно.
-
конструкцияFeagin10Tableau()— Метод порядка 10 Фигина. -
structCurtis10()— Метод Кертиса порядка 10. -
structBaker10()— метод Baker’s order 10. -
structHairer10()Метод Hairer порядка 10. -
structFeagin12Tableau()— Метод Фигина порядка 12. -
structOno12()— метод Оно порядка 12. -
buildFeagin14Tableau()Метод Фигина порядка 14.
Неявные методы Рунге-Кутты
-
structImplicitEuler— Неявный метод Эйлера 1-го порядка. -
buildMidpointRule— Метод средней точки 2-го порядка. -
constructTrapezoidalRule— The 2nd order Trapezoidal rule (2nd order LobattoIIIA) -
constructLobattoIIIA4— The 4th order LobattoIIIA -
constructLobattoIIIB2— The 2nd order LobattoIIIB -
constructLobattoIIIB4— The 4th order LobattoIIIB -
constructLobattoIIIC2— The 2nd order LobattoIIIC -
constructLobattoIIIC4— The 4th order LobattoIIIC -
constructLobattoIIICStar2— The 2nd order LobattoIIIC* -
constructLobattoIIICStar4— The 4th order LobattoIIIC* -
constructLobattoIIID2— The 2nd заказ LobattoIIID -
конструкцияLobattoIIID4— 4-й порядок LobattoIIID -
конструкцияRadauIA3— 3 -й заказ Radauia -
Constructradauia5— Radauia -
Constructradauiia3— ZDAUIIA VL1 -5'TCGATCGACTCTAGAGCCGCCACCATGGAGACAGACACACTCCTGCTATGGGTGCTGCTGCTCTGGGTTCCAGGTTCC;
VL2 -5′TGGGTGCTGCTGCTCTGGGTTCCAGGTTCCACAGGTGACATTCAGCTGACCCAATCTCCAAGCTCTTTGTCCGCCTCTG;
VL3 -5'CCCAATCTCCAAGCTCTTTGTCCGCCTCTGTGGGGGATAGGGTCACCATCACCTGCAGAGCCGGTGAAAGTGTTGATAT;
VL4 -5′CACCTGCAGAGCCGGTGAAAGTGTTGATATTTTTGGCGTTGGGTTTTTGCACTGGTACCAGCAGAAACCAGGAAAAGCT;
VL5 -5'AAGGGACGCCAGATTCTAGGTTGGATGCACGATAGATGAGGAGTTTGGGAGCTTTTCCTGGTTTCTGCTGGTACCAGTG;
VL6 -5'CTAATGGTGAGGGTGAAGTCTGTCCTAGACCCGGAGCCACTGAACCTAGAAGGGACGCCAGATTCTAGGTTGGATGCAC;
VL7 -5′ATTAGTTTGCTGACAGTAATAGGTGGCGAAATCTTCCGGCTGCAGACTGCTAATGGTGAGGGTGAAGTCTGTCCTAGAC;
VL8 -5’ACGTTTTATCTCGAGCTTGGTCCCCTGTCCGAACGTGTACGGGTCTTCATTAGTTGCTGACAGTAATAGGTGGCGAA;
Vh2 -5′TCGATCGACTCTAGAGCCGCCACCATGAAATGCAGCTGGGTTATCTTCTTCCTGATGGCAGTGGTTACAGGGGTCAATTCAGAGGTTC;
Vh3 -5′CAGTGGTTACAGGGTCAATTCAGAGGTTCAGCTGGTGGAGTCTGGGGGTGGCCTTGTGCAGCCAGGGGGCTCACTCCGTTTGTCCTGC;
Vh4 -5'CAGCCAGGGGGCTCACTCCGTTTGTCCTGCGCAGCTTCTGGCTTCAACATTAAAGACACCTATATGCACTGGGTGCGTCAGGCCCCTG;
Vh5 -5'CCTATATGCACTGGGTGCGTCAGGCCCCTGGTAAGGGCTGGAATGGGTTGCAAGGATTGATCCTGCGAATGGTAATAGTAAATATG;
VH5A -5′AGGTAGGCTGTGTTTTTGGATGTGTCTGGCCTTAGTGAAACGGCCCTTGACGCTATCGGCATATTACTATTACCATTCGCAGGATC;
VH5B -5′AGGTAGGCTGTGTTTTTGGATGTGTCTGGCCTTAGTGGCACGGCCCTGGAACTTCGGGACATATTACTATTACCATTCGCAGGATC;
VH6 -5'ACCAAACGGAGCACAATAATAGACGGCAGTGTCCTCAGCACGCAGGCTGTTCATCTGCAGGTAGGCTGTGTTTTTGGATGTGTCTGCG;
VH7 -5′GAGACGGTGACCAGGGTTCCTTGACCCCAGTAGGCCATAGCATAGTCAGACACGTAGTAACCAAACGGAGCACAATAATAGACGGCAGT;
VH8 -5′GGTGCTCTTGCTCGAGGGTGCCAGGGGGAAGACCGATGGGCCCTTAGTGGAGGCTGAGGAGACGGTGACCAGGGTTCCTTGACCCCAG;
- 1
- 1
- 1911111119.
 вводили отдельным группам бестимусных мышей с ксенотрансплантатами опухоли LS174T. В каждый момент времени для каждого mAb умерщвляли пять животных. Исследования биораспределения в тканях проводились на 0, 6, 24, 48, 72 и 96 ч.
вводили отдельным группам бестимусных мышей с ксенотрансплантатами опухоли LS174T. В каждый момент времени для каждого mAb умерщвляли пять животных. Исследования биораспределения в тканях проводились на 0, 6, 24, 48, 72 и 96 ч.a
Ошибки в скобках являются стандартными отклонениями.
Открыть в новой вкладке
Таблица II.
Биораспределение Процент введенной дозы на грамм (% ID/г) 131 I-меченых mAb cT84.66, M5A и M5B у мышей с опухолями
.Время (ч)
.. . . . .
.0
.6
.24
.48
.
72
.96
.cT84.66 mAb Blood 31.75 (1.36) a 17.89 (1.04) 13.47 (0.88) 6.67 (1.11) 6.30 (0.50) 5.19 (0.72) Liver 6.22 (0.47) 4.11 (0.30) 2.87 (0.29) 2.00 (0.16) 1.68 (0.14) 1.51 (0.18) Spleen 4.66 (0.35) 3.60 (0.27) 2.78 (0.23) 1.60 (0.28) 1.57 (0.15) 1.31 (0.21) Kidney 5.24 (0.39) 3.56 (0.29) 2.77 (0.18) 1.67 (0.29) 1.34 (0.16) 1.15 (0.18) Lung 8.  05 (0.56)
05 (0.56) 6.13 (0.41) 4.68 (0.27) 2,65 (0,50) 2,43 (0,16) 1.92 (0.23) Tumor 1.05 (0.09) 13.53 (1.26) 24.11 (0.94) 24.08 (3.75) 25.31 (2.38) 25.45 (3.04) Carcass 2.04 (0.04) 3.25 (0.22) 2.95 (0.08) 2.02 (0.24) 1.80 (0.10) 1.53 (0.17) M5A mAb Blood 38.7 (0.65) 23.86 (0.79) 11.92 (0.72) 10.31 (1.15) 5.10 (0.68) 3.75 (0.39) Liver 8.14 (0.48) 5.42 (0.30) 2.44 (0.29) 2.65 (0.11) 1.68 (0.  37)
37) 1.27 (0.18) Spleen 7.35 (0.65 ) 4.63 (0.43) 2.35 (0.28) 2.67 (0.34) 1.52 (0.31) 1.05 (0.23) Kidney 6.75 (0.11) 4.80 (0.21) 2.43 (0.31) 2.27 (0.17) 1.20 (0.28) 0.90 (0.21) Lung 11.09 (0.72) 7.84 (0.15) 4.18 (0.41) 3.59 (0.26) 2,00 (0,43) 1,45 (0,37) Tumor 1.78 (0.09) 14.06 (1.26) 26.83 (0.94) 32.65 (3.75) 22.67 (2.38) 23.83 (3.04) Carcass 2.5 ( 0.12) 3.44 (0.05) 2.75 (0.20) 2.67 (0.13) 1.68 (0.21) 1.39 (0.18) M5B mAb Blood 31.  37 (1.00)
37 (1.00) 15.81 (0.43) 10.49 (0.51) 8.43 (0.92) 5.79 (0.83) 5.81 (0.63) Liver 8.2 (0.41) 3.54 (0.11) 3.06 (0.33) 2.31 (0.10) 1.72 (0.19) 1.72 (0.15) Spleen 5.53 (0.30) 3.31 (0,26) 2.51 (0.22) 2.07 (0.11) 1.53 (0.17) 1.83 (0.33) Kidney 5.13 (0.51) 3.17 (0.15) 2.43 (0.28) 2.01 (0.22) 1.38 (0.20) 1.52 (0.15) Lung 9.51 (0.68) 5.05 (0.16) 3.74 (0.15) 3.35 (0.27) 2.41 (0.41) 2,30 (0,16) Tumor 5.17 (3.66) 10.52 (0.75) 19.58 (0.92) 24.  83 (4.84)
83 (4.84) 18.57 (2.62) 7.15 (2.25) Carcass 2.36 (0.18) 2.56 (0.10) 2.54 (0.10) 2.18 (0.10) 1.81 (0.14) 1.60 (0.10)
.Время (ч)
.. . . . .
.0
.6
.24
.48
.72
.96
.cT84.66 mAb Blood 31.  75 (1.36) a
75 (1.36) a 17.89 (1.04) 13.47 (0.88) 6.67 (1,11) 6,30 (0,50) 5,19 (0,72) печени 6,22 (0,47) 4,11 (0,30) 77 (0,1489 4,11 (0,30) 77 (0,2989 4,11 (0,30) 77 (0,2, 88,4, 1.51 (0.18) Spleen 4.66 (0.35) 3.60 (0.27) 2.78 (0.23) 1.60 (0.28) 1.57 (0.15) 1.31 (0.21) Kidney 5.24 (0.39) 3.56 (0.29) 2.77 (0.18) 1.67 (0.29) 1.34 (0.16) 1.15 (0.18) Lung 8.05 (0.56) 6,13 (0,41) 4.68 (0.27) 2.65 (0.50) 2.43 (0.16) 1.92 (0.23) Tumor 1.05 (0.09) 13.53 (1.26) 24.  11 (0.94)
11 (0.94) 24.08 (3.75) 25.31 (2.38) 25.45 (3.04) Carcass 2.04 (0.04) 3.25 (0.22) 2.95 (0.08) 2.02 (0.24) 1.80 (0.10) 1,53 (0,17) M5A mAb Blood 38.7 (0.65) 23.86 (0.79) 11.92 (0.72) 10.31 (1.15) 5.10 (0.68) 3.75 (0.39) Liver 8.14 (0.48) 5.42 (0.30) 2.44 (0.29) 2.65 (0.11) 1.68 (0.37) 1.27 (0.18) Spleen 7.35 (0.65) 4.63 (0.43) 2.35 (0.28) 2.67 (0.34) 1.52 (0.31) 1.05 (0.23) Kidney 6.  75 (0.11)
75 (0.11) 4.80 (0.21) 2.43 (0.31) 2.27 (0.17) 1.20 (0.28) 0.90 (0.21) Lung 11.09 (0.72) 7,84 (0,15) 4.18 (0.41) 3.59 (0.26) 2.00 (0.43) 1.45 (0.37) Tumor 1.78 (0.09) 14.06 (1.26) 26.83 (0.94) 32.65 (3.75) 22.67 (2.38) 23.83 (3.04) Carcass 2.5 (0.12) 3.44 (0.05) 2.75 (0.20) 2.67 (0.13) 1.68 (0.21) 1,39 (0,18) M5B mAb Blood 31.37 (1.00) 15.81 (0.43) 10.49 (0.51) 8.43 (0.92) 5.79 (0.  83)
83) 5.81 (0.63) Liver 8.2 (0.41) 3.54 (0.11) 3.06 (0.33) 2.31 (0.10) 1.72 (0.19) 1.72 (0.15) Spleen 5.53 (0.30) 3.31 (0.26) 2.51 (0.22) 2.07 (0.11) 1.53 (0.17) 1.83 (0.33) Kidney 5.13 (0.51) 3.17 (0.15) 2.43 (0.28) 2.01 (0.22) 1.38 (0.20) 1.52 (0.15) Lung 9.51 (0.68) 5,05 (0,16) 3.74 (0.15) 3.35 (0.27) 2.41 (0.41) 2.30 (0.16) Tumor 5.17 (3.66) 10.52 (0.75) 19.58 (0.92) 24.83 (4.84) 18.57 (2.62) 7.15 (2.25) Carcass 2.  36 (0.18)
36 (0.18) 2.56 (0.10) 2.54 (0.10) 2.18 (0.10) 1.81 (0.14) 1,60 (0,10) 131 I-меченые антитела cT84.66, M5A и M5B вводили отдельным группам бестимусных мышей, несущих ксенотрансплантаты опухоли LS174T. В каждый момент времени для каждого mAb умерщвляли пять животных. Исследования биораспределения в тканях проводились через 0, 6, 24, 48, 72 и 96 часов.
a
Ошибки в скобках являются стандартными отклонениями.
Открыть в новой вкладке
мАт M5A было выбрано в качестве кандидата для клинической разработки на основании более высокого поглощения опухолью и большего содержания «человеческих» остатков и было переименовано в hT84.66. Для определения производственной способности клона hT84.66 клон с наилучшей экспрессией был субклонирован и размножен в биореакторе с полыми волокнами CP2000. В ограниченном производственном цикле уровень активности анти-СЕА составил 250 мкг/мл, а урожай составил 640 мг.
 Часть урожая очищали, конъюгировали с макроциклом 1,4,7,10-тетраазациклододеканом 9.0437 N , N ′, N ″, N ″′-тетрауксусной кислоты (DOTA) (Lewis, 2001) и радиоактивно меченных 111 In. [ 111 In]DOTA-hT84.66 вводили внутривенно двум бестимусным мышам, несущим ксенотрансплантаты LS174T. Мышам ввели седацию и сделали снимки с помощью планарной сцинтиграфической камеры высокого разрешения. мАт hT84.66 продемонстрировали высокоспецифичную локализацию опухоли и удаление из нормальных тканей в течение 7 дней (фиг. 8). Эта комбинация данных свидетельствует о терапевтическом потенциале mAb hT84.66.
Часть урожая очищали, конъюгировали с макроциклом 1,4,7,10-тетраазациклододеканом 9.0437 N , N ′, N ″, N ″′-тетрауксусной кислоты (DOTA) (Lewis, 2001) и радиоактивно меченных 111 In. [ 111 In]DOTA-hT84.66 вводили внутривенно двум бестимусным мышам, несущим ксенотрансплантаты LS174T. Мышам ввели седацию и сделали снимки с помощью планарной сцинтиграфической камеры высокого разрешения. мАт hT84.66 продемонстрировали высокоспецифичную локализацию опухоли и удаление из нормальных тканей в течение 7 дней (фиг. 8). Эта комбинация данных свидетельствует о терапевтическом потенциале mAb hT84.66.Рис. 8.
Открыть в новой вкладкеСкачать слайд
[ 111 В]M5A γ изображение камеры. [ 111 In]DOTA-M5A mAb вводили внутривенно бестимусной мыши с ксенотрансплантатом LS174T. Мышам вводили седативное средство и помещали на плоскостную сцинтиграфическую камеру высокого разрешения на 0, 1, 2, 6 и 7 дни.

Резюме
Настоящая стратегия гуманизации была основана на необходимости сохранить наш обширный клинический опыт использования мышиных и химерных антител T84.66 для радиоиммунотерапии. Хотя в последние годы появились новые технологии гуманизации, подход с прививкой CDR сохранил высокую специфичность T84.66 при одновременном снижении потенциала иммунологического ответа. Полученные ранее данные о кристаллической структуре рекомбинантного диатела T84.66 сыграли важную роль в использовании этого подхода. Интересно, что наложение структур показало, что пептидные сегменты, которые необходимо было трансплантировать, не соответствовали общепринятым определениям петель CDR. В качестве процесса проектирования гуманизация T84.66 прошла успешно, о чем свидетельствует тот факт, что не потребовалось утомительных обратных мутаций для восстановления специфичности или аффинности. Вопрос о том, будет ли это недавно сконструированное антитело против СЕА иммуногенным, еще предстоит решить в клинике.
 Радиоактивно меченое hT84.66 mAb является многообещающим новым терапевтическим средством, которое может помочь в решении этой проблемы.
Радиоактивно меченое hT84.66 mAb является многообещающим новым терапевтическим средством, которое может помочь в решении этой проблемы.2
P.J.Yazaki и M.A.Sherman внесли равный вклад в эту работу
Авторы выражают благодарность за экспертную техническую помощь Cheryl Clark, Chia-wei Cheung, Agnes Gardner, Anne-line Anderson и Desiree Crow в этом исследовании. Эта работа была поддержана грантами Национального института здравоохранения (CA 43904 и грант поддержки онкологического центра CA 33572) и Министерства обороны N00014-02-1-0958.
Ссылки
Banfield, M.J., King, D.J., Mountain,A. и Брэди, Р.Л. (
1997
)
Белки
,
29
,
161
–171.
Битти, Джей Ди и др. . (
1986
)
Рак Res.

,
46
,
6494
–6502.
Беббингтон, К., Реннер, Г., Томсон, С., Кинг, Д., Абрамс, Д. и Яррантон, Г.Т. (
1992
)
Био/технология
,
10
,
169
–75.
Бернштейн, Ф. К., Кетцле, Т. Ф., Уильямс, Г. Дж., Мейер, Э. Ф., младший, Брайс, доктор медицинских наук, Роджерс, младший, Кеннард, О., Шиманучи, Т. и Тасуми, М. (
1977
)
J. Mol. биол.
,
112
,
535
–542.
Брюггеманн М., Спайсер К., Булувела Л., Розуэлл И., Бартон С., Сурани М.А. и Кролики, Т.Х. (
1991
)
евро.
 Дж. Иммунол.
Дж. Иммунол.,
5
,
1323
–1326.
Кармайкл, Дж. А., Пауэр, Б. Э., Гарретт, Т. П., Язаки, П. Дж., Шивли, Дж. Э., Раубичек, А. А., Ву, А. М. и Хадсон, П.Дж. (
2003
)
J. Mol. биол.
,
326
,
341
–351.
Картер, П., Горман, К.М., Риджуэй, Дж.Б.Б., Хеннер, Д., Вонг, У.Л.Т., Роуленд, А.М., Коттс, К., Карвер, М.Э. и Шепард, Х.М. (
1992
)
Проц. Натл акад. науч. США
,
89
,
4285
–4289.
Чотия, К. и Леск, А.М. (
1987
)
J.
 Mol. биол.
Mol. биол.,
196
,
901
–917.
Эйгенброт, К., Рэндал, М., Преста, Л., Картер, П. и Коссяков А.А. (
1993
)
J. Mol. биол.
,
229
,
969
–995.
Эйгенброт, К., Гонсалес, Т., Майеда, Дж., Картер, П., Вертер, В., Хоталинг, Т., Фокс, Дж. и Кесслер, Дж. (
1994
)
Белки
,
18
,
49
–62.
Фут, Дж. и Винтер, Г. (
1992
)
J. Mol. биол.
,
224
,
487
–499.

Гибрат, Дж., Мадей, Т. и Брайант, С.Х. (
1996
)
Тел. мнение Структура биол.
,
6
,
377
–385.
Хортон Р.М., Хант Х.Д., Хо С.Н., Пуллен Дж.К. и Пиз, Л.Р. (
1989
)
Ген
,
77
,
61
–68.
Джонсон, Г. и Ву, Т.Т. (
2001
)
Nucleic Acids Res.
,
29
,
205
–206.
Джонс, П.Т., Уважаемый, П.Х., Фут, Дж., Нойбергер, М.С. и Винтер, Г. (
1986
)
Природа
,
6069
,
522
–525.

Кабат, Э.А. и Ву, Т.Т. (
1971
)
Энн. Н. Я. акад. науч.
,
190
,
382
–393.
Лэммли, У. (
1970
)
Природа
,
227
,
680
–685.
Льюис, М. Р., Као, Дж. Ю., Андерсон, А. Л., Шивли, Дж. Э. и Раубичек, А. (
2001
)
Bioconj. хим.
12
,
320
–324.
Лоу, Нью-Мексико, Холлигер, П.Х. и Винтер, Г. (
1996
)
J. Mol. биол.
,
260
,
359
–368.

МакКаллум, Р.М., Мартин, А.К. и Торнтон, Дж.М. (
1996
)
J. Mol. биол.
,
262
,
732
–745.
Мендес, М.Дж. и др. . (
1997
)
Нац. Жене.
,
2
,
146
–156.
Мореа, В.Т.А., Рустичи, М., Чотия, К. и Леск, А.М. (
1998
)
J. Mol. биол.
,
275
,
269
–294.
Мортон, Б.А., О'Коннор-Трессел, М., Битти, Б.Г., Шивли, Дж.Е. и Битти, Дж.Д. (
1988
)
Арх.
 Surg.
Surg.,
10
,
1242
–1246.
Ноймайер, М., Шивли, Л., Чен, Ф.С., Гайда, Ф.Дж., Ильген, К., Пакстон, Р.Дж., Шивли, Дж.Е. и Риггс, А.Д. (
1990
)
Рак Res.
,
50
,
2128
–2134.
О'Брайен, С. и Джонс, Т. (
2003
)
Методы Мол. биол.
,
207
,
81
–100.
О'Коннор, С.Дж., Мэн, Ю.Г., Резайе, А.Р. и Преста, Л.Г. (
1998
)
Protein Eng.
,
11
,
321
–328.

Падлан, Э.А., Абергель, К. и Типпер, Дж.П. (
1995
)
FASEB J.
,
9
,
133
–139.
Шрофф Р.В., Фун К.А., Битти С.М., Олдхэм Р.К. и Морган, AC, Jr. (
1985
)
Рак Res.
,
45
,
879
–885.
Шаулер Д.Л., Варфоломей Р.М., Смит Л.М. и Диллман, Р.О. (
1985
)
J. Immunol.
,
135
,
1530
–1535.
Вагенер, К., Кларк, Б.Р., Рикард, К.Дж. и Шивели, Дж.Э. (
1983
)
J.
 Immunol.
Immunol.,
130
,
2302
–2307.
Винтер, Г., Гриффитс, А.Д., Хокинс, Р.Е. и Хугенбум, Х.Р. (
1994
)
Год. Преподобный Иммунол.
,
12
,
433
–455.
Вонг, Д.Ю.К. и др. . (
1995
)
Рак Res.
,
55
,
5929с
–5934с.
Вонг, Д.Ю.К. и др. . (
1997
)
J. Nucl. Мед.
,
38
,
1951
–1959.

Вонг, Д.Ю.К. и др. . (
1999
)
Клин. Рак рез.
,
5
,
3224
–3231.
Ву А.М., Чен В., Раубитчек А., Уильямс Л.Е., Ноймайер М., Фишер Р. и Шивели, Дж.Э. (
1996
)
Иммунотехнология
,
2
,
221
–236.
Сян Дж., Ша Ю., Цзя З., Прасад Л. и Дельбэр, Л.Т. (
1995
)
Дж. Мол. биол.
,
253
,
385
–390.
Язаки, П.Дж., Кларк, К., Шивли, Л., Чунг, К.-В., Ле, В., Шпиковска, Б., Шивели, Дж. Э., Раубичек, А.
 А. и Ву, А.М. (
А. и Ву, А.М. (2001
)
J. Immunol. Методы
,
253
,
195
–208.
Янг, Х.Ю., Хефта, Л.Дж., Язаки, П.Дж., Ву, А.М. и Шивели, Дж.Э. (
1998
)
Противораковые рез.
,
18
,
3192
–202.
Примечания автора
1 Отделение радиоиммунотерапии, 6 Отделение радиологии и 7 Отделение радиационной онкологии, Национальный медицинский центр «Город надежды», 1500 East Duarte Road, Duarte, CA
, 4 Отделение информационных наук и 5 Отделение иммунологии, Научно-исследовательский институт Бекмана Город надежды, Дуарте, Калифорния
и 8 Кафедра молекулярной и медицинской фармакологии, Институт молекулярной визуализации Крампа, Медицинский факультет Калифорнийского университета, Лос-Анджелес, Калифорния
Последний
Самые читаемые
Самые цитируемые
- Доступ через ВАШЕГО Учреждение
- Технический комитет ATM Forum, Спецификация управления трафиком, версия 4.0, af-tm-0056.000,...
- Технический комитет ATM Forum, Интерфейс частного сетевого узла, версия 2.0, Рабочий проект,..
- А. Э. Экберг, Т.-К. Хоу, Влияние совместного использования выходного буфера на потребность в буфере в коммутаторе пакетов ATDM, в: Proc....
- Н. Эндо, Т. Охучи, Т. Козаки, Х. Кувахара, М. Мори, Оценка характеристик трафика A Коммутатор ATM с общим буфером,.
 ..
.. - Н. Эндо, Т. Козаки, Т. Охучи, Х. Кувахара, С. Гохара, Переключатель общей буферной памяти для обмена банкоматом, IEEE Trans....
- Н. Эндо, А. Такасе, С. Гохара , С. Такахаши, Дж. Янаги, Архитектура системы ATM для плавного развития сети, в:...
- Скачать : Скачать полноразмерное изображение
- Скачать : Скачать полноразмерное изображение
- Скачать : Скачать полноразмерное изображение
- Скачать : Скачать полноразмерное изображение
- Обзор
- Открытый доступ
- Опубликовано:
- Yoshiki Sekijima 1 ,
- Mitsuharu Ueda 2 ,
- Haruki Koike 3 ,
- Sonoko Misawa 4 ,
- Tomonori Ishii 5 &
- …
- Yukio Ando 2
11 тыс.
 обращений
обращений70 цитирований
2 Альтметрический
Сведения о показателях
- 1.
История болезни и физикальное обследование, которые могут вызвать клиническое подозрение и позволить поставить предварительный диагноз ATTR-FAP
- 2.
Подтверждение с использованием точных диагностических инструментов, включая гистопатологию и генетический анализ (рис. 4)
- 1.
Таргетная терапия, модифицирующая заболевание, для предотвращения дальнейшего образования амилоидных отложений (например, ЛТ, кинетические стабилизаторы транстиретина, такие как тафамидис, дифлунизал) [1, 35]
- 2.
Симптоматическая терапия сенсомоторной и вегетативной полинейропатии и травм сердца, почек и глаз [1, 35]
- 3.
Генетическое консультирование и поддерживающая терапия [1, 105]
21 мая 2019
.
- AE:
Побочное явление
- АТТР:
Транстиретин
- ATTRwt:
Транстиретин дикого типа
- ДИ:
Доверительный интервал
- CIDP:
Хроническая воспалительная демиелинизирующая полиневропатия
- CTS:
Синдром запястного канала
- ФАП:
Семейная амилоидная полиневропатия
- ФАПВТР:
Семейная амилоидотическая полинейропатия Всемирный реестр трансплантологов
- h-ATTRm:
наследственный транстиретин
- LT:
Трансплантация печени
- ИМТ:
модифицированный индекс массы тела
- МВАО:
Министерство здравоохранения, труда и социального обеспечения, Япония
- ШН+7:
Оценка нейропатии плюс 7 нервных тестов
- NIS-LL:
Оценка нейропатии — нижние конечности
- НПВП:
нестероидный противовоспалительный препарат
- NYHA:
Нью-Йоркская кардиологическая ассоциация
- PND:
Инвалидность полиневропатии
- Общее качество жизни:
Общий балл диабетической нейропатии качества жизни в Норфолке
- ТТР:
Транстиретин
- ТУДКА:
Тауроурсодезоксихолевая кислота
- Val30Met:
Замена валина метионином в положении 30
Benson MD, Kincaid JC. Молекулярная биология и клинические особенности амилоидной невропатии. Мышечный нерв. 2007; 36: 411–23.
КАС пабмед Google ученый
Като-Мотозаки Ю., Оно К., Шима К., Моринага А., Матия Т., Нодзаки И., Сибата-Хамагути А., Фурукава Ю., Янасэ Д., Исида С. и др. Эпидемиология семейной амилоидной полинейропатии в Японии: выявление нового эндемического очага. J Neurol Sci. 2008; 270:133–40.
ПабМед Google ученый
Alemi M, Gaiteiro C, Ribeiro CA, Santos LM, Gomes JR, Oliveira SM, Couraud PO, Weksler B, Romero I, Saraiva MJ, et al.
 Транстиретин участвует в транспорте бета-амилоида из головного мозга в печень — участие белка 1?, связанного с рецептором липопротеинов низкой плотности. Научный доклад 2016; 6: 20164.
Транстиретин участвует в транспорте бета-амилоида из головного мозга в печень — участие белка 1?, связанного с рецептором липопротеинов низкой плотности. Научный доклад 2016; 6: 20164.КАС пабмед ПабМед Центральный Google ученый
Кавалларо Т., Мартоне Р.Л., Дворк А.Дж., Шон Э.А., Герберт Дж. Пигментный эпителий сетчатки является уникальным местом синтеза транстиретина в крысином глазу. Invest Ophthalmol Vis Sci. 1990; 31: 497–501.
КАС пабмед Google ученый
Герберт Дж., Уилкокс Дж. Н., Фам К. Т., Фремо Р. Т. мл., Зевиани М., Дворк А., Сопрано Д. Р., Маковер А., Гудман Д. С., Циммерман Э. А. и др. Транстиретин: специфический транспортный белок сосудистого сплетения в головном мозге человека. 1986 Премия С. Вейра Митчелла. Неврология. 1986; 36: 900–11.
КАС пабмед Google ученый
">Ричардсон С.Дж., Виджаягунаратне Р.С., Д'Суза Д.Г., Даррас В.М., Ван Херк С.Л. Транспорт гормонов щитовидной железы через сосудистое сплетение в головной мозг: роль трансмембранных переносчиков транстиретина и гормонов щитовидной железы. Фронтальные нейроски. 2015;9:66.
ПабМед ПабМед Центральный Google ученый
Шрайбер Г., Олдред А.Р., Яворовски А., Нильссон С., Ахен М.Г., Сегал М.Б. Транспорт тироксина из крови в мозг посредством синтеза транстиретина в сосудистых сплетениях. Am J Phys. 1990; 258: R338–45.
КАС Google ученый
">Hou X, Aguilar MI, Small DH. Транстиретин и семейная амилоидотическая полиневропатия. Недавний прогресс в понимании молекулярного механизма нейродегенерации. FEBS J. 2007; 274: 1637–50.
КАС пабмед Google ученый
Брито Р.М.М., Дамас А.М., Сарайва М.Дж. Образование амилоида транстиретином: от стабильности белка к агрегации белка. Curr Med Chem – агенты Immun, Endoc и Metab. 2003;3:349–60.
КАС Google ученый
">Takahashi K, Yi S, Kimura Y, Araki S. Семейная амилоидотическая полинейропатия 1 типа в Кумамото, Япония: клинико-патологическое, гистохимическое, иммуногистохимическое и ультраструктурное исследование. Хум Патол. 1991;22:519-27.
КАС пабмед Google ученый
Койке Х., Мису К., Сугиура М., Иидзима М., Мори К., Ямамото М., Хаттори Н., Мукаи Э., Андо Ю., Икеда С. и др. Патология семейной амилоидной полинейропатии TTR Met30 с ранним и поздним началом. Неврология. 2004; 63: 129–38.
КАС пабмед Google ученый
">Takahashi K, Sakashita N, Ando Y, Suga M, Ando M. Семейная амилоидотическая полинейропатия I с поздним началом: представление трех случаев вскрытия по сравнению с 19 случаями вскрытия обычного типа. Патол Инт. 1997; 47: 353–9.
КАС пабмед Google ученый
Адамс Д., Лозерон П., Лакруа С. Амилоидные невропатии. Карр Опин Нейрол. 2012; 25: 564–72.
КАС пабмед Google ученый
Дорн М.Ф., Рёкен С., Де Блекер Дж.Л., Мартин Дж.Дж., Форгерд М., Ван ден Берг П.Ю., Ферберт А., Хиндерхофер К.
 , Шредер Дж.М., Вейс Дж. и др. Диагностические признаки и подводные камни при прогрессирующей транстиретиновой амилоидной нейропатии с поздним началом. Дж Нейрол. 2013; 260:3093–108.
, Шредер Дж.М., Вейс Дж. и др. Диагностические признаки и подводные камни при прогрессирующей транстиретиновой амилоидной нейропатии с поздним началом. Дж Нейрол. 2013; 260:3093–108.КАС пабмед Google ученый
Коике Х., Танака Ф., Хасимото Р., Томита М., Кавагашира Ю., Иидзима М., Фудзитаке Дж., Каванами Т., Като Т., Ямамото М. и др. Естественная история транстиретиновой семейной амилоидной полинейропатии Val30Met: анализ случаев с поздним началом в неэндемичных районах. J Neurol Нейрохирург Психиатрия. 2012;83:152–158.
ПабМед Google ученый
Мариани Л.Л., Лозерон П., Теодин М., Минчева З., Синьяте А., Дюко Б., Альгаларрондо В., Денье С., Адам С., Николя Г. и др. Корреляция генотип-фенотип и течение транстиретиновых семейных амилоидных полиневропатий во Франции. Энн Нейрол. 2015; 78: 901–16.
КАС пабмед ПабМед Центральный Google ученый
">Кито С., Итога Э., Камия К., Кишида Т., Ямамура Ю. Исследования семейной амилоидной полинейропатии в деревне Огава, Япония. Евр Нейрол. 1980; 19: 141–51.
КАС пабмед Google ученый
Мису К., Хаттори Н., Нагамацу М., Икеда С., Андо Ю., Наказато М., Такей Ю., Ханью Н., Усуи Ю., Танака Ф. и др. Семейная амилоидная полинейропатия I с поздним началом (транстиретин-Met30-ассоциированная семейная амилоидная полинейропатия), не связанная с эндемическим очагом в Японии. Клинико-патологические и генетические особенности. Мозг. 1999; 122 (часть 10): 1951–62.
ПабМед Google ученый
">Sousa A, Andersson R, Drugge U, Holmgren G, Sandgren O. Семейная амилоидотическая полинейропатия в Швеции: географическое распространение, возраст начала и распространенность. Хам Херед. 1993; 43: 288–94.
КАС пабмед Google ученый
Sousa A, Coelho T, Barros J, Sequeiros J. Генетическая эпидемиология семейной амилоидотической полинейропатии (FAP) типа I в Повуа-ду-Варзин и Вила-ду-Конде (север Португалии). Am J Med Genet. 1995;60:512–21.
КАС пабмед Google ученый
">Парман Ю., Адамс Д., Обичи Л., Галан Л., Гергельчева В., Зур О.Б., Коэльо Т. Шестьдесят лет транстиретиновой семейной амилоидной полинейропатии (TTR-FAP) в Европе: где мы сейчас? Европейский сетевой подход к определению эпидемиологии и моделей лечения TTR-FAP. Карр Опин Нейрол. 2016;29(Приложение 1): S3–S13.
КАС пабмед ПабМед Центральный Google ученый
Планте-Борденев В., Феррейра А., Лалу Т., Зарос С., Лакруа С., Адамс Д., Саид Г. Диагностические ошибки при спорадической транстиретиновой семейной амилоидной полинейропатии (TTR-FAP).
 Неврология. 2007; 69: 693–8.
Неврология. 2007; 69: 693–8.ПабМед Google ученый
Koike H, Hashimoto R, Tomita M, Kawagashira Y, Iijima M, Tanaka F, Sobue G. Диагностика спорадической транстиретиновой семейной амилоидной полинейропатии Val30Met: практический анализ. Амилоид. 2011;18:53–62.
КАС пабмед Google ученый
Coelho T, Maia LF, Martins da Silva A, Waddington Cruz M, Planté-Bordeneuve V, Lozeron P, Suhr OB, Campistol JM, Conceição IM, Schmidt HH, et al. Тафамидис при транстиретиновой семейной амилоидной полинейропатии: рандомизированное контролируемое исследование. Неврология. 2012; 79: 785–92.
КАС пабмед ПабМед Центральный Google ученый
Эрикзон Б.Г., Вильчек Х.Е., Ларссон М., Виджаятунга П., Стангоу А., Пена Дж.Р., Фуртадо Э., Баррозу Э.
 , Даниэль Дж., Сэмюэл Д. и другие. Трансплантация печени при наследственном транстиретиновом амилоидозе: спустя 20 лет все еще лучшая терапевтическая альтернатива? Трансплантация. 2015; 99: 1847–54.
, Даниэль Дж., Сэмюэл Д. и другие. Трансплантация печени при наследственном транстиретиновом амилоидозе: спустя 20 лет все еще лучшая терапевтическая альтернатива? Трансплантация. 2015; 99: 1847–54.КАС пабмед Google ученый
Планте-Борденев В. Обновление диагностики и лечения транстиретиновой семейной амилоидной полинейропатии. Дж Нейрол. 2014; 261:1227–33.
ПабМед Google ученый
Adams D, Théaudin M, Cauquil C, Algalarrondo V, Slama M. Невропатия FAP и новые методы лечения. Curr Neurol Neurosci Rep. 2014; 14:435.
Holmgren G, Steen L, Ekstedt J, Groth CG, Ericzon BG, Eriksson S, Andersen O, Karlberg I, Norden G, Nakazato M, et al. Биохимический эффект трансплантации печени у двух шведских пациентов с семейной амилоидотической полинейропатией (FAP-met30). Клин Жене. 1991;40:242–6.

КАС пабмед Google ученый
Икеда С., Такей Ю., Янагисава Н., Мацунами Х., Хашикура Ю., Икегами Т., Кавасаки С. Регенерация периферических нервов при семейной амилоидной полиневропатии после трансплантации печени. Энн Интерн Мед. 1997; 127: 618–20.
КАС пабмед Google ученый
Ando Y, Tanaka Y, Ando E, Yamashita T, Nishida Y, Tashima K, Suga M, Uchino M, Ando M. Влияние трансплантации печени на вегетативную дисфункцию при семейной амилоидотической полинейропатии I типа. Lancet. 1995;345:195–6.
КАС пабмед Google ученый
Okumura K, Yamashita T, Masuda T, Misumi Y, Ueda A, Ueda M, Obayashi K, Jono H, Yamashita S, Inomata Y и др. Отдаленные результаты лечения больных наследственным транстиретиновым амилоидозом В30М с полинейропатией после трансплантации печени.
 Амилоид. 2016;23:39–45.
Амилоид. 2016;23:39–45.КАС пабмед Google ученый
Хуанг Г., Уэда М., Тасаки М., Ямасита Т., Мисуми Ю., Масуда Т., Суэнага Г., Иноуэ Ю., Киношита Ю., Мацумото С. и др. Клинико-патологические и биохимические признаки тиреоидного амилоида при наследственном транстиретиновом амилоидозе с трансплантацией печени и без нее. Амилоид. 2017; 24:24–9.
КАС пабмед Google ученый
Ямасита Т., Андо Ю., Уэда М., Накамура М., Окамото С., Зеледон М.Е., Хирахара Т., Хираи Т., Уэда А., Мисуми Ю. и др. Влияние трансплантации печени на церебральную амилоидную ангиопатию, связанную с транстиретином Tyr114Cys. Неврология. 2008; 70: 123–128.
КАС пабмед Google ученый
Waddington Cruz M, Benson MD. Обзор тафамидиса для лечения амилоидоза, связанного с транстиретином.
 Нейрол Тер. 2015; 4:61–79.
Нейрол Тер. 2015; 4:61–79.ПабМед ПабМед Центральный Google ученый
Misu K, Hattori N, Ando Y, Ikeda S, Sobue G. Ожидание семейной амилоидной полинейропатии с ранним, но не поздним началом (TTR met 30) в Японии. Неврология. 2000;55:451–2.
КАС пабмед Google ученый
Koike H, Ikeda S, Takahashi M, Kawagashira Y, Iijima M, Misumi Y, Ando Y, Ikeda SI, Katsuno M, Sobue G. Повреждение шванновских клеток и эндотелиальных клеток при транстиретиновой семейной амилоидной полинейропатии. Неврология. 2016; 87: 2220–9.
КАС пабмед Google ученый
Koike H, Kawagashira Y, Iijima M, Yamamoto M, Hattori N, Tanaka F, Hirayama M, Ando Y, Ikeda S, Sobue G. Электрофизиологические особенности семейной полинейропатии транстиретина Met30 с поздним началом, не связанной с эндемическими очагами.
 Дж Нейрол. 2008; 255:1526–33.
Дж Нейрол. 2008; 255:1526–33.ПабМед Google ученый
Conceição I, Gonzalez-Duarte A, Obici L, Schmidt HH, Simoneau D, Ong ML, Amass L. Кластеры симптомов «красного флага» при транстиретиновой семейной амилоидной полинейропатии. J Периферийная нервная система. 2016;21:5–9.
ПабМед ПабМед Центральный Google ученый
Икеда С. Редка ли семейная амилоидная полинейропатия? Тестирование ДНК меняет представление об этом заболевании. Неврология. 2007; 69: 627–8.
ПабМед Google ученый
Ando Y, Araki S, Ando M. Транстиретин и семейная амилоидотическая полиневропатия. Интерн Мед. 1993;32:920–2.
КАС пабмед Google ученый
Андо Ю., Зур OB. Вегетативная дисфункция при семейной амилоидотической полинейропатии (САП).
 Амилоид. 1998; 5: 288–300.
Амилоид. 1998; 5: 288–300.КАС пабмед Google ученый
Андраде CA. Своеобразная форма периферической невропатии; знакомый атипичный генерализованный амилоидоз с особым поражением периферических нервов. Мозг. 1952; 75: 408–27.
КАС пабмед Google ученый
Араки С. Семейная амилоидотическая полинейропатия I типа (японский тип). Мозг Дев. 1984; 6: 128–33.
КАС пабмед Google ученый
Ando Y, Nakamura M, Araki S. Семейная амилоидотическая полинейропатия, связанная с транстиретином. Арх Нейрол. 2005;62:1057–62.
ПабМед Google ученый
Икеда С., Ханью Н., Хонго М., Йошиока Дж., Огучи Х., Янагисава Н., Кобаяши Т., Цукагоши Х., Ито Н., Йокота Т.
 Наследственный генерализованный амилоидоз с полинейропатией. Клинико-патологическое исследование 65 японских пациентов. Мозг. 1987; 110 (ч. 2): 315–37.
Наследственный генерализованный амилоидоз с полинейропатией. Клинико-патологическое исследование 65 японских пациентов. Мозг. 1987; 110 (ч. 2): 315–37.ПабМед Google ученый
Наказато М., Сиоми К., Миядзато М., Мацукура С. Семейная амилоидотическая полинейропатия I типа в Японии. Интерн Мед. 1992; 31:1335–1338.
КАС пабмед Google ученый
Sobue G, Koike H, Misu K, Hattori N, Yamamoto M, Ikeda S, Ando Y, Nakazato M, Inukai A. Клинико-патологические и генетические особенности раннего и позднего FAP типа I (FAP ATTR Val30Met) в Японии. Амилоид. 2003; 10 (Приложение 1): 32–8.
КАС пабмед Google ученый
Ямамото К., Икеда С., Ханью Н., Такеда С., Янагисава Н. Анализ родословной с минимальной систематической ошибкой подтверждения показывает ожидание семейной амилоидной полинейропатии, связанной с Met30-транстиретином.
 J Med Genet. 1998; 35: 23–30.
J Med Genet. 1998; 35: 23–30.КАС пабмед ПабМед Центральный Google ученый
Sekijima Y, Yoshida K, Tokuda T, Ikeda S. Семейный транстиретиновый амилоидоз. В: GeneReviews. Сиэтл (Вашингтон): Вашингтонский университет, Сиэтл. 1993-2017. https://www.ncbi.nlm.nih.gov/books/NBK1194/. По состоянию на 14 апреля 2017 г.
Обаяши К., Андо Ю., Накамура М., Ямасита Т., Уэда М., Хараока К., Терадзаки Х., Учино М. Спектрофотоскопия пальцевых венул в ближней инфракрасной области для оценки вегетативной дисфункции. Неврология. 2004; 63: 164–6.
КАС пабмед Google ученый
Коике Х., Морозуми С., Кавагашира Ю., Иидзима М., Ямамото М., Хаттори Н., Танака Ф., Накамура Т., Хираяма М., Андо Ю. и др. Значение синдрома запястного канала при транстиретиновой семейной амилоидной полинейропатии Val30Met.
 Амилоид. 2009 г.;16:142–8.
Амилоид. 2009 г.;16:142–8.КАС пабмед Google ученый
Икеда С. Клиническая картина и исход связанной с транстиретином семейной амилоидной полинейропатии (САП) у японских пациентов. Clin Chem Lab Med. 2002;40:1257–61.
КАС пабмед Google ученый
Maia LF, Magalhães R, Freitas J, Taipa R, Pires MM, Osório H, et al. Поражение ЦНС при транстиретиновом амилоидозе V30M: клинические, невропатологические и биохимические данные. J Neurol Нейрохирург Психиатрия. 2015;86:159–67.
ПабМед Google ученый
Секидзима Ю., Ядзаки М., Огучи К., Эдзава Н., Йошинага Т., Ямада М. и др. Церебральная амилоидная ангиопатия у посттрансплантационных пациентов с наследственным ATTR-амилоидозом. Неврология. 2016; 87: 773–81.
КАС пабмед Google ученый
">Накамура М., Ямасита Т., Уэда М., Обаяси К., Сато Т., Икеда Т., Васими Ю., Хираи Т., Кувахара Ю., Ямамото М.Т. и др. Нейрорентгенологические и клинико-патологические особенности окулолептоменингеального амилоидоза. Неврология. 2005;65:1051–6.
КАС пабмед Google ученый
Уэда М., Андо Ю., Хараока К., Кацураги С., Терасаки Ю., Сугимото М., Сунь Х., Учино М. Старение и транстиретин-связанный амилоидоз: патологические исследования при легочном амилоидозе. Амилоид. 2006; 13:24–30.
КАС пабмед Google ученый
">Mitsuhashi S, Yazaki M, Tokuda T, Sekijima Y, Washimi Y, Shimizu Y, Ando Y, Benson MD, Ikeda S. Биохимические характеристики вариантов транстиретинов, вызывающих наследственный лептоменингеальный амилоидоз. Амилоид. 2005; 12: 216–25.
КАС пабмед Google ученый
Эллиотт П., Андерссон Б., Арбустини Э., Билинска З., Чекки Ф., Чаррон П., Дюбур О., Кюль У., Майш Б., МакКенна В.Дж. и др. Классификация кардиомиопатий: заявление рабочей группы Европейского общества кардиологов по миокардиальным и перикардиальным заболеваниям. Европейское сердце J.
 2008; 29: 270–6.
2008; 29: 270–6.ПабМед Google ученый
Андо Э., Андо Ю., Окамура Р., Учино М., Андо М., Неги А. Глазные проявления семейной амилоидотической полинейропатии I типа: долгосрочное наблюдение. Бр Дж Офтальмол. 1997; 81: 295–8.
КАС пабмед ПабМед Центральный Google ученый
Lobato L, Rocha A. Транстиретиновый амилоидоз и почки. Clin J Am Soc Нефрол. 2012;7:1337–46.
ПабМед Google ученый
Beirão I, Lobato L, Costa PM, Fonseca I, Mendes P, Silva M, Bravo F, Cabrita A, Porto G. Почки и анемия при семейном амилоидозе типа I. Kidney Int. 2004;66:2004–9.
ПабМед Google ученый
Араки С., Курихара Т., Тавара С., Курибаяси Т. Семейная амилоидотическая полинейропатия на японском языке.
 В: Гленнер Г.Г., Пиньо а Коста П., де Фрейтас Ф., редакторы. Амилоид и амилоидоз. Амстердам: Excerpta Medica; 1980. с. 67–77.
В: Гленнер Г.Г., Пиньо а Коста П., де Фрейтас Ф., редакторы. Амилоид и амилоидоз. Амстердам: Excerpta Medica; 1980. с. 67–77.Coutinho P, Martins da Silva A, Lopes Lima J, Resende Barbosa A. Сорок лет опыта работы с амилоидной невропатией I типа. Рассмотрение 483 дел. В: Гленнер Г.Г., Пиньо а Коста П., де Фрейтас Ф., редакторы. Амилоид и амилоидоз. Амстердам: Excerpta Medica; 1980. с. 88–98.
Tashima K, Suhr OB, Ando Y, Holmgren G, Yamashita T, Obayashi K, Terazaki H, Uchino M. Желудочно-кишечная дисфункция при семейной амилоидотической полинейропатии (ATTR Val30Met) — сравнение шведских и японских пациентов. Амилоид. 1999;6:124–9.
КАС пабмед Google ученый
Маццео А., Руссо М., Ди Белла Г., Минутоли Ф., Станченелли С., Джентиле Л., Тоскано А., Вита Г. TTR-FAP: одноцентровый опыт на Сицилии, итальянском эндемичном районе.
 Orphanet J Rare Dis. 2015;10(Приложение 1):O1.
Orphanet J Rare Dis. 2015;10(Приложение 1):O1.Центральный пабмед Google ученый
Nakagawa M, Sekijima Y, Yazaki M, Tojo K, Yoshinaga T, Doden T, Koyama J, Yanagisawa S, Ikeda S. Туннельный синдром запястья: общий начальный симптом системного амилоидоза ATTR дикого типа (ATTRwt). Амилоид. 2016;23:58–63.
КАС пабмед Google ученый
Икегава С., Араки С., Нагата Дж., Такаба Й., Накашима А. Обзор клинических записей и терапевтических испытаний семейной амилоидотической полинейропатии - исследование 50 случаев в Кумамото (1967–1984). Ринсё Синкэйгаку 1986; 26: 175–179. [Статья на японском языке].
Икеда С. Амилоидоз сердца: гетерогенные патогенетические предпосылки. Интерн Мед. 2004;43:1107–14.
ПабМед Google ученый
">Хонго М., Хираяма Дж., Фуджи Т., Ямада Х., Окубо С., Кусама С. и др. Раннее выявление амилоидного заболевания сердца с помощью сцинтиграфии с технецием-99м-пирофосфатом: исследование семейной амилоидной полинейропатии. Ам Харт Дж. 1987;113:654–62.
КАС пабмед Google ученый
Бохари С., Кастано А., Позняков Т., Деслиль С., Латиф Ф., Маурер М.С. (99m)Tc-пирофосфатная сцинтиграфия для дифференциации амилоидоза легких цепей сердца от семейного и старческого амилоидоза сердца, связанного с транстиретином. Циркулярная кардиоваскулярная визуализация. 2013;6:195–201.
ПабМед ПабМед Центральный Google ученый
">Suhr O, Danielsson A, Holmgren G, Steen L. Недоедание и желудочно-кишечная дисфункция как прогностические факторы выживания при семейной амилоидотической полиневропатии. J Интерн Мед. 1994;235:479–85.
КАС пабмед Google ученый
Гай CD, Джонс CK. Аспирационная биопсия жировой ткани брюшной полости для подтверждения системного амилоидоза: специфичность, положительная прогностическая ценность и диагностические ошибки. Диагностика Цитопатол. 2001; 24:181–185.
КАС пабмед Google ученый
">Do Amaral B, Coelho T, Sousa A, Guimarães A. Полезность биопсии губной слюнной железы при семейной амилоидной полинейропатии португальского типа. Амилоид. 2009;16:232–238.
КАС пабмед Google ученый
Кайл Р.А., Спенсер Р.Дж., Далин, округ Колумбия. Значение ректальной биопсии в диагностике первичного системного амилоидоза. Am J Med Sci. 1966;251:501–6.
КАС пабмед Google ученый
Пикен М.М., Вестермарк П. Обнаружение и типирование амилоидов: краткое изложение текущей практики и рекомендаций группы консенсуса.
 Амилоид. 2011; 18 (Приложение 1): 48–50.
Амилоид. 2011; 18 (Приложение 1): 48–50.ПабМед Google ученый
Röcken C, Sletten K. Амилоид в хирургической патологии. Арка Вирхова. 2003; 443:3–16.
ПабМед Google ученый
Вестермарк П. Биопсия подкожной жировой ткани для исследования амилоидного белка. Методы Мол Биол. 2012; 849: 363–71.
КАС пабмед Google ученый
Бриани С, Кавалларо Т, Феррари С, Тайоли Ф, Каламелли С, Верга Л, Адами Ф, Фабрици ГМ. Спорадический транстиретиновый амилоидоз с новой мутацией гена TTR, ошибочно диагностированный как первичный амилоидоз. Дж Нейрол. 2012; 259:2226–8.
ПабМед Google ученый
Conceição I, De Carvalho M. Клиническая вариабельность семейной амилоидной полинейропатии I типа (Val30Met): сравнение поздних и ранних случаев в Португалии.
 Мышечный нерв. 2007; 35:116–8.
Мышечный нерв. 2007; 35:116–8.ПабМед Google ученый
Cowan AJ, Skinner M, Berk JL, Sloan JM, O’hara C, Seldin DC, Sanchorawala V. Макроглоссия — не всегда AL-амилоидоз. Амилоид. 2011;18:83–86.
ПабМед Google ученый
Rowczenio DM, Noor I, Gillmore JD, Lachmann HJ, Whelan C, Hawkins PN, et al. Онлайн-реестр мутаций при наследственном амилоидозе, включая рекомендации по номенклатуре. Хум Мутат. 2014; 35:E2403–12.
КАС пабмед Google ученый
Келли Дж.В. Альтернативные конформации амилоидогенных белков и пути их многостадийной сборки. Curr Opin Struct Biol. 1998; 8: 101–6.
КАС пабмед Google ученый
Rochet JC, Lansbury PT Jr. Амилоидный фибриллогенез: темы и варианты.
 Curr Opin Struct Biol. 2000;10:60–8.
Curr Opin Struct Biol. 2000;10:60–8.КАС пабмед Google ученый
Татибана Н., Токуда Т., Йошида К., Такетоми Т., Наказато М., Ли Ю.Ф., Масуда И., Икеда С. Полезность масс-спектрометрии MALDI/TOF иммунопреципитированного сывороточного варианта транстиретина в диагностике семейной амилоидной полинейропатии. Амилоид. 1999; 6: 282–8.
КАС пабмед Google ученый
Ando Y, Ohlsson PI, Suhr O, Nyhlin N, Yamashita T, Holmgren G, Danielsson A, Sandgren O, Uchino M, Ando M. Новый простой и быстрый метод скрининга вариантов амилоидоза, связанного с транстиретином. Biochem Biophys Res Commun. 1996; 228:480–3.
КАС пабмед Google ученый
Уэда М., Мисуми Ю., Мидзугути М., Накамура М., Ямасита Т., Секидзима Ю., Ота К., Шинрики С., Джоно Х.
 , Икеда С. и др. SELDI-TOF масс-спектрометрическая оценка вариантов транстиретинов для диагностики и патогенеза семейной амилоидотической полинейропатии. Клин Хим. 2009 г.;55:1223–7.
, Икеда С. и др. SELDI-TOF масс-спектрометрическая оценка вариантов транстиретинов для диагностики и патогенеза семейной амилоидотической полинейропатии. Клин Хим. 2009 г.;55:1223–7.КАС пабмед Google ученый
Тасаки М., Уэда М., Обаяси К., Койке Х., Китагава К., Оги Ю., Джоно Х., Су Ю., Суэнага Г., Осима Т. и др. Влияние возрастных и половых различий на образование амилоида транстиретина дикого типа при семейной амилоидотической полинейропатии: протеомный подход. Int J Кардиол. 2013; 170:69–74.
ПабМед Google ученый
Коннорс Л.Х., Лим А., Прокаева Т., Роскенс В.А., Костелло К.Е. Таблица вариантов человеческого транстиретина (TTR), 2003 г. Амилоид. 2003; 10: 160–84.
КАС пабмед Google ученый
Руссо А., Касвин Г., Адамс Д.
 , Кокиль С., Теаудин М., Минчева З., Мгарреш М., Лабетулль М., Барро Э. Поражение глаз при семейной амилоидной полинейропатии. J Fr Офтальмол. 2013; 36: 779–88.
, Кокиль С., Теаудин М., Минчева З., Мгарреш М., Лабетулль М., Барро Э. Поражение глаз при семейной амилоидной полинейропатии. J Fr Офтальмол. 2013; 36: 779–88.КАС пабмед Google ученый
Lobato L, Beirão I, Silva M, Bravo F, Silvestre F, Guimarães S, Sousa A, Noël LH, Sequeiros J. Семейный ATTR-амилоидоз: микроальбуминурия как предиктор симптоматического заболевания и клинической нефропатии. Трансплантация нефролового циферблата. 2003;18:532–538.
КАС Google ученый
Адамс Д., Лозерон П., Теаудин М., Минчева З., Кокиль С., Адам С., Сигнейт А., Виал С., Мэйсонобе Т., Дельмонт Э. и др. Региональные различия и сходство семейного амилоидоза с полинейропатией во Франции. Амилоид. 2012; 19 (Приложение 1): 61–4.
КАС пабмед Google ученый
">Хокинс П.Н., Андо Ю., Диспенцери А., Гонсалес-Дуарте А., Адамс Д., Сур О.Б. Развивающийся ландшафт в лечении транстиретинового амилоидоза. Энн Мед. 2015; 47: 625–38.
КАС пабмед ПабМед Центральный Google ученый
Охья Ю., Окамото С., Тасаки М., Уэда М., Джоно Х., Обаяси К., Такеда К., Окадзима Х., Асонума К., Хара Р. и др. Проявления семейной амилоидотической полинейропатии, связанной с транстиретином: длительное наблюдение за японскими пациентами после трансплантации печени. Серж сегодня. 2011;41:1211–8.

ПабМед Google ученый
Окамото С., Викснер Дж., Обаяши К., Андо Ю., Эрикзон Б.Г., Фриман С., Учино М., Сур О.Б. Трансплантация печени при семейной амилоидотической полинейропатии: влияние на выживаемость шведских пациентов. Трансплант печени. 2009; 15:1229–35.
ПабМед Google ученый
Ямамото С., Вильчек Х.Э., Новак Г., Ларссон М., Оксанен А., Ивата Т., Гьерцен Х., Содердал Г., Викстром Л., Андо Ю. и другие. Трансплантация печени при семейной амилоидотической полинейропатии (САП): одноцентровый опыт более 16 лет. Ам Джей Трансплант. 2007;7:2597–604.
КАС пабмед Google ученый
Lemos C, Coelho T, Alves-Ferreira M, Martins-da-Silva A, Sequeiros J, Mendonça D, Sousa A. Преодоление артефакта: ожидание у 284 португальских родственников с семейной амилоидной полинейропатией (FAP) ATTRV30M.
 J Neurol Нейрохирург Психиатрия. 2014; 85: 326–30.
J Neurol Нейрохирург Психиатрия. 2014; 85: 326–30.ПабМед Google ученый
Tashima K, Ando Y, Tanaka Y, Uchino M, Ando M. Изменение возраста дебюта у пациентов с семейной амилоидотической полинейропатией I типа. Intern Med. 1995;34:748–50.
КАС пабмед Google ученый
Tsuchiya A, Yazaki M, Kametani F, Takei Y, Ikeda S. Заметная регрессия амилоида брюшного жира у пациентов с семейной амилоидной полинейропатией во время длительного наблюдения после трансплантации печени. Трансплант печени. 2008; 14: 563–70.
ПабМед Google ученый
Sekijima Y. Транстиретиновый (ATTR) амилоидоз: клинический спектр, молекулярный патогенез и лечение, модифицирующее заболевание. J Neurol Нейрохирург Психиатрия. 2015;86:1036–43.
ПабМед Google ученый
">Herlenius G, Wilczek HE, Larsson M, Ericzon BG. Десятилетний международный опыт трансплантации печени при семейной амилоидотической полинейропатии: результаты из Всемирного реестра трансплантологов семейной амилоидотической полинейропатии. Трансплантация. 2004; 77: 64–71.
ПабМед Google ученый
Ямасита Т., Андо Ю., Окамото С., Мисуми Ю., Хирахара Т., Уэда М., Обаяши К., Накамура М., Джоно Х., Шоно М. и др. Отдаленная выживаемость после трансплантации печени у больных семейной амилоидной полинейропатией. Неврология. 2012; 78: 637–43.
КАС пабмед Google ученый
">Адамс Д., Сэмюэл Д., Гулон-Гоу С., Наказато М., Коста П. М., Ферай С. и др. Течение и прогностические факторы семейной амилоидной полинейропатии после трансплантации печени. Мозг. 2000; 123:1495–504.
ПабМед Google ученый
Альгаларрондо В., Антонини Т., Теудин М., Дюко Б., Лозерон П., Чемла Д. и др. Прогнозирование отдаленной выживаемости после трансплантации печени при семейном транстиретиновом амилоидозе. J Am Coll Кардиол. 2015;66:2154–6.
ПабМед Google ученый
Осима Т.
 , Кавахара С., Уэда М., Каваками Й., Танака Р., Оказаки Т., Мисуми Й., Обаяси К., Ямасита Т., Ойя Й. и др. Изменения патологоанатомических и биохимических показателей системных тканевых участков при семейной амилоидной полинейропатии спустя более 10 лет после трансплантации печени. J Neurol Нейрохирург Психиатрия. 2014;85:740–6.
, Кавахара С., Уэда М., Каваками Й., Танака Р., Оказаки Т., Мисуми Й., Обаяси К., Ямасита Т., Ойя Й. и др. Изменения патологоанатомических и биохимических показателей системных тканевых участков при семейной амилоидной полинейропатии спустя более 10 лет после трансплантации печени. J Neurol Нейрохирург Психиатрия. 2014;85:740–6.ПабМед Google ученый
Ihse E, Suhr OB, Hellman U, Westermark P. Изменение количества транстиретина дикого типа в различных типах фибрилл и тканей при ATTR-амилоидозе. J Mol Med (Берл). 2011; 89: 171–80.
КАС Google ученый
Лиепниекс Ю.Й., Бенсон МД. Прогрессирование отложения сердечного амилоида у больных наследственным транстиретиновым амилоидозом после трансплантации печени. Амилоид. 2007; 14: 277–82.
КАС пабмед Google ученый
">Sakashita N, Ando Y, Haraoka K, Terazaki H, Yamashita T, Nakamura M, Takeya M. Тяжелая застойная сердечная недостаточность с кардиальным циррозом печени через 10 лет после ортотопической трансплантации печени по поводу семейной амилоидотической полиневропатии. Патол Инт. 2006; 56: 408–12.
ПабМед Google ученый
Hara R, Kawaji T, Ando E, Ohya Y, Ando Y, Tanihara H. Влияние трансплантации печени на связанный с транстиретином глазной амилоидоз у японских пациентов. Арка Офтальмол. 2010;128:206–10.
ПабМед Google ученый
">Андо Э., Андо Ю., Хараока К. Амилоидное поражение глаз после трансплантации печени при полинейропатии. Энн Интерн Мед. 2001; 135:931–2.
КАС пабмед Google ученый
Андо Ю., Терадзаки Х., Накамура М., Андо Э., Хараока К., Ямасита Т., Уэда М., Окабе Х., Сасаки Ю., Танихара Х. и др. Другой механизм образования амилоида: de novo окулолептоменингеальные отложения амилоида после трансплантации печени. Трансплантация. 2004; 77: 345–9..
КАС пабмед Google ученый
Хараока К., Андо Ю., Андо Э., Сун Х., Накамура М., Терадзаки Х., Мисуми С., Таноуэ Ю.
 , Тадзири Т., Шоджи С. и др. Наличие варианта транстиретина в водянистой влаге пациента с семейной амилоидотической полинейропатией после трансплантации печени. Амилоид. 2002; 9: 247–51.
, Тадзири Т., Шоджи С. и др. Наличие варианта транстиретина в водянистой влаге пациента с семейной амилоидотической полинейропатией после трансплантации печени. Амилоид. 2002; 9: 247–51.ПабМед Google ученый
Sekijima Y. Недавний прогресс в понимании и лечении транстиретинового амилоидоза. Дж. Клин Фарм Тер. 2014;39: 225–33.
КАС пабмед Google ученый
Misumi Y, Narita Y, Oshima T, Ueda M, Yamashita T, Tasaki M, Obayashi K, Isono K, Inomata Y, Ando Y. Старение реципиента ускоряет приобретенный транстиретиновый амилоидоз после трансплантации печени домино. Трансплант печени. 2016;22:656–64.
ПабМед Google ученый
Sekijima Y. Недавно разработанные лекарственные препараты для семейной амилоидной полинейропатии: дифлюнизал и тафамидис.
 Мозговой нерв. 2014;66:773–781. [Статья на японском языке].
Мозговой нерв. 2014;66:773–781. [Статья на японском языке].Саид Г., Гриппон С., Киркпатрик П. Тафамидис. Nat Rev Drug Discov. 2012;11:185–186.
КАС пабмед Google ученый
Bulawa CE, Connelly S, Devit M, Wang L, Weigel C, Fleming JA, Packman J, Powers ET, Wiseman RL, Foss TR, et al. Тафамидис, мощный и селективный кинетический стабилизатор транстиретина, который ингибирует амилоидный каскад. Proc Natl Acad Sci U S A. 2012;109:9629–34.
КАС пабмед ПабМед Центральный Google ученый
Джонсон С.М., Коннелли С., Фернс С., Пауэрс Э.Т., Келли Дж.В. Транстиретиновые амилоидозы: от описания молекулярного механизма агрегации, связанного с патологией, до препарата, одобренного регулирующим органом. Дж Мол Биол. 2012; 421:185–203.
КАС пабмед ПабМед Центральный Google ученый
">Waddington Cruz M, Amass L, Keohane D, Schwartz J, Li H, Gundapaneni B. Раннее введение тафамидиса обеспечивает длительную (5,5 лет) задержку неврологического прогрессирования транстиретиновой наследственной амилоидной полинейропатии. Амилоид. 2016;23:178–83.
КАС пабмед ПабМед Центральный Google ученый
Андо Ю., Секидзима Ю., Обаяши К., Ямасита Т., Уэда М., Мисуми Ю., Морита Х., Матии К., Охта М., Таката А. и др. Влияние лечения тафамидисом на стабилизацию, эффективность и безопасность транстиретина (TTR) у японских пациентов с семейной амилоидной полинейропатией (TTR-FAP) с Val30Met и без Val30Met: фаза III, открытое исследование.
 J Neurol Sci. 2016; 362: 266–71.
J Neurol Sci. 2016; 362: 266–71.ПабМед Google ученый
Секидзима Ю., Дендл М.А., Келли Дж.В. При пероральном введении дифлунизал стабилизирует транстиретин против диссоциации, необходимой для амилоидогенеза. Амилоид. 2006; 13: 236–49..
КАС пабмед Google ученый
Tojo K, Sekijima Y, Kelly JW, Ikeda S. Diflunisal стабилизирует тетрамеры вариантов транстиретина, связанные с семейной амилоидной полинейропатией, в сыворотке против диссоциации, необходимой для амилоидогенеза. Нейроси Рес. 2006; 56: 441–9.
КАС пабмед Google ученый
Берк Д.Л., Зур О.Б., Обичи Л., Секидзима Ю., Зельденруст С.Р., Ямасита Т., Хенеган М.А., Горевич П.Д., Литчи В.Дж., Висман Д.Ф. и др. Повторное назначение дифлюнизала при семейной амилоидной полинейропатии: рандомизированное клиническое исследование.
 ДЖАМА. 2013; 310:2658–67.
ДЖАМА. 2013; 310:2658–67.КАС пабмед ПабМед Центральный Google ученый
Whelan CJ, Sattianayagam P, Dungu J, Pinney J, Gibbs S, Banypersad S, Venner C, Lachmann HJ, Wechalekar AD, Gillmore JD, et al. Переносимость терапии дифлюнизалом у больных транстиретиновым амилоидозом. На XIII Международном симпозиуме по амилоидозу. май 2012 г.; Аннотация OP 56. http://www.amyloid.nl/Files/Abstract_Book_ISA_2012.pdf. По состоянию на 21 апреля 2017 г.
Harirforoosh S, Asghar W, Jamali F. Побочные эффекты нестероидных противовоспалительных препаратов: обновленная информация о желудочно-кишечных, сердечно-сосудистых и почечных осложнениях. J Фарм Фарм Науки. 2013;16:821–47.
ПабМед Google ученый
Sekijima Y, Tojo K, Morita H, Koyama J, Ikeda S. Безопасность и эффективность длительного введения дифлюнизала при наследственном транстиретиновом (ATTR) амилоидозе.
 Амилоид. 2015;22:79–83.
Амилоид. 2015;22:79–83.КАС пабмед Google ученый
Андо Ю., Йонехара Т., Танака Ю., Ташима К., Учино М., Андо М. Ранняя имплантация кардиостимулятора у пациентов с семейной амилоидотической полинейропатией. Мышечный нерв. 1996; 19:1640–1.
КАС пабмед Google ученый
Алгаларрондо В., Динаниан С., Джуин С., Чемла Д., Беннани С.Л., Себаг С., Планте В., Ле Гулюдек Д., Сэмюэл Д., Адамс Д. и др. Профилактическая имплантация кардиостимулятора при семейной амилоидной полиневропатии. Ритм сердца. 2012;9: 1069–75.
ПабМед Google ученый
Дхармараджан К., Маурер М.С. Транстиретиновый сердечный амилоидоз у пожилых жителей Северной Америки. J Am Geriatr Soc. 2012;60:765–74.
ПабМед ПабМед Центральный Google ученый
">Планте-Борденёв В., Саид Г. Семейная амилоидная полиневропатия. Ланцет Нейрол. 2011;10:1086–97.
ПабМед Google ученый
Всемирный реестр трансплантологов семейной амилоидотической полинейропатии. http://www.fapwtr.org/ram1.htm. По состоянию на 26 апреля 2017 г.
Акерманн Э.Дж., Го С., Бутен С., Альварадо Л., Бенсон М., Хьюз С., Мониа Б.П. Клиническая разработка антисмысловой терапии для лечения транстиретин-ассоциированной полинейропатии. Амилоид. 2012;19(Приложение 1): 43–4.
КАС пабмед Google ученый
">Адамс Д., Коэльо Т., Зур О., Консейсао И., Уоддингтон-Круз М., Шмидт Х., Кампистол Дж., Пуже Дж., Буадес Дж., Берк Дж. и др. Промежуточные результаты фазы II исследования ALN-TTR02, нового терапевтического средства с РНК-интерференцией для лечения семейной амилоидотической полинейропатии. На двухгодичном собрании Общества периферических нервов, Сен-Мало, Франция. 29июнь – 3 июля 2013 г. www.alnylam.com/capella/presentations/aln-ttr02phiidata/. По состоянию на 21 апреля 2017 г.
Циммерманн Т., Карстен В., Харроп Дж., Чан А., Кьеза Дж., Петерс Г., Фальцоне Р., Цехелски Дж., Ночур С., Вайшнав А. и др. Фаза I первого испытания на людях ALN-TTRsc, нового терапевтического средства с интерференцией РНК для лечения семейной амилоидотической кардиомиопатии (FAC).
 Ошибка J Card 2013; 19: S66–S66.
Ошибка J Card 2013; 19: S66–S66.Google ученый
Кардосу И., Мартинс Д., Рибейро Т., Мерлини Г., Сарайва М.Дж. Синергизм комбинированного лечения доксициклином / TUDCA в снижении отложения транстиретина и связанных с ним биомаркеров: исследования на моделях мышей FAP. J Transl Med. 2010;8:74.
ПабМед ПабМед Центральный Google ученый
Хосой А., Су Ю., Торикай М., Джоно Х., Исикава Д., Соэдзима К., Хигучи Х., Го Дж., Уэда М., Суэнага Г. и др. Новое антитело для лечения транстиретинового амилоидоза. Дж. Биол. Хим. 2016;291:25096–105.
КАС пабмед ПабМед Центральный Google ученый
Икеда С., Наказато М., Андо Ю., Собуэ Г. Семейная транстиретиновая амилоидная полинейропатия в Японии: клиническая и генетическая гетерогенность.
 Неврология. 2002;58:1001–7.
Неврология. 2002;58:1001–7.КАС пабмед Google ученый
Медицинский факультет (неврология и ревматология), Медицинский факультет Университета Синсю, Мацумото, Япония
Yoshiki Sekijima
Кафедра неврологии, Высшая школа медицинских наук, Университет Кумамото, 1-1-1 Honjo, Chuo-ku, Kumamoto-shi, Kumamoto, 860-8556, Japan
Mitsuharu Ueda & Yukio Ando
Кафедра неврологии Высшей школы медицины Университета Нагоя, Нагоя, Япония
Харуки Койке
Кафедра неврологии Высшей школы медицины Университета Тиба, Тиба, Япония
Sonoko Misawa
Pfizer Japan Inc., Tokyo, Japan
Tomonori Ishii
- Yoshiki Sekijima
Посмотреть автора19 по этому автору также можно найти 604
PubMed Google Scholar - Mitsuharu Ueda
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Харуки Койке
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Sonoko Misawa
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Tomonori Ishii
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Юкио Андо
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
9 9 9 9 9 9 9669 9669669 9 9 9 9669 966 9 ,tab::ODERKTableau) Вычисляет функцию устойчивости по таблице с координатами z . Стабильный, если <1.
Стабильный, если <1.
\[r(z) = 1 + z bᵀ(I - zA)⁻¹ e\]
, где e обозначает вектор из единиц.
stable_region(tab::ODERKTableau; initial_guess=-3.0)
Вычисляет длину области стабильности на действительной оси.
OrdinaryDiffEq.ODE_DEFAULT_TABLEAU — Константа ODE DEFAULT TABLEAU
Задает таблицу по умолчанию для решателя ODE. В настоящее время Дорманд-Принц 4/5.
DiffEqDevTools.constructEuler — Функция Метод Эйлера.
DiffEqDevTools.constructRalston — Функция Метод порядка 2 Ральстона.
DiffEqDevTools.constructHeun — Функция Метод Heun's Order 2.
DiffEqDevTools.constructKutta3 — Функция Метод порядка 3 Кутты.
Отсутствует строка документации для OrdinaryDiffEq.constructBS3 . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructBogakiShampine3 — Функция buildBogakiShampine3()
Создает табличный объект для метода Bogakai-Shampine Order 2/3.
DiffEqDevTools.constructRK4 — Функция Классический метод RK4.
DiffEqDevTools.constructRK438Rule — Функция Классический метод правила RK4 3/8.
DiffEqDevTools.constructRKF4 — Функция Метод Рунге-Кутта-Фехберга Порядок 4/3
DiffEqDevTools.constructRKF5 — Функция Метод Рунге-Кутта-Фельберга Порядок 4/5.
DiffEqDevTools.constructCashKarp — ФункцияstructCashKarp()
Создает объект-таблицу для метода Cash-Karp Order 4/5.
Отсутствует строка документации для DiffEqDevTools.constructDormandPrince . Подробности смотрите в журнале сборки Documenter.
Отсутствует строка документации для OrdinaryDiffEq.constructBS5 . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructPapakostasPapaGeorgiou5 — Функция S.N. Папакостас и Г. Папа Джорджиу более высокая ошибка более стабильная
Семейство пар Рунге-Кутта пятого порядка, С. Н. Папакостас и Г. Папа Джорджиу, Математика вычислений, том 65, номер 215, 19 июля.96, страницы 1165-1181.
Н. Папакостас и Г. Папа Джорджиу, Математика вычислений, том 65, номер 215, 19 июля.96, страницы 1165-1181.
DiffEqDevTools.constructPapakostasPapaGeorgiou52 — Функция S.N. Папакостас и Г. Папа Джорджиу Менее стабильная нижняя ошибка Строго лучше, чем DP5
Семейство пар Рунге-Кутта пятого порядка, С.Н. Папакостас и Г. Папа Джорджиу, Математика вычислений, том 65, номер 215, июль 1996 г., страницы 1165–1181.
DiffEqDevTools.constructTsitouras5 — Функция Пары Рунге–Кутты порядка 5(4) с использованием минимального набора упрощающих предположений по гл. Цитоурас, TEI Халкиды, кафедра прикладных наук, GR34400, Псана, Греция.
DiffEqDevTools.constructLutherKonen5 — Функция Первый порядок Лютера и Конена 5 Некоторые классические формулы Рунге-Кутты пятого порядка, H.A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558.
DiffEqDevTools.constructLutherKonen52 — Функция Второй порядок Лютера и Конена 5 Некоторые классические формулы Рунге-Кутты пятого порядка, H. A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558.
A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558.
DiffEqDevTools.construct Лютер Конен53 - Функция Третий порядок Лютера и Конена 5 Некоторые классические формулы Рунге Кутты пятого порядка, H.A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558.
Diffeqdevtools.construngefirst5 - Функция Рунге первого порядка 5 Метод
Diffeqdevtools.constructlawson5 - Функция Схема 5th Order Lawson. Анализ, Том. 3, № 4, (19 декабря66) стр. 593-597
DiffEqDevTools.constructSharpSmart5 — Функция Явные пары Рунге-Кутты с вычислением производной на одну больше, чем минимум, P.W.Sharp и E.Smart, Siam Journal of Scientific Computing, Vol. 14, № 2, с. 338-348, март 1993 г.
DiffEqDevTools.constructBogakiShampine5 — Функция Эффективная пара Рунге-Кутта (4,5) П.Богацки и Л.Ф.Шампайн Computers and Mathematics with Applications, Vol. 32, № 6, 1996, страницы с 15 по 28
32, № 6, 1996, страницы с 15 по 28
DiffEqDevTools.constructCassity5 — Функция Метод Cassity's Order 5
DiffEqDevTools.constructButcher6 — Функция Метод мясника First Order 6 . 4, (1964), страницы со 179 по 194
DiffEqDevTools.constructButcher62 — Функция Второй порядок мясника 6, метод
О процессах Рунге-Кутты высокого порядка, Дж. К. Батчер, Журнал Австралийского математического общества, Vol. 4, (1964), страницы с 179 по 194
DiffEqDevTools.constructButcher63 — Function Третий порядок Мясника 6
О процессах Рунге-Кутты высокого порядка, JC Butcher, Journal of the Australian Mathematical Society, Vol. 4, (1964), страницы с 179 по 194
Об оптимизации некоторых восьмиэтапных явных методов Рунге-Кутты шестого порядка, М. Танака, К. Касуга, С. Ямасита и Х. Язаки, Журнал Японского общества обработки информации, Vol. 34, № 1 (1993), страницы 62–74. , К. Касуга, С. Ямасита и Х. Ядзаки, Журнал Японского общества обработки информации, Vol. 34, № 1 (1993), страницы с 62 по 74.
34, № 1 (1993), страницы с 62 по 74.
DiffEqDevTools.constructTanakaKasugaYamasitaYazaki6C — Function buildTanakaKasugaYamasitaYazaki Order 6 C
Об оптимизации некоторых восьмиэтапных явных методов Рунге-Кутты шестого порядка, М. Касуга Танака , Ямасита и Х. Ядзаки, Журнал Общества обработки информации Японии, Vol. 34, № 1 (1993), страницы 62–74.0419
Об оптимизации некоторых восьмиэтапных явных методов Рунге-Кутты шестого порядка, М. Танака, К. Касуга, С. Ямасита и Х. Язаки, Журнал Японского общества обработки информации, Vol. 34, No. 1 (1993), страницы 62–74. премьер-министр, Антон Хута, Acta Fac. Нац. ун-т Коменская математика, Vol. 1, стр. 201-224 (1956).
DiffEqDevTools.constructHuta62 — Функция Метод Антона Хутаса второго порядка 6
Усовершенствование метода Рунге-Кутта-Нистрём для числового разрешения различных уравнений первого порядка, Fac Huta. Нац. ун-т Коменская математика, Vol. 1, страницы 201-224 (1956).
DiffEqDevTools. constructVerner6
constructVerner6 — Функция Метод Verner Order 5/6
Сравнение новой пары RK56 с DP56, Джим Вернер, факультет математики. Университет Саймона Фрейзера, Бернаби, Канада, 2006 г.
DiffEqDevTools.constructDormandPrince6 — Функция Дорманд-Принц Метод порядка 5//6
П. Дж. Принс и Дж. Р. Дорманд, Встроенные формулы Рунге-Кутты высокого порядка, Журнал вычислительной и прикладной математики. 7 (1981), стр. 67-75.
DiffEqDevTools.constructSharpVerner6 — Функция Метод Шарпа-Вернера порядка 5/6
Полностью вложенные пары Рунге-Кутта, П. В. Шарп и Дж. Х. Вернер, SIAM Journal on Numerical Analysis, Vol. 31, № 4. (19 авг.94), стр. с 1169 по 1190.
Отсутствует строка документации для DiffEqDevTools.constructVern6 . Подробности смотрите в журнале сборки Documenter.
DiffeQdevtools.constructclassicverner6 -Функция Явные методы Runge-Kutfa с оценками локальной ошибки усечения
DiffeQdevtools. constructchummund6
constructchummund6 -Функция СЕССИОНСКОЙ СЕМЕРС. порядка 6, Г. М. Чаммуд (Хаммуд), Численные методы и программирование, 2001 г., том 2, 2001 г., стр. 159.-166 (журнал Advanced Computing Scientific, издаваемый НИЦ МГУ им. М.В. Ломоносова)
DiffEqDevTools.constructChummund62 — Функция Метод Чумунда второго порядка 6
Трехмерное семейство семишаговых методов Рунге-Кутты приказ 6, Г. М. Чамуд (Хаммуд), Численные методы и программирование, 2001, Том 2, 2001, страницы 159-166 (Научный журнал Advanced Computing, издаваемый Научно-исследовательским вычислительным центром МГУ им. М.В. Ломоносова)
DiffEqDevTools.constructPapakostas6 — Функция Приказ Папакостаса 6
О подобранных по фазам модифицированных парах Рунге-Кутта порядка 6(5), по гл. Цитурас и И.Т. Famelis, Международная конференция по численному анализу и прикладной математике, Крит, (2006)
DiffEqDevTools.constructLawson6 — Функция Приказ Лоусона 6
Процесс Рунге-Кутты порядка 6 с расширенной областью стабильности, Дж. Д. Лоусон, Siam Journal по численному анализу, Vol. 4, № 4 (19 декабря67) стр. 620-625.
Д. Лоусон, Siam Journal по численному анализу, Vol. 4, № 4 (19 декабря67) стр. 620-625.
DiffEqDevTools.constructTsitourasPapakostas6 — Функция Приказ Цитураса-Папакостаса 6
Дешевая оценка погрешности для методов Рунге-Кутты, по гл. Цитурас и С.Н. Папакостас, Siam Journal on Scientific Computing, Vol. 20, Issue 6, Nov 1999.
DiffEqDevTools.constructDormandLockyerMcCorriganPrince6 — Function DormandLockyerMcCorriganPrince Order 6 Global Error Estimation
Global Error estimation with Runge-Kutta triples, by J.R.Dormand, M.A.Lockyer, N.E.McCorrigan and P.J.Prince, Computers and Mathematics с приложениями, 18 (1989) стр. 835-846.
DiffEqDevTools.constructVernerEfficient6 — Function From Verner's Website
DiffEqDevTools.constructMikkawyEisa — Function Mikkawy-Eisa Order 6
A general four-parameter non-FSAL embedded Runge–Kutta algorithm of orders 6 and 4 in seven stages, М. Е.А. Эль-Миккави и М.М.М. Эйса, Прикладная математика и вычисления, Vol. 143, № 2, (2003) страницы 259–267.
Е.А. Эль-Миккави и М.М.М. Эйса, Прикладная математика и вычисления, Vol. 143, № 2, (2003) страницы 259–267.
DiffEqDevTools.constructVernerEfficient7 — Функция с веб-сайта Verner's
DiffeQdevtools.constructclassicverner7 -Функция Явные методы Runge-Kutfa с оценками локального усечения
Diffeqdevtools.constrctsharpverner7 -Функция. по численному анализу, Vol.31, No.4. (Август 1994 г.) страницы 1169-1190.
DiffEqDevTools.constructTanakaYamasitaStable7 — Функция Об оптимизации некоторых девятиэтапных методов Рунге-Кутты седьмого порядка, М. Танака, С. Мурамацу и С. Ямасита, Общество обработки информации Японии, Vol. 33, № 12 (1992) страницы 1512-1526.
DiffEqDevTools.constructSharpSmart7 — Функция Явные пары Рунге-Кутты с вычислением производной на одну больше, чем минимум, авторы P.W.Sharp и E.Smart, Siam Journal of Scientific Computing, Vol. 14, № 2, с. 338-348, март 1993 г.
DiffEqDevTools. constructTanakaYamasitaEfficient7
constructTanakaYamasitaEfficient7 — Функция Об оптимизации некоторых девятиэтапных методов Рунге-Кутты седьмого порядка, М. Танака, С. Мурамацу и С. Ямасита, Общество обработки информации Японии , Том. 33, № 12 (1992) страницы 1512-1526.
DiffEqDevTools.constructVernerRobust7 — Функция С веб-сайта Вернера
Отсутствует строка документации для OrdinaryDiffEq.constructTanYam7 . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructEnrightVerner7 — Функция Относительная эффективность альтернативных схем контроля дефектов для непрерывных формул Рунге-Кутты высокого порядка WH Enright Журнал SIAM по численному анализу, Vol. 30, № 5. (19 окт.93), стр. 1419-1445.
DiffEqDevTools.constructDormandPrince8 — Функция buildDormandPrice8()
Создает объект таблицы для метода Приказ Дорманд-Принс 6/8.
DiffEqDevTools.constructRKF8 — ФункцияstructRKF8()
Создает табличный объект для метода Рунге-Кутта-Фельберга порядка 7/8.
DiffEqDevTools.constructCooperVerner8 — Функция Некоторые явные методы Рунге-Кутты высокого порядка, Г. Дж. Купер и Дж. Х. Вернер, SIAM Journal on Numerical Analysis, Vol. 9, № 3, (сентябрь 1972 г.), страницы с 389 по 405
DiffEqDevTools.constructCooperVerner82 - Функция Некоторые явные методы Рунге-Кутты высокого порядка, Г. Дж. Купер и Дж. Х. Вернер, SIAM Journal on Numerical Analysis, Vol. 9, № 3 (сентябрь 1972 г.), страницы с 389 по 405
DiffEqDevTools.constructTsitourasPapakostas8 — Функция Дешевая оценка погрешности для методов Рунге-Кутты, гл. Цитурас и С.Н. Папакостас, Siam Journal on Scientific Computing, Vol. 20, выпуск 6, 19 ноября99.
DiffEqDevTools.constructEnrightVerner8 — Функция Относительная эффективность альтернативных схем контроля дефектов для непрерывных формул Рунге-Кутты высокого порядка WH Enright SIAM Journal on Numerical Analysis, Vol. 30, № 5 (октябрь 1993 г.), стр. 1419-1445.
DiffEqDevTools.constructdverk78 — Функция «Клен» Джима Вернера (dverk78)
DiffEqDevTools.constructClassicVerner8 — Функция ЯВНЫЙ МЕТОД РУНГА-КУТФА С ОЦЕНКАМИ LOCAL TRUNC0419 DiffEqDevTools.constructDormandPrince8_64bit — Функция
buildDormandPrice8_64bit()
Создает табличный объект для метода Дорманд-Принц Орден 6/8 с аппроксимированными коэффициентами из статьи. Это работает до 64-битной точности.
DiffEqDevTools.constructCurtis8 — Функция Процесс Рунге-Кутты восьмого порядка с одиннадцатью вычислениями функций на шаг, А. Р. Кертис, Numerische Mathematik, Vol. 16, № 3 (1970), страницы 268–277
Отсутствует строка документации для OrdinaryDiffEq.constructTsitPap8 . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructSharp9 — Function Journal of Applied Mathematics & Decision Sciences, 4(2), 183-192 (2000), «Явные пары Рунге-Кутты высокого порядка для эфемерид Солнечной системы и Луны».
DiffEqDevTools.constructTsitouras9 — Функция Оптимизированные явные пары Рунге-Кутта порядка 9(8), по гл. Цитоурас, Прикладная вычислительная математика, 38 (2001) 123-134.
DiffEqDevTools.constructTsitouras92 — Функция Оптимизированные явные пары Рунге-Кутта порядка 9(8), по гл. Цитоурас, Прикладная вычислительная математика, 38 (2001) 123-134.
DiffEqDevTools.constructVernerEfficient9 — Функция Из веб-сайта Verner
Отсутствует строка документации для OrdinaryDiffEq.constructVern9 . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructVerner916 — Функция Вернер 1991 Первый порядок 5/6 метод
Некоторые пары формул Руге-Кутты, Дж. Х. Вернер, SIAM Journal on Numerical Analysis, Vol. 28, № 2 (апрель 1991 г.), страницы 496–511. , Том. 28, № 2 (апрель 1991 г.), страницы с 496 по 511.0007 — Функция
Feagin10 в форме таблицы
Отсутствует строка документации для DiffEqDevTools. constructFeagin10Tableau
constructFeagin10Tableau . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructOno10 — Функция Ono10
DiffEqDevTools.constructCurtis10 — Функция Явные формулы Рунге-Кутты высокого порядка, их использование и ограничения, A.R.Curtis, J. Inst. Математические приложения (1975) 16, 35-55.
DiffEqDevTools.constructHairer10 — Функция Метод Рунге-Кутты порядка 10, E. Hairer, J. Inst. Математические приложения (1978) 21, 47–59.
DiffEqDevTools.constructBaker10 — Функция Том Бейкер, Университет Тисайда. Часть RK-Aid http://www.scm.tees.ac.uk/users/u0000251/research/researcht.htm http://www.scm.tees.ac.uk/users/u0000251/j.r.dormand/t .baker/rk10921m/rk10921m
DiffEqDevTools.constructFeagin12 — Функция Табличная форма Feagin12
DiffEqDevTools.constructOno12 — Функция На 25 этапе явный метод Рунге-Кутты 12-го порядка Хироши Оно. Труды Японского общества промышленной и прикладной математики, Vol. 6, № 3, (2006) страницы 177–186
6, № 3, (2006) страницы 177–186
Отсутствует строка документации для DiffEqDevTools.constructFeagin12Tableau . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructFeagin14 — Функция Табличная форма Feagin14
Отсутствует строка документации для DiffEqDevTools.constructFeagin14Tableau . Подробности смотрите в журнале сборки Documenter.
DiffEqDevTools.constructImplicitEuler — Function Implicit Euler Method
DiffEqDevTools.constructMidpointRule — Function Order 2 Midpoint Method
DiffEqDevTools.constructTrapezoidalRule — Function Order 2 Trapezoidal Rule (LobattoIIIA2)
DiffEqDevTools.constructLobattoIIIA4 — Function LobattoIIIA Порядок 4, метод
DiffEqDevTools.constructLobattoIIIB2 — Функция LobattoIIIB Порядок 2, метод
DiffEqDevTools.constructLobattoIIIB4 — Function LobattoIIIB Order 4 method
DiffEqDevTools. constructLobattoIIIC2
constructLobattoIIIC2 — Function LobattoIIIC Order 2 method
DiffEqDevTools.constructLobattoIIIC4 — Function LobattoIIIC Order 4 method
DiffEqDevTools.constructLobattoIIICStar2 — Function LobattoIIIC* Заказ 2, метод
DiffEqDevTools.constructLobattoIIICStar4 — Функция LobattoIIIC* Заказ 4, метод
DiffEqDevTools.constructLobattoIIID2 — Function LobattoIIID Order 2 method
DiffEqDevTools.constructLobattoIIID4 — Function LobattoIIID Order 4 method
DiffEqDevTools.constructGL2 — Function Gauss-Legendre Order 2.
DiffEqDevTools.constructGL4 — Function Порядок Гаусса-Лежандра 4.
DiffEqDevTools.constructGL6 — Функция Порядок Гаусса-Лежандра 6.
DiffEqDevTools.constructRadauIA3 — Function RadauIA Order 3 method
DiffEqDevTools.constructRadauIA5 — Function RadauIA Order 5 method
DiffEqDevTools. constructRadauIIA3
constructRadauIIA3 — Function RadauIIA Order 3 method
DiffEqDevTools.constructRadauIIA5 — Function RadauIIA Order 5 method
Humanization анти-CEA антитела T84.66 на основе данных о кристаллической структуре | Белковая инженерия, дизайн и отбор
Журнальная статья
Пол Дж. Язаки,
Пол Дж. Ядзаки
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Марк А. Шерман,
Марк А. Шерман
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Джон Э. Шивли,
Джон Э. Шивли
Шивли
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Дэвид Икл,
Дэвид Икл
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Лоуренс Э. Уильямс,
Лоуренс Э. Уильямс
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Джеффри Ю.К. Вонг,
Джеффри Ю.К. Вонг
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Дэвид Колчер,
Дэвид Колчер
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Анна М. Ву,
Ву,
Анна М. Ву
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Эндрю А. Раубичек
Эндрю А. Раубичек
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Белковая инженерия, дизайн и отбор , том 17, выпуск 5, май 2004 г., страницы 481–489, https://doi.org/10.1093/protein/gzh056
Опубликовано:
17 августа 2004 г.
История статьи
Получено:
09 апреля 2004 г.
Принято:
03 июня 2004 г.
Опубликовано:
17 августа 2004 г.
Фильтр поиска панели навигации
Protein Engineering, Design and SelectionЭтот выпускProteinsBooksJournalsOxford Academic
Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации
Protein Engineering, Design and SelectionЭтот выпускProteinsBooksJournalsOxford Academic
Термин поиска на микросайте
Advanced Search
Abstract
Химерное T84. 66 (cT84.66) представляет собой моноклональное антитело (мАт) с высокой специфичностью и аффинностью к опухолеассоциированному карциноэмбриональному антигену (СЕА). Радиоактивно-меченый cT84.66 продемонстрировал полезность в клинике в качестве реагента для радиоиммуносцинтиграфии и радиоиммунотерапии СЕА-положительных колоректальных опухолей и злокачественных новообразований молочной железы. Для увеличения терапевтической эффективности T84.66 использовали гуманизацию путем прививки определяющей комплементарность области (CDR). Прививка CDR является хорошо зарекомендовавшим себя методом, хотя часто для восстановления высокой аффинности требуется серия обратных мутаций каркаса. Недавно была определена кристаллическая структура диатела T84.66 (димер scFv), полученного из мышиного mAb T84.66, что облегчило процесс гуманизации благодаря наличию данных о кристаллической структуре как донора, так и акцептора трансплантата. Поиск в Protein Data Bank выявил близкое структурное сходство (среднеквадратичное отклонение 1,07 Å) между Fv T84.
66 (cT84.66) представляет собой моноклональное антитело (мАт) с высокой специфичностью и аффинностью к опухолеассоциированному карциноэмбриональному антигену (СЕА). Радиоактивно-меченый cT84.66 продемонстрировал полезность в клинике в качестве реагента для радиоиммуносцинтиграфии и радиоиммунотерапии СЕА-положительных колоректальных опухолей и злокачественных новообразований молочной железы. Для увеличения терапевтической эффективности T84.66 использовали гуманизацию путем прививки определяющей комплементарность области (CDR). Прививка CDR является хорошо зарекомендовавшим себя методом, хотя часто для восстановления высокой аффинности требуется серия обратных мутаций каркаса. Недавно была определена кристаллическая структура диатела T84.66 (димер scFv), полученного из мышиного mAb T84.66, что облегчило процесс гуманизации благодаря наличию данных о кристаллической структуре как донора, так и акцептора трансплантата. Поиск в Protein Data Bank выявил близкое структурное сходство (среднеквадратичное отклонение 1,07 Å) между Fv T84. 66 и Fv 4D5v8, гуманизированного анти-p185 9.Антитело 1121 HER2 , продаваемое как Герцептин® (трастузумаб). Это привело к двум гуманизированным версиям mAb M5A и M5B T84.66, которые различались только количеством мышиных остатков, присутствующих в C-концевой половине CDR-h3. Для оценки гуманизированных mAb были проведены биохимический анализ и исследования биораспределения на животных. мАт M5A, M5B и cT84.66 проявляли субнаномолярное сродство к СЕА, а в качестве радиоактивно меченых мАт обнаруживали специфическую локализацию в опухоли у мышей с опухолями. мАт T84.66 M5A было выбрано для клинической разработки из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и было переименовано в hT84.66. Ограниченное производство и исследование изображений на животных продемонстрировали способность hT84.66 поддерживать клинические испытания. Запланированные клинические испытания определят эффективное использование этого структурного подхода при разработке многообещающего нового терапевтического средства.
66 и Fv 4D5v8, гуманизированного анти-p185 9.Антитело 1121 HER2 , продаваемое как Герцептин® (трастузумаб). Это привело к двум гуманизированным версиям mAb M5A и M5B T84.66, которые различались только количеством мышиных остатков, присутствующих в C-концевой половине CDR-h3. Для оценки гуманизированных mAb были проведены биохимический анализ и исследования биораспределения на животных. мАт M5A, M5B и cT84.66 проявляли субнаномолярное сродство к СЕА, а в качестве радиоактивно меченых мАт обнаруживали специфическую локализацию в опухоли у мышей с опухолями. мАт T84.66 M5A было выбрано для клинической разработки из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и было переименовано в hT84.66. Ограниченное производство и исследование изображений на животных продемонстрировали способность hT84.66 поддерживать клинические испытания. Запланированные клинические испытания определят эффективное использование этого структурного подхода при разработке многообещающего нового терапевтического средства.
Под редакцией Hennie Hoogenboom
Введение
Ключевой проблемой in vivo терапевтического применения моноклональных антител (мАт) была реакция иммунной системы человека на ксеногенные антитела. Клинические исследования с мышиными моноклональными антителами показали эффективное нацеливание на опухоль, но привели к быстрому выведению мышиных антител при последующих дозах из-за генерирования иммунного ответа человеческого антимышиного антитела (HAMA) (Schroff, 1985; Shawler, 19).85). Рекомбинантные методологии позволили создать химерные mAb человека и мыши, которые имеют более низкую частоту иммунологического ответа, но не устранили проблему. Современное поколение гуманизированных mAb, одобренных для терапии, является результатом прививки CDR мышиного происхождения на каркас человеческого антитела (Jones, 1986; Low, 1996). Новые технологические достижения, позволяющие генерировать антитела человека из библиотек фагового дисплея иммуноглобулинов человека (Winter, 1994) или трансгенных животных (Bruggemann, 1991; Mendez, 19). 97) проходят текущую клиническую оценку.
97) проходят текущую клиническую оценку.
T84.66 представляет собой mAb мыши с высокой специфичностью и аффинностью к карциноэмбриональному антигену (CEA), хорошо охарактеризованному антигену, ассоциированному с опухолью человека (Wagener, 1983). Т84.66 с радиоактивной меткой, оцененный в клинике, смог визуализировать 69% первичных колоректальных карцином до операции (Beatty, 1986), но наблюдался ответ НАМА (Morton, 1988). Гены для T84.66 были клонированы, и химерная версия человека и мыши (cT84.66) была экспрессирована в клетках млекопитающих (Neumaier, 19).90). В экспериментальном исследовании визуализации колоректального заболевания с однократным введением только у 1 из 29 пациентов наблюдался ответ человеческих антител против химерных антител (Wong, 1997). Однако по мере того, как продолжались испытания радиоиммунотерапии с многократным введением (Wong, 1995, 1999), было отмечено увеличение частоты ответа НАСА.
При сосредоточении внимания на снижении иммунного ответа ключевым требованием было сохранение высокой специфичности и аффинности исходного mAb T84. 66. Это препятствовало выбору совершенно нового mAb из библиотек фагового дисплея генов иммуноглобулинов человека или трансгенных животных. Таким образом, проводилась гуманизация путем прививки мышиных CDR на Fv-каркас человека. В опубликованной литературе имеется множество примеров гуманизации антител с помощью прививки CDR (O'Brien, 2003). Однако часто наблюдалась существенная потеря аффинности связывания антигена из-за стерических столкновений между человеческим каркасом и остатками CDR мыши, которые изменяли конформацию антигенсвязывающих петель. Эти непредвиденные столкновения являются результатом использования молекулярных моделей для разработки трансплантата, а не реальных кристаллических структур молекул донора и акцептора трансплантата. Часто требуется трудоемкий и часто случайный повторяющийся процесс введения обратных мутаций для восстановления ключевых остатков мышиного каркаса, ответственных за поддержание правильной конформации петли (Foote, 19).92).
66. Это препятствовало выбору совершенно нового mAb из библиотек фагового дисплея генов иммуноглобулинов человека или трансгенных животных. Таким образом, проводилась гуманизация путем прививки мышиных CDR на Fv-каркас человека. В опубликованной литературе имеется множество примеров гуманизации антител с помощью прививки CDR (O'Brien, 2003). Однако часто наблюдалась существенная потеря аффинности связывания антигена из-за стерических столкновений между человеческим каркасом и остатками CDR мыши, которые изменяли конформацию антигенсвязывающих петель. Эти непредвиденные столкновения являются результатом использования молекулярных моделей для разработки трансплантата, а не реальных кристаллических структур молекул донора и акцептора трансплантата. Часто требуется трудоемкий и часто случайный повторяющийся процесс введения обратных мутаций для восстановления ключевых остатков мышиного каркаса, ответственных за поддержание правильной конформации петли (Foote, 19).92).
Недавно кристаллическая структура вариабельной области мышиного T84. 66 была решена с помощью рентгеноструктурного анализа диатела T84.66 (димер scFv) с разрешением 2,6 Å (Carmichael, 2003). Поиск в банке белковых данных выявил близкое структурное сходство с 4D5v8, гуманизированным антителом против p185 HER2 , продаваемым как Герцептин® (трастузумаб). Компьютерная графическая визуализация наложенных структур позволила сделать рациональный выбор сплайс-соединений трансплантатов и обратных мутаций каркаса. Путем прививки CDR были созданы две версии: mAb T84.66 M5A и mAb T84.66 M5B. Они различались только количеством мышиных остатков, присутствующих в С-концевой половине CDR-h3. Биохимические исследования и исследования биораспределения на животных использовали для сравнения гуманизированных mAb с химерной версией. Все mAb M5A, M5B и cT84.66 имели схожую субнаномолярную аффинность к СЕА и, будучи радиоактивно мечеными мАт, проявляли специфическую локализацию в опухоли у бестимусных мышей, несущих ксенотрансплантаты опухоли с положительным результатом на СЕА.
66 была решена с помощью рентгеноструктурного анализа диатела T84.66 (димер scFv) с разрешением 2,6 Å (Carmichael, 2003). Поиск в банке белковых данных выявил близкое структурное сходство с 4D5v8, гуманизированным антителом против p185 HER2 , продаваемым как Герцептин® (трастузумаб). Компьютерная графическая визуализация наложенных структур позволила сделать рациональный выбор сплайс-соединений трансплантатов и обратных мутаций каркаса. Путем прививки CDR были созданы две версии: mAb T84.66 M5A и mAb T84.66 M5B. Они различались только количеством мышиных остатков, присутствующих в С-концевой половине CDR-h3. Биохимические исследования и исследования биораспределения на животных использовали для сравнения гуманизированных mAb с химерной версией. Все mAb M5A, M5B и cT84.66 имели схожую субнаномолярную аффинность к СЕА и, будучи радиоактивно мечеными мАт, проявляли специфическую локализацию в опухоли у бестимусных мышей, несущих ксенотрансплантаты опухоли с положительным результатом на СЕА. T84.66 M5A был выбран для доклинического производства из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и был переименован в mAb hT84.66. Было проведено масштабное производство, чтобы продемонстрировать способность этого клона поддерживать клинические испытания. Запланированные клинические испытания определят эффективность использования этого структурного подхода.
T84.66 M5A был выбран для доклинического производства из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и был переименован в mAb hT84.66. Было проведено масштабное производство, чтобы продемонстрировать способность этого клона поддерживать клинические испытания. Запланированные клинические испытания определят эффективность использования этого структурного подхода.
Материалы и методы
Гуманизация дизайна
Используя технологию молекулярной графики, рентгеновские координаты для одной единицы T84.66 Fv были извлечены из набора координат соответствующей структуры диатела (файл PDB 1MOE). Затем набор координат Fv был представлен в VAST (Gibrat, 1996), сетевом сервере структурного выравнивания по методу наименьших квадратов, чтобы идентифицировать человеческий или гуманизированный Fv, каркас которого будет служить подходящим акцептором для предлагаемого трансплантата CDR. Из 20 антител, появившихся в списке гомологичных структур, пять были выбраны для дальнейшего рассмотрения на основании их высокой степени перекрытия альфа-углерода с запрашиваемой структурой (среднеквадратическое среднеквадратичное отклонение от 1,00 до 1,25 Å). Затем были идентифицированы остатки, определяющие каркасные области по Кабату, и они были наложены на атомы каркаса исследуемой структуры (1312 атомов), в результате чего было получено среднеквадратичное отклонение. значения 1,00 Å (файл PDB1CZ8), 1,00 Å (2FGW), 1,06 Å (1AD9), 1,06 Å (1FVC) и 1,06 Å (1BJ1). Учитывая близость этих значений, в качестве второго фактора скрининга рассчитывали процентную идентичность последовательностей (общую и только каркасную). Полученные значения для 1CZ8 (в целом 63%, каркас 54%), 2FGW (61% и 54%), 1AD9 (65% и 60%), 1FVC (67% и 61%) и 1BJ1 (63% и 53%). %), предположили, что 1FVC [гуманизированное антитело 4D5, версия 8, анти-p185 HER2 , герцептин трастузумаб, (Eigenbrot, 1993)] является наиболее подходящим источником каркаса, поскольку степень перекрытия и процент идентичности последовательностей были высокими.
Из 20 антител, появившихся в списке гомологичных структур, пять были выбраны для дальнейшего рассмотрения на основании их высокой степени перекрытия альфа-углерода с запрашиваемой структурой (среднеквадратическое среднеквадратичное отклонение от 1,00 до 1,25 Å). Затем были идентифицированы остатки, определяющие каркасные области по Кабату, и они были наложены на атомы каркаса исследуемой структуры (1312 атомов), в результате чего было получено среднеквадратичное отклонение. значения 1,00 Å (файл PDB1CZ8), 1,00 Å (2FGW), 1,06 Å (1AD9), 1,06 Å (1FVC) и 1,06 Å (1BJ1). Учитывая близость этих значений, в качестве второго фактора скрининга рассчитывали процентную идентичность последовательностей (общую и только каркасную). Полученные значения для 1CZ8 (в целом 63%, каркас 54%), 2FGW (61% и 54%), 1AD9 (65% и 60%), 1FVC (67% и 61%) и 1BJ1 (63% и 53%). %), предположили, что 1FVC [гуманизированное антитело 4D5, версия 8, анти-p185 HER2 , герцептин трастузумаб, (Eigenbrot, 1993)] является наиболее подходящим источником каркаса, поскольку степень перекрытия и процент идентичности последовательностей были высокими.
Визуальный осмотр наложенных друг на друга структур T84.66 и Herceptin Fv показал, что минимальное нарушение петель CDR может быть достигнуто путем делеции семи пептидных сегментов (L24–L34, L50–L56, L66–L69, L89–L97, h40–h45 , H50–H58, H93–h202) из структуры Herceptin (трансплантат-акцептор Fv) и заменив их соответствующими сегментами из T84.66 (трансплантат-донор Fv). После завершения трансплантации полученную молекулярную модель проверяли на наличие возможных стерических столкновений между донорными и акцепторными боковыми цепями на границе CDR-каркас. Единственное столкновение между каркасным остатком L4 (met) и остатком CDR-L1 L33 (leu) устраняли путем замены первого его мышиным эквивалентом (leu). Полученная гуманизированная структура M5A была подвергнута алгоритму минимизации энергии (сопряженные градиенты до максимальной производной 5,0 ккал/моль-Å) для оптимизации длин связей и углов в местах сращивания. Включая остатки H59–H65 в списке пересаженных сегментов, так что вся петля Kabat CDR-h3 из T84. 66 присутствовала в пересаженной структуре, что привело к получению второй гуманизированной конструкции, M5B. Чтобы приспособить дополнительный сегмент, каркасный остаток H67 (phe) был заменен его мышиным эквивалентом (ala), чтобы облегчить стерическое столкновение с CDR-h3 остатком H63 (phe).
66 присутствовала в пересаженной структуре, что привело к получению второй гуманизированной конструкции, M5B. Чтобы приспособить дополнительный сегмент, каркасный остаток H67 (phe) был заменен его мышиным эквивалентом (ala), чтобы облегчить стерическое столкновение с CDR-h3 остатком H63 (phe).
Молекулярная биология
ПЦР удлинения с перекрытием сплайсинга (Horton, 1989) использовали для создания полностью синтетических генов, кодирующих белковые последовательности M5A и M5B Fv. Схематическая диаграмма стратегии ПЦР показана на рисунке 1. Восемь олигонуклеотидов (Integrated DNA Technologies, Inc., Coralville, IA) размером от 79для каждой конструкции домена требовалось до 89 оснований. Степень перекрытия между соседними олигонуклеотидами соответствовала 30 парам оснований. Последовательности праймеров ПЦР для вариабельного домена легкой цепи (VL) и вариабельной области тяжелой цепи (VH) были следующими:
Рис. 1.
1.
Открыть в новой вкладкеСкачать слайд
Схематическая диаграмма стратегии праймеров для ПЦР. Для создания полностью синтетических генов, кодирующих белковые последовательности M5A и M5B Fv, использовали ПЦР удлинения сплайсинга с перекрыванием. Для каждого вариабельного домена легкой цепи и вариабельной области тяжелой цепи использовали восемь олигонуклеотидов размером от 79 до 89 оснований.
Для построения каждого гена вариабельного домена потребовалось четыре амплификации SOE-PCR. Сначала амплифицировали самую внутреннюю пару праймеров (4 и 5). Полученный продукт ПЦР подвергали гель-очистке и дополняли следующим набором внешних праймеров (3 и 6). В третьем расширении использовались праймеры 2 и 7, тогда как в последнем расширении использовались праймеры 1 и 8. Каждая 50 мкл реакционной смеси содержала реакционный буфер, 2 ед. ДНК-полимеразы Vent (New England Biolabs, Беверли, Массачусетс), праймеры для амплификации по 1 мкМ каждый и дНТФ при 200 мкМ. Использование GeneAmp PCR 9600 (Perkin Elmer, Wellesley, MA), образцы нагревали в течение 2 мин при 94°C, после чего следовали 30 циклов нагревания по 30 с при 94°C, 30 с при 55°C и 30 с при 72°C. После 30 циклов температуру поддерживали постоянной на уровне 72°С в течение 10 мин для обеспечения полного удлинения. В каждом случае готовую реакционную смесь для ПЦР подвергали электрофорезу на 1% агарозном геле (Sigma Chemical, Сент-Луис, Миссури) и желаемый продукт экстрагировали из среза геля массой 200 мг с использованием колонки Qiaquik (Qiagen, Валенсия, Калифорния). Для второй, третьей и четвертой реакций в качестве матрицы использовали 10 нг очищенного продукта предыдущей реакции. По отдельности очищенные полноразмерные синтетические гены расщепляли Xba I и Xho I и лигировали в одну из двух экспрессионных плазмид (pEE12 для VL; pEE6 для VH). Эти плазмиды, которые содержат ген глутаминсинтетазы (GS) (Lonza Biologics, Slough, UK; Bebbington, 1992), были предварительно модифицированы, чтобы содержать кДНК, соответствующую константным областям человеческого антитела IgG 1 .
Использование GeneAmp PCR 9600 (Perkin Elmer, Wellesley, MA), образцы нагревали в течение 2 мин при 94°C, после чего следовали 30 циклов нагревания по 30 с при 94°C, 30 с при 55°C и 30 с при 72°C. После 30 циклов температуру поддерживали постоянной на уровне 72°С в течение 10 мин для обеспечения полного удлинения. В каждом случае готовую реакционную смесь для ПЦР подвергали электрофорезу на 1% агарозном геле (Sigma Chemical, Сент-Луис, Миссури) и желаемый продукт экстрагировали из среза геля массой 200 мг с использованием колонки Qiaquik (Qiagen, Валенсия, Калифорния). Для второй, третьей и четвертой реакций в качестве матрицы использовали 10 нг очищенного продукта предыдущей реакции. По отдельности очищенные полноразмерные синтетические гены расщепляли Xba I и Xho I и лигировали в одну из двух экспрессионных плазмид (pEE12 для VL; pEE6 для VH). Эти плазмиды, которые содержат ген глутаминсинтетазы (GS) (Lonza Biologics, Slough, UK; Bebbington, 1992), были предварительно модифицированы, чтобы содержать кДНК, соответствующую константным областям человеческого антитела IgG 1 . В плазмиде легкой цепи рЕЕ12 остаток L104, кодон которого является частью сайта рестрикции Xho I, мутировали с лейцина на валин с использованием набора QuikChange (Stratagene, Сан-Диего, Калифорния) для восстановления последовательности герцептина в этом область, край. Двухцепочечная плазмида была сконструирована путем расщепления плазмиды тяжелой цепи pEE6 с помощью Bgl II и Bam HI для выделения гена тяжелой цепи, который затем лигировали в сайт Bam HI плазмиды легкой цепи pEE12. Весь ген IgG 1 был секвенирован в обоих направлениях для подтверждения его идентичности. Перед электропорацией двухцепочечную плазмиду линеаризовали с помощью Sal I, фильтровали через связывающую белок мембрану для удаления рестриктазы (Millipore, Bedford, MA), осаждали этанолом и ресуспендировали в стерильной воде до концентрации 1 мкг/мл. мкл.
В плазмиде легкой цепи рЕЕ12 остаток L104, кодон которого является частью сайта рестрикции Xho I, мутировали с лейцина на валин с использованием набора QuikChange (Stratagene, Сан-Диего, Калифорния) для восстановления последовательности герцептина в этом область, край. Двухцепочечная плазмида была сконструирована путем расщепления плазмиды тяжелой цепи pEE6 с помощью Bgl II и Bam HI для выделения гена тяжелой цепи, который затем лигировали в сайт Bam HI плазмиды легкой цепи pEE12. Весь ген IgG 1 был секвенирован в обоих направлениях для подтверждения его идентичности. Перед электропорацией двухцепочечную плазмиду линеаризовали с помощью Sal I, фильтровали через связывающую белок мембрану для удаления рестриктазы (Millipore, Bedford, MA), осаждали этанолом и ресуспендировали в стерильной воде до концентрации 1 мкг/мл. мкл.
Экспрессия в культуре клеток млекопитающих
Двухцепочечный вектор экспрессии pEE12/6 подвергали электропорации в клетки мышиной миеломы NS0 в соответствии с ранее описанными процедурами (Bebbington, 1992; Yazaki, 2001). Селекция трансфектантов в культуральной среде без глютамина (JRH Biosciences, Kenexa, KN) привела к многочисленным клонам, которые подвергали скринингу с использованием рекомбинантного фрагмента СЕА (Young, 1998) на основе ELISA (Yazaki, 2001). M5A mAb получали в биореакторе с полыми волокнами Cell Pharm (CP) 2000 в соответствии с руководством оператора (Biovest International, Minneapolis, MN). CP2000 был оснащен одним картриджем с полым волокном площадью 20 кв. футов (за исключением молекулярной массы 10 кДа) и оксигенатором площадью 10 кв. футов. Уровни рН, глюкозы, лактата, аммиака и продукции антител контролировали через день. Внесены коррективы в поступающий O 2 и CO 2 для поддержания pH в диапазоне от 7,0 до 7,2. Среду IMDM (Biowhittaker, Walkerville, MD) с добавлением 2% эмбриональной бычьей сыворотки (FBS) (Hyclone, Logan, UT) использовали во внутрикапиллярном пространстве (ICS). Селективную среду GS (JRH Bioscience, Lenexa, KS) +2% FBS использовали во внекапиллярном пространстве (ECS).
Селекция трансфектантов в культуральной среде без глютамина (JRH Biosciences, Kenexa, KN) привела к многочисленным клонам, которые подвергали скринингу с использованием рекомбинантного фрагмента СЕА (Young, 1998) на основе ELISA (Yazaki, 2001). M5A mAb получали в биореакторе с полыми волокнами Cell Pharm (CP) 2000 в соответствии с руководством оператора (Biovest International, Minneapolis, MN). CP2000 был оснащен одним картриджем с полым волокном площадью 20 кв. футов (за исключением молекулярной массы 10 кДа) и оксигенатором площадью 10 кв. футов. Уровни рН, глюкозы, лактата, аммиака и продукции антител контролировали через день. Внесены коррективы в поступающий O 2 и CO 2 для поддержания pH в диапазоне от 7,0 до 7,2. Среду IMDM (Biowhittaker, Walkerville, MD) с добавлением 2% эмбриональной бычьей сыворотки (FBS) (Hyclone, Logan, UT) использовали во внутрикапиллярном пространстве (ICS). Селективную среду GS (JRH Bioscience, Lenexa, KS) +2% FBS использовали во внекапиллярном пространстве (ECS). Скорость подачи ИКС составляла 1,0–2,2 л/сут, скорость рециркуляции – 350–500 мл/мин. К ECS был подключен автоуборочный комбайн (Biowest International), запрограммированный на производительность 30–80 мл в сутки.
Скорость подачи ИКС составляла 1,0–2,2 л/сут, скорость рециркуляции – 350–500 мл/мин. К ECS был подключен автоуборочный комбайн (Biowest International), запрограммированный на производительность 30–80 мл в сутки.
Количественное определение антител
Для количественного определения антител использовали аффинную колонку с белком А (Poros 20A, Applied Biosystems, Foster City, CA; 0,46 см внутр. диаметра × 10 см ч, 0,5 мл/мин). Колонку уравновешивали в PBS, загружали образец, промывали 0,02 М цитрата натрия/0,02 М фосфата натрия, рН 7,4/0,5 М хлорида натрия и 0,1 М цитрата натрия. Антитело элюировали линейным градиентом от 100% 0,1 М цитрата натрия до 100% 0,1 М лимонной кислоты. Поглощение контролировали при 280 нм и концентрацию антител определяли путем сравнения со стандартом.
Очистка
Индивидуально собранные культуры клеток очищали периодической обработкой (5% мас./об.) анионообменником AG1x8 (Bio-Rad Laboratories, Hercules, CA). Начальный захват проводили на колонке Prosep rA (Millipore, 1 см × 10 см, 2,5 мл/мин), предварительно уравновешенной PBS. Осветленный урожай загружали и промывали смесью 0,02 М цитрата натрия/0,02 М фосфата натрия, рН 7,4/0,5 М хлорида натрия. Антитело элюировали линейным градиентом от 100% 0,01 М фосфата натрия, рН 7,4, до 100% 0,01 М фосфата натрия, рН 4,0. Элюированный материал собирали в пробирки, содержащие 0,05 М фосфата натрия, рН 8,0 (10% по объему). Элюированный пик белка А подвергали диализу относительно 0,05 М фосфата натрия, рН 5,5, в течение ночи перед загрузкой на катионообменную колонку Source 15S (GE Biosciences, Piscataway, NJ; 0,4 см × 10 см, 2 мл/мин). МкАТ элюировали линейным градиентом от 0 до 0,4 М хлорида натрия/0,05 М фосфата натрия, рН 5,5. Элюированное антитело собирали в пробирки, содержащие 1 М трис, рН 8,0 (10% по объему). При анализе с помощью SDS-PAGE и ВЭЖХ фракции, содержащие антитела, объединяли и подвергали диализу в течение ночи по сравнению с PBS.
Начальный захват проводили на колонке Prosep rA (Millipore, 1 см × 10 см, 2,5 мл/мин), предварительно уравновешенной PBS. Осветленный урожай загружали и промывали смесью 0,02 М цитрата натрия/0,02 М фосфата натрия, рН 7,4/0,5 М хлорида натрия. Антитело элюировали линейным градиентом от 100% 0,01 М фосфата натрия, рН 7,4, до 100% 0,01 М фосфата натрия, рН 4,0. Элюированный материал собирали в пробирки, содержащие 0,05 М фосфата натрия, рН 8,0 (10% по объему). Элюированный пик белка А подвергали диализу относительно 0,05 М фосфата натрия, рН 5,5, в течение ночи перед загрузкой на катионообменную колонку Source 15S (GE Biosciences, Piscataway, NJ; 0,4 см × 10 см, 2 мл/мин). МкАТ элюировали линейным градиентом от 0 до 0,4 М хлорида натрия/0,05 М фосфата натрия, рН 5,5. Элюированное антитело собирали в пробирки, содержащие 1 М трис, рН 8,0 (10% по объему). При анализе с помощью SDS-PAGE и ВЭЖХ фракции, содержащие антитела, объединяли и подвергали диализу в течение ночи по сравнению с PBS.
Биохимическая характеристика
Аликвоты очищенных mAb M5A, M5B и cT84. 66 подвергли электрофорезу с помощью SDS-PAGE (Laemmli, 1970). Эксклюзионную хроматографию проводили на колонке Superdex 200 HR10/30 (GE Biosciences, 0,5 мл/мин) в изократическом режиме с PBS. Колонку стандартизировали стандартами гель-фильтрации (Bio-Rad Laboratories). Изоэлектрическую точку каждого mAb определяли в гелях IEF с pH 3–10 (Novex Inc., Сан-Диего, Калифорния) и сравнивали со стандартами белка IEF (Serva Electrophoresis, Heidelberg, Germany).
66 подвергли электрофорезу с помощью SDS-PAGE (Laemmli, 1970). Эксклюзионную хроматографию проводили на колонке Superdex 200 HR10/30 (GE Biosciences, 0,5 мл/мин) в изократическом режиме с PBS. Колонку стандартизировали стандартами гель-фильтрации (Bio-Rad Laboratories). Изоэлектрическую точку каждого mAb определяли в гелях IEF с pH 3–10 (Novex Inc., Сан-Диего, Калифорния) и сравнивали со стандартами белка IEF (Serva Electrophoresis, Heidelberg, Germany).
Кинетическое сродство mAb к связыванию с очищенным CEA определяли методом поверхностного плазмонного резонанса (SPR) на приборе BIAcore 1000 (BIAcore AB, Уппсала, Швеция). CEA биотинилировали с использованием набора EZ-Link Sulfo-NHS-LC-Biotin (Pierce, Rockford, IL) и иммобилизовали на чипе биосенсора SA (BIAcore Inc.) в буфере HBS. Кинетический аффинный анализ проводили при серии концентраций mAb (3,12, 6,25, 12,5, 25, 50 и 100 нМ), инъецированных поверх низкой плотности (175 RU) иммобилизованного СЕА-биотина с регенерацией однократным импульсом 6 М гидрохлорида гуанидина. . Данные были проанализированы с помощью программного обеспечения BIAevaluation (v3.0) с использованием модели двухвалентного аналита для расчета K A = k на / k на . Концентрации белка определяли аминокислотным анализом.
. Данные были проанализированы с помощью программного обеспечения BIAevaluation (v3.0) с использованием модели двухвалентного аналита для расчета K A = k на / k на . Концентрации белка определяли аминокислотным анализом.
Радиоактивное мечение
мАт M5A, M5B и cT84.66 подвергали радиоактивному йодированию методом йодогена, как описано ранее (Wu, 1996). Чистоту радиоактивно меченых mAb определяли путем наблюдения за радиохроматограммой тандемных колонок Superose 6 HR10/30 (GE Biosciences). Для 111 При маркировке mAb M5A конъюгировали с N -гидроксисукцинимидил DOTA (Macrocyclos, Dallas, TX) с использованием ранее описанных условий (Lewis, 2001).
Исследования на животных
Группам самок бестимусных мышей в возрасте от 7 до 8 недель (Charles River Laboratories, Wilmington, MA) вводили подкожно в боковую область 10 6 клеток карциномы толстой кишки человека LS174T, полученных от American Tissue Culture Центр (ATCC, Манассас, Вирджиния). Через 10 дней, когда опухолевые массы были в пределах 100–300 мг, 1–3 мкКи 131 I-меченые M5A, M5B или cT84.66 на животное вводили в хвостовую вену. В моменты времени 0, 6, 24, 48, 72 и 96 ч животных подвергали эвтаназии, проводили вскрытие, органы взвешивали и подсчитывали на радиоактивность. Все данные являются средними значениями и были скорректированы с учетом радиоактивного распада до момента инъекции, что позволяет сообщать о поглощении органами в процентах от введенной дозы на грамм (% ID г -1 ) со стандартными ошибками.
Через 10 дней, когда опухолевые массы были в пределах 100–300 мг, 1–3 мкКи 131 I-меченые M5A, M5B или cT84.66 на животное вводили в хвостовую вену. В моменты времени 0, 6, 24, 48, 72 и 96 ч животных подвергали эвтаназии, проводили вскрытие, органы взвешивали и подсчитывали на радиоактивность. Все данные являются средними значениями и были скорректированы с учетом радиоактивного распада до момента инъекции, что позволяет сообщать о поглощении органами в процентах от введенной дозы на грамм (% ID г -1 ) со стандартными ошибками.
Для исследований на животных мышам с опухолями вводили седативное средство, 20 мкКи [ 111 In] DOTA-M5A вводили внутривенно, и мышь помещали вентральной стороной вниз на миниатюрную сцинтиграфическую камеру высокого разрешения γ IMAGER (BIOSPACE Mesures s.a., Париж, Франция). Система γ IMAGER была переработана с учетом наших требований к визуализации мышей. Модификации состояли из непрерывного кристалла йодида цезия диаметром 120 мм и толщиной 4 мм, который обеспечивает круглое поле зрения диаметром 100 мм, и коллиматора с параллельными отверстиями, специально разработанного для визуализации. Седацию и визуализацию повторяли в дни 1, 2, 3, 6 и 7.
Седацию и визуализацию повторяли в дни 1, 2, 3, 6 и 7.
Биостатистический анализ
Для сравнения различий в поглощении mAb M5A, M5B и cT84.66 с течением времени был проведен двухфакторный дисперсионный анализ (ANOVA). Взаимодействие между временем и антителами было включено в статистическую модель наряду с основными эффектами времени и антител. Зависимые переменные, сравниваемые с использованием этой модели, включали процент введенной дозы на грамм для органов: кровь, печень, селезенка, почка, легкое, опухоль и туша, анализируемые отдельно. Регистрировали отношение опухоли к крови, а также массу опухоли. Для сравнения различий между антителами в определенные моменты времени использовали защищенную процедуру наименьших значимых различий. Все тесты значимости проводились на уровне 0,01 с использованием программного обеспечения SAS (SAS Inc., Кэри, Северная Каролина).
Результаты и обсуждение
Гуманизация дизайна
Структура мышиного T84. 66 (в виде димера scFv) была предварительно определена с помощью рентгеноструктурного анализа с разрешением 2,6 Å (Carmichael, 2003). Доступность структурных данных значительно облегчила подход к гуманизации CDR-прививки. Обычно подходящие акцепторные последовательности VL и VH выбирают на основе поиска гомологии в базе данных последовательностей иммуноглобулинов Kabat (Johnson, 2001). В этом исследовании подходящая акцепторная структура была выбрана на основе поиска гомологов T84.66 в базе данных белков (Bernstein, 19).77) с использованием векторной программы структурного выравнивания (Gibrat, 1996). Это гарантировало, что родственная пара VL:VH будет выбрана с углом спаривания доменов, который соответствует углу спаривания T84.66, сохраняя относительную ориентацию петель CDR тяжелой и легкой цепей. Из антител, которые имели гомологичные структуры, гуманизированное антитело 4D5, версия 8 (анти-p185 HER2 , Герцептин, файл PDB 1FVC) (Eigenbrot, 1993) было выбрано в качестве наиболее подходящего поставщика каркаса.
66 (в виде димера scFv) была предварительно определена с помощью рентгеноструктурного анализа с разрешением 2,6 Å (Carmichael, 2003). Доступность структурных данных значительно облегчила подход к гуманизации CDR-прививки. Обычно подходящие акцепторные последовательности VL и VH выбирают на основе поиска гомологии в базе данных последовательностей иммуноглобулинов Kabat (Johnson, 2001). В этом исследовании подходящая акцепторная структура была выбрана на основе поиска гомологов T84.66 в базе данных белков (Bernstein, 19).77) с использованием векторной программы структурного выравнивания (Gibrat, 1996). Это гарантировало, что родственная пара VL:VH будет выбрана с углом спаривания доменов, который соответствует углу спаривания T84.66, сохраняя относительную ориентацию петель CDR тяжелой и легкой цепей. Из антител, которые имели гомологичные структуры, гуманизированное антитело 4D5, версия 8 (анти-p185 HER2 , Герцептин, файл PDB 1FVC) (Eigenbrot, 1993) было выбрано в качестве наиболее подходящего поставщика каркаса. Наложенные структуры показали высокую степень перекрытия со среднеквадратичным отклонением. 1,07 Å для 1326 атомов основной цепи. Кроме того, угол спаривания доменов VL-VH был практически одинаковым для обеих структур, как видно из двух ортогональных проекций на рис. 2.9.0419
Наложенные структуры показали высокую степень перекрытия со среднеквадратичным отклонением. 1,07 Å для 1326 атомов основной цепи. Кроме того, угол спаривания доменов VL-VH был практически одинаковым для обеих структур, как видно из двух ортогональных проекций на рис. 2.9.0419
Рис. 2.
Открыть в новой вкладкеСкачать слайд
Наложенные следы альфа-углерода T84.66 Fv (черный) и герцептина (серый). Показаны два ортогональных вида. Наблюдается высокая степень структурного перекрытия в каркасных областях.
При конструировании гуманизированного антитела T84.66 были исследованы многие структурные особенности Fv донора и акцептора трансплантата, чтобы лучше понять, как различные остатки каркаса влияют на конформацию петель CDR и наоборот. Исследование T84.66, донора трансплантата, показало, что петли CDR L2, L3, h2 и h3 имеют каноническую структуру и, следовательно, могут быть трансплантированы без значительных изменений в структуре или значительной потери антигенсвязывающей аффинности, как показано с помощью недавнее кристаллографическое сравнение двух гуманизированных Fv с их мышиными аналогами (Banfield, 1997). Однако было обнаружено, что петли CDR L1 и h4 являются структурно уникальными и, следовательно, требуют более тщательного изучения, чтобы определить, как сохраняются их необычные конформации. Петля CDR-L1 из 11 остатков напоминала каноническую петлю из 13 остатков, но удаление двух остатков с ее кончика вызвало непредвиденный поворот в этой области и нарушение сети водородных связей, которая стабилизирует остатки L30–L32. Структура петли CDR-h4 из 12 остатков также оказалась не такой, как предсказывалось на основе гомологичных структур, в основном из-за редкого остатка пролина, расположенного в каркасном положении H9.4. Пролин, лишенный амидного водорода, не может участвовать в сети водородных связей, которая обычно стабилизирует основание большинства петель h4 и в значительной степени определяет их конформацию (Morea, 1998). Чтобы компенсировать его неспособность образовывать водородные связи, боковая цепь пролина присоединяется к гидрофобному кластеру, образованному каркасными остатками h3 (val), h5 (leu) и h37 (phe), а также остатками CDR-h4 H99 (val) и h201 (tyr).
Однако было обнаружено, что петли CDR L1 и h4 являются структурно уникальными и, следовательно, требуют более тщательного изучения, чтобы определить, как сохраняются их необычные конформации. Петля CDR-L1 из 11 остатков напоминала каноническую петлю из 13 остатков, но удаление двух остатков с ее кончика вызвало непредвиденный поворот в этой области и нарушение сети водородных связей, которая стабилизирует остатки L30–L32. Структура петли CDR-h4 из 12 остатков также оказалась не такой, как предсказывалось на основе гомологичных структур, в основном из-за редкого остатка пролина, расположенного в каркасном положении H9.4. Пролин, лишенный амидного водорода, не может участвовать в сети водородных связей, которая обычно стабилизирует основание большинства петель h4 и в значительной степени определяет их конформацию (Morea, 1998). Чтобы компенсировать его неспособность образовывать водородные связи, боковая цепь пролина присоединяется к гидрофобному кластеру, образованному каркасными остатками h3 (val), h5 (leu) и h37 (phe), а также остатками CDR-h4 H99 (val) и h201 (tyr). , таким образом заставляя кончик петли CDR-h4 (H98-h200A) загибаться, а не вытягиваться к сайту объединения, как ожидается для петли такой длины. Поэтому мы постарались сохранить все эти уникальные структурные особенности при разработке гуманизированной версии T84.66.
, таким образом заставляя кончик петли CDR-h4 (H98-h200A) загибаться, а не вытягиваться к сайту объединения, как ожидается для петли такой длины. Поэтому мы постарались сохранить все эти уникальные структурные особенности при разработке гуманизированной версии T84.66.
Структуру акцептора трансплантата также тщательно исследовали, чтобы определить, влияют ли какие-либо каркасные остатки неожиданным образом на конформацию петель CDR. Данные о структуре герцептина (как Fv, определенные с разрешением 2,2 Å) (Carter, 1992; Eigenbrot, 1993) в сочетании с данными сайт-направленного мутагенеза подтвердили влияние пяти каркасных остатков на конформацию петли CDR и на относительное связывание. близость. В частности, авторы исследования идентифицировали каркасные остатки L66, H71, H73, H78 и H9.3, как основные детерминанты конформации петли CDR. Аргинин L66, который образует солевой мостик с аспартатом в положении L28 в CDR-L1, либо непосредственно взаимодействует с антигеном, либо стабилизирует специфическую конформацию CDR-L1, поскольку замена аргинина глицином приводит к 4-кратному снижению аффинности связывания. Было показано, что аланин H93 при обратной мутации в его мышиный аналог (серин) увеличивает сродство герцептина к антигену в 2 раза. Структурные последствия гуманизации каркасных остатков H71, H73 и H78 в нашей гибридной конструкции можно смело игнорировать, поскольку эти остатки одинаковы в донорных и акцепторных Fvs.
Было показано, что аланин H93 при обратной мутации в его мышиный аналог (серин) увеличивает сродство герцептина к антигену в 2 раза. Структурные последствия гуманизации каркасных остатков H71, H73 и H78 в нашей гибридной конструкции можно смело игнорировать, поскольку эти остатки одинаковы в донорных и акцепторных Fvs.
При наложении донорной и акцепторной структур Fv стало ясно, что пептидные сегменты, которые необходимо было трансплантировать, не обязательно соответствовали ни петлям CDR, определенным Kabat (1971) или Chothia (1987), ни определяющей специфичность области (SDR ) петли, определенные Падланом (1995). Скорее, сегменты просто соответствовали областям, которые различались по структуре, когда две единицы Fv накладывались друг на друга. При конструировании гибридной VL традиционные границы петель CDR по Kabat не изменялись. Однако пептидный сегмент, не относящийся к CDR (L66–L69) от донора также трансплантировали на акцепторный каркас, поскольку было показано, что остаток L66 влияет на конформацию CDR-L1 герцептина, как описано выше. При конструировании гибридной VH все три границы петель CDR были изменены. Определение по Кабату CDR-h2 (h41–h45) было расширено за счет включения h40, так как этот остаток упаковывается против кончика CDR-h3 в T84.66. Для CDR-h3 существует большое расхождение между определением Kabat, основанным на гипервариабельности последовательности (H50–H65), и определением Chothia, основанным на структурной изменчивости (H52–H56). Еще больше усложняет ситуацию то, что только остатки H50–H58 Kabat CDR-h3 взаимодействуют с антигеном в тех случаях, когда исследуются сокристаллы антитело-антиген (Padlan, 19).95; МакКаллум, 1996). Обратите внимание, однако, что два независимых отчета о гуманизации предполагают, что это не всегда так, поскольку неспособность сохранить мышиные остатки в положениях H59–H65 в гуманизированной конструкции снижала аффинность связывания более чем в 1000 раз в каждом случае (Eigenbrot, 1994; O' Коннор, 1998). По этой причине были разработаны две гуманизированные конструкции: T84.
При конструировании гибридной VH все три границы петель CDR были изменены. Определение по Кабату CDR-h2 (h41–h45) было расширено за счет включения h40, так как этот остаток упаковывается против кончика CDR-h3 в T84.66. Для CDR-h3 существует большое расхождение между определением Kabat, основанным на гипервариабельности последовательности (H50–H65), и определением Chothia, основанным на структурной изменчивости (H52–H56). Еще больше усложняет ситуацию то, что только остатки H50–H58 Kabat CDR-h3 взаимодействуют с антигеном в тех случаях, когда исследуются сокристаллы антитело-антиген (Padlan, 19).95; МакКаллум, 1996). Обратите внимание, однако, что два независимых отчета о гуманизации предполагают, что это не всегда так, поскольку неспособность сохранить мышиные остатки в положениях H59–H65 в гуманизированной конструкции снижала аффинность связывания более чем в 1000 раз в каждом случае (Eigenbrot, 1994; O' Коннор, 1998). По этой причине были разработаны две гуманизированные конструкции: T84. 66 M5A, в которой остатки H59–H65 соответствуют последовательности акцептора человека (рис. 3a), и T84.66 M5B, в которой эти остатки соответствуют последовательности донора мыши (рис. 3b). Наконец, основываясь на наших знаниях о ключевой структурной роли, которую играет редкий пролин в положении H94 в T84.66 и важности H93 (Xiang, 1995), мы расширили определение CDR-h4 по Кабату, включив в него каркасные остатки H93 и H94. Стратегия трансплантации CDR показана путем выравнивания последовательностей на рисунке 4.
66 M5A, в которой остатки H59–H65 соответствуют последовательности акцептора человека (рис. 3a), и T84.66 M5B, в которой эти остатки соответствуют последовательности донора мыши (рис. 3b). Наконец, основываясь на наших знаниях о ключевой структурной роли, которую играет редкий пролин в положении H94 в T84.66 и важности H93 (Xiang, 1995), мы расширили определение CDR-h4 по Кабату, включив в него каркасные остатки H93 и H94. Стратегия трансплантации CDR показана путем выравнивания последовательностей на рисунке 4.
Рис. 3.
Открыть в новой вкладкеСкачать слайд
Рендеринг ленты модели M5A ( a ) и модели M5B ( b ). Красные сегменты представляют человеческие остатки Герцептина. Синие сегменты представляют мышиные остатки из T84.66. Границы сегментов отмечены остаточными номерами. Остатки, представленные в виде шариков и стержней, представляют собой остатки каркаса, которые были подвергнуты обратной мутации для облегчения стерических столкновений с соседними остатками CDR.
Рис. 4.
Открыть в новой вкладкеСкачать слайд
Основанное на структуре выравнивание последовательностей вариабельного легкого (VL) и вариабельного домена тяжелой цепи (VH) T84.66 с Герцептином, M5A и M5B. Сегменты пептидов человеческого происхождения показаны обычным шрифтом. Остатки пептидов мышиного происхождения выделены жирным шрифтом. Последовательности и границы CDR пронумерованы согласно Kabat and Wu (1971). Обратите внимание, что сегменты, которые были трансплантированы от донора к акцептору для создания M5A и M5B, не обязательно соответствуют петлям CDR Kabat и Wu.
Экспрессия, характеристика и получение
Полностью синтетические гены, кодирующие последовательности белков M5A и M5B Fv, были сконструированы с использованием серии реакций SOE-PCR, как показано на рисунке 1. После конструирования гены для вариабельных доменов M5A и M5B были лигированы. к человеческому IgG 1 константных доменов, и mAb были экспрессированы в мышиных миеломных клетках NS0 (Bebbington, 1992; Yazaki, 2001). Очистка с помощью протеина А и катионообменная хроматография с использованием стандартных условий привели к получению высокоочищенных антител. мАт М5А и М5В подвергали биохимической характеристике, при этом мАт cT84.66 служили контролем. Правильная сборка антител была подтверждена эксклюзионной хроматографией ВЭЖХ после очистки (фиг. 5, левая панель) и после радиоактивного йодирования (фиг. 5, правая панель). Гуманизированные mAb M5A и M5B имеют изоэлектрическую точку (стр. I ) в диапазоне 8,4, демонстрируя явную миграцию от исходного mAb T84.66 (p I 7,4) к более щелочному герцептину (p I > 9,0) (рис. 6). SPR-анализ с помощью BIAcore продемонстрировал субнаномолярное сродство к СЕА для mAb M5A, M5B и cT84,66 с K A = 1,1×10 10 M -1 , 1,9×10 12 -1 21 10 и 1,6×10 10 M -1 соответственно (таблица I).
Очистка с помощью протеина А и катионообменная хроматография с использованием стандартных условий привели к получению высокоочищенных антител. мАт М5А и М5В подвергали биохимической характеристике, при этом мАт cT84.66 служили контролем. Правильная сборка антител была подтверждена эксклюзионной хроматографией ВЭЖХ после очистки (фиг. 5, левая панель) и после радиоактивного йодирования (фиг. 5, правая панель). Гуманизированные mAb M5A и M5B имеют изоэлектрическую точку (стр. I ) в диапазоне 8,4, демонстрируя явную миграцию от исходного mAb T84.66 (p I 7,4) к более щелочному герцептину (p I > 9,0) (рис. 6). SPR-анализ с помощью BIAcore продемонстрировал субнаномолярное сродство к СЕА для mAb M5A, M5B и cT84,66 с K A = 1,1×10 10 M -1 , 1,9×10 12 -1 21 10 и 1,6×10 10 M -1 соответственно (таблица I).
Рис. 5.
Открыть в новой вкладкеЗагрузить слайд
Эксклюзионная хроматография ВЭЖХ. Аликвоты очищенных mAb M5A, M5B и cT84.66 анализировали с помощью эксклюзионной хроматографии ВЭЖХ после очистки на калиброванной колонке Superdex 200 HR10/30 (справа) и после радиоактивного иодирования на калиброванной колонке Superdex 60 HR10/30 (слева). Отображается поглощение при 280 нм (мАЕ) или радиоактивность в зависимости от времени (минуты).
Аликвоты очищенных mAb M5A, M5B и cT84.66 анализировали с помощью эксклюзионной хроматографии ВЭЖХ после очистки на калиброванной колонке Superdex 200 HR10/30 (справа) и после радиоактивного иодирования на калиброванной колонке Superdex 60 HR10/30 (слева). Отображается поглощение при 280 нм (мАЕ) или радиоактивность в зависимости от времени (минуты).
Рис. 6.
Открыть в новой вкладкеСкачать слайд
Гель-электрофорез ИЭФ. Аликвоты очищенных mAb cT84.66, M5A, M5B и Herceptin (Her) вместе со стандартами изоэлектрического белка (Std) подвергали электрофорезу на изоэлектрофокусирующем геле, pH 3–10.
Таблица I.
BIAcore-анализ аффинности M5A, M5B и cT84.66 mAb к CEA
Антитело
. к а1 (М -1 с -1 )
. к d1 (s −1 )
.
K A = k на / k на (M −1 )
. M5A 3.3 × 10 5 3.01 × 10 −5 1.1 × 10 10 M5B 4.88 × 10 5 2.56 × 10 −5 1.9 × 10 10 cT84.66 2.61 × 10 5 1.62 × 10 −5 1.6 × 10 10
Антитело
. к а1 (М -1 с -1 )
. к d1 (s −1 )
. K A = k на / k на (M −1 )
.
M5A 3.3 × 10 5 3.01 × 10 −5 1.1 × 10 10 M5B 4.88 × 10 5 2.56 × 10 −5 1,9 × 10 10 cT84.66 2,61 × 10 5 1,62 × 10 -5 1,6 × 10 10
. 66 мАТ для СЕА. Биотинилированный CEA был соединен с чипом SA при низкой плотности ( R max = 175 RU). Сенсограммы анализировали с помощью программного обеспечения BIAeval 3.0. Открыть в новой вкладке
Таблица I.
BIAcore анализ аффинности M5A, M5B и cT84.66 mAb к CEA
Антитело
. к а1 (М -1 с -1 )
.
к d1 (s −1 )
. K A = k на / k на (M −1 )
. M5A 3.3 × 10 5 3.01 × 10 −5 1.1 × 10 10 M5B 4.88 × 10 5 2.56 × 10 −5 1.9 × 10 10 cT84.66 2.61 × 10 5 1.62 × 10 −5 1.6 × 10 10
Антитело
. к а1 (М -1 с -1 )
. к d1 (s −1 )
. K A = k на / k на (M −1 )
.
М5А 3.3 × 10 5 3.01 × 10 −5 1.1 × 10 10 M5B 4.88 × 10 5 2.56 × 10 −5 1.9 × 10 10 cT84.66 2.61 × 10 5 1.62 × 10 −5 1.6 × 10 10
SPR analysis by BIAcore was used to определяют кинетическую аффинность mAb M5A, M5B и cT84.66 к CEA. Биотинилированный CEA был соединен с чипом SA при низкой плотности ( Р max = 175 РУ). Сенсограммы анализировали с помощью программного обеспечения BIAeval 3.0.
Открыть в новой вкладке
Исследования биораспределения на животных с опухолями были проведены для определения нацеливания in vivo на опухоль и распределения mAb M5A и M5B в нормальных тканях. Результаты, представленные в Таблице II, показывают, что уровни поглощения mAb M5A статистически не отличались от уровней захвата cT84.66 в крови, опухоли или любых других органах. Точно так же mAb M5B в целом статистически не отличались от mAb cT84.66 в отношении поглощения кровью или любым другим нормальным органом. Однако M5B имел несколько более низкое поглощение опухолью (9).0437 p = 0,012), как показано на фигуре 7. При сопоставимой аффинности, клиренсе крови и 100% иммунореактивности после мечения растворимым антигеном in vitro (данные не показаны) было неясно, почему mAb M5B имело более низкое поглощение опухолью, чем M5A и может быть результатом экспериментальной вариации.
Результаты, представленные в Таблице II, показывают, что уровни поглощения mAb M5A статистически не отличались от уровней захвата cT84.66 в крови, опухоли или любых других органах. Точно так же mAb M5B в целом статистически не отличались от mAb cT84.66 в отношении поглощения кровью или любым другим нормальным органом. Однако M5B имел несколько более низкое поглощение опухолью (9).0437 p = 0,012), как показано на фигуре 7. При сопоставимой аффинности, клиренсе крови и 100% иммунореактивности после мечения растворимым антигеном in vitro (данные не показаны) было неясно, почему mAb M5B имело более низкое поглощение опухолью, чем M5A и может быть результатом экспериментальной вариации.
Рис. 7.
Открыть в новой вкладкеСкачать слайд
Поглощение опухолью и выведение из крови моноклональных антител Т84.66 у мышей с опухолями. 131 I-меченые антитела cT84.66, M5A и M5B вводили отдельным группам бестимусных мышей, несущих ксенотрансплантаты опухоли LS174T. Поглощение опухолью (сплошные линии) и клиренс крови (пунктирные линии) измеряли в процентах от введенной дозы на грамм на 0, 6, 24, 48, 72 и 96 ч.
Поглощение опухолью (сплошные линии) и клиренс крови (пунктирные линии) измеряли в процентах от введенной дозы на грамм на 0, 6, 24, 48, 72 и 96 ч.
Таблица II.
Биораспределение Процент введенной дозы на грамм (% ID/г) 131 I-меченых mAb cT84.66, M5A и M5B у мышей с опухолями
. Время (ч)
. . . . . .
. 0
. 6
. 24
. 48
. 72
. 96
. cT84.66 mAb Blood 31. 75 (1.36) a
75 (1.36) a 17.89 (1.04) 13.47 (0.88) 6.67 (1.11) 6.30 (0.50) 5.19 (0.72) Liver 6.22 (0.47) 4.11 (0.30) 2.87 (0.29) 2.00 (0.16) 1.68 (0.14) 1.51 (0.18) Spleen 4.66 (0.35) 3.60 (0.27) 2.78 (0.23) 1.60 (0,28) 1,57 (0,15) 1.31 (0.21) Kidney 5.24 (0.39) 3.56 (0.29) 2.77 (0.18) 1.67 (0.29) 1.34 (0.16) 1.15 (0.18) Lung 8.05 (0.56) 6.13 (0.41) 4.68 (0.27) 2.65 (0.50) 2.43 (0.16) 1.92 (0.23) Tumor 1.05 (0.09) 13,53 (1,26) 24.11 (0.94) 24. 08 (3.75)
08 (3.75) 25.31 (2.38) 25.45 (3.04) Carcass 2.04 (0.04) 3.25 (0.22) 2.95 (0.08) 2.02 (0.24) 1.80 (0.10) 1.53 (0.17) M5A mAb Blood 38.7 (0.65) 23.86 (0.79) 11.92 (0.72) 10.31 (1.15) 5.10 (0.68) 3.75 (0.39) Liver 8.14 (0.48) 5.42 (0.30) 2.44 (0.29) 2.65 (0.11) 1.68 (0.37) 1.27 (0.18) Spleen 7.35 (0.65) 4.63 (0.43) 2.35 (0.28) 2.67 (0.34) 1,52 (0,31) 1.05 (0.23) Kidney 6. 75 (0.11)
75 (0.11) 4.80 (0.21) 2.43 (0.31) 2.27 (0.17) 1.20 (0.28) 0.90 (0.21) Lung 11.09 (0.72) 7.84 (0.15) 4.18 (0.41) 3.59 (0.26) 2.00 (0.43) 1.45 (0.37) Tumor 1.78 (0.09) 14,06 (1,26) 26.83 (0.94) 32.65 (3.75) 22.67 (2.38) 23.83 (3.04) Carcass 2.5 (0.12) 3.44 (0.05) 2.75 (0.20) 2.67 ( 0.13) 1.68 (0.21) 1.39 (0.18) M5B mAb Blood 31.37 (1.00) 15.81 (0.43) 10.49 (0.51) 8.43 (0.92) 5.79 (0. 83)
83) 5.81 (0.63) Liver 8.2 (0.41) 3.54 (0.11) 3.06 (0.33) 2.31 (0.10) 1.72 (0.19) 1.72 (0.15) Spleen 5.53 (0.30) 3.31 (0.26) 2.51 (0.22) 2.07 (0.11) 1,53 (0,17) 1.83 (0.33) Kidney 5.13 (0.51) 3.17 (0.15) 2.43 (0.28) 2.01 (0.22) 1.38 (0.20) 1.52 (0.15) Lung 9.51 (0.68) 5.05 (0.16) 3.74 (0.15) 3.35 (0.27) 2.41 (0.41) 2.30 (0.16) Tumor 5.17 (3.66) 10,52 (0,75) 19.58 (0.92) 24.83 (4.84) 18.57 (2.62) 7.15 (2.25) Carcass 2. 36 (0.18)
36 (0.18) 2.56 (0.10) 2.54 (0.10) 2.18 ( 0,10) 1,81 (0,14) 1,60 (0,10)
. Время (ч)
. . . . . .
. 0
. 6
. 24
. 48
. 72
. 96
. cT84.66 mAb Blood 31.75 (1.36) a 17.89 (1.04) 13.47 (0.88) 6.67 (1.11) 6.30 (0.50) 5. 19 (0.72)
19 (0.72) Liver 6.22 (0.47) 4.11 (0.30) 2.87 (0.29) 2.00 (0.16) 1.68 (0.14) 1.51 (0.18) Spleen 4.66 (0.35) 3.60 (0.27) 2.78 (0.23) 1.60 (0.28) 1.57 (0.15) 1.31 (0.21) Kidney 5.24 (0.39) 3.56 (0.29) 2.77 (0.18) 1.67 (0.29) 1.34 (0.16) 1.15 (0.18) Lung 8.05 (0.56) 6.13 (0.41) 4.68 (0.27) 2,65 (0,50) 2,43 (0,16) 1.92 (0.23) Tumor 1.05 (0.09) 13.53 (1.26) 24.11 (0.94) 24.08 (3.75) 25.31 (2.38) 25.45 (3.04) Carcass 2.04 (0.04) 3. 25 (0.22)
25 (0.22) 2.95 (0.08) 2.02 (0.24) 1.80 (0.10) 1.53 (0.17) M5A mAb Blood 38.7 (0.65) 23.86 (0.79) 11.92 (0.72) 10.31 (1.15) 5.10 (0.68) 3.75 (0.39) Liver 8.14 (0.48) 5.42 (0.30) 2.44 (0.29) 2.65 (0.11) 1.68 (0.37) 1.27 (0.18) Spleen 7.35 (0.65 ) 4.63 (0.43) 2.35 (0.28) 2.67 (0.34) 1.52 (0.31) 1.05 (0.23) Kidney 6.75 (0.11) 4.80 (0.21) 2.43 (0.31) 2.27 (0.17) 1.20 (0.28) 0.90 (0. 21)
21) Lung 11.09 (0.72) 7.84 (0.15) 4.18 (0.41) 3.59 (0.26) 2,00 (0,43) 1,45 (0,37) Tumor 1.78 (0.09) 14.06 (1.26) 26.83 (0.94) 32.65 (3.75) 22.67 (2.38) 23.83 (3.04) Carcass 2.5 ( 0.12) 3.44 (0.05) 2.75 (0.20) 2.67 (0.13) 1.68 (0.21) 1.39 (0.18) M5B mAb Blood 31.37 (1.00) 15.81 (0.43) 10.49 (0.51) 8.43 (0.92) 5.79 (0.83) 5.81 (0.63) Liver 8.2 (0.41) 3.54 (0.11) 3. 06 (0.33)
06 (0.33) 2.31 (0.10) 1.72 (0.19) 1.72 (0.15) Spleen 5.53 (0.30) 3.31 (0,26) 2.51 (0.22) 2.07 (0.11) 1.53 (0.17) 1.83 (0.33) Kidney 5.13 (0.51) 3.17 (0.15) 2.43 (0.28) 2.01 (0.22) 1.38 (0.20) 1.52 (0.15) Lung 9.51 (0.68) 5.05 (0.16) 3.74 (0.15) 3.35 (0.27) 2.41 (0.41) 2,30 (0,16) Tumor 5.17 (3.66) 10.52 (0.75) 19.58 (0.92) 24.83 (4.84) 18.57 (2.62) 7.15 (2.25) Carcass 2.36 (0.18) 2,56 (0,10) 2,54 (0,10) 2,18 (0,10) 1,81 (0,14) 1,60 (0,10)
61, USA Protein Engineering, Design & Selection vol. 17 нет. 5 © Издательство Оксфордского университета, 2004 г.; все права защищены
17 нет. 5 © Издательство Оксфордского университета, 2004 г.; все права защищены
Protein Engineering, Design & Selection vol. 17 нет. 5 © Издательство Оксфордского университета, 2004 г.; все права защищены
Раздел выпуска:
Оригинальные статьи
Скачать все слайды
Реклама
Цитаты
Альтметрика
Дополнительная информация о метриках
Оповещения по электронной почте
Оповещение об активности статьи
Предварительные уведомления о статьях
Оповещение о новой проблеме
Оповещение о текущей проблеме
Получайте эксклюзивные предложения и обновления от Oxford Academic
Ссылки на статьи по номеру
Подход белковой инженерии к повышению активности моно-АДФ-рибозилтрансфераз за счет близости
Голубые флуоресцентные белки, полученные из mNeonGreen
Стабилизация домена, связывающего рецептор SARS-CoV-2, путем редизайна ядра белка и глубокого мутационного сканирования
Созревание аффинности TCR-подобных антител с использованием фагового дисплея на основе структурного моделирования
Иммортализация и функциональный скрининг репертуаров нативно спаренных Т-клеточных рецепторов человека
Реклама
Крупномасштабный корпоративный банкоматный узел с управлением трафиком для каждого виртуального канала
ScienceDirect Регистенс в
View PDF
Том 31, выпуск 6, 25 марта 1999 г. , PAGES 617-659
, PAGES 617-659
. S0169-7552(98)00285-2Получение прав и контента
На магистральных узлах корпоративных сетей, обрабатывающих данные и голосовой трафик, требуются комплексные возможности качества обслуживания (QoS), эффективность передачи и высокая надежность. Технология ATM удовлетворяет этим требованиям. Мы разработали крупномасштабный корпоративный банкомат на основе архитектуры коммутатора с общим буфером. В узле функции управления трафиком для каждого виртуального канала реализованы с низкими затратами за счет централизованного управления записью и чтением буфера. В этой статье мы объясняем детали функций управления трафиком для каждого виртуального канала и показываем результаты производительности управления ABR с использованием узла.
В последнее время для узлов быстрой коммутации в корпоративных сетях доступно несколько альтернатив, таких как коммутатор ATM, коммутатор быстрого эфира и маршрутизатор с аппаратной коммутацией. Для локальной сети этажа и локальной сети рабочей группы быстрый эфирный коммутатор подходит с точки зрения стоимости и простоты управления. Маршрутизатор с аппаратной коммутацией является кандидатом на роль узла магистральной сети передачи данных из-за его эффективности и совместимости с современной IP-технологией.
Маршрутизатор с аппаратной коммутацией является кандидатом на роль узла магистральной сети передачи данных из-за его эффективности и совместимости с современной IP-технологией.
Однако ATM лучше других технологий коммутации с точки зрения качества обслуживания (QoS) и эффективности передачи в глобальной сети (WAN), которая обрабатывает трафик данных и голосовой трафик. В магистральных сетях предприятия также требуется высокая надежность. Дублирование линии доступно в технологии ATM, а быстрая установка альтернативного пути с использованием сигнализации будет стандартизирована [2], чтобы узлы ATM могли достичь более высокой надежности. Кроме того, в ATM стандартизированы различные функции управления трафиком [1], так что ATM позволяет эффективно использовать ресурсы в магистральной сети, в которой должен обрабатываться большой объем трафика, и в глобальной сети, в которой стоимость связи относительно высока.
Мы разрабатываем коммутатор с общим буфером для узлов ATM 4, 5, 6, 7, 8, 9, 10. На коммутаторе с общим буфером каждый выходной порт совместно использует буфер в коммутаторе, что позволяет повысить производительность при потере ячеек. чем другие схемы буферизации, такие как буферизация ввода и буферизация вывода 3, 4. Переключатель общего буфера выполняет управление записью и чтением буфера централизованно и может снизить стоимость реализации сложных функций управления трафиком по сравнению с реализацией для каждого порта. схемы буферизации [9]. Мы разработали крупномасштабный корпоративный банкомат на основе архитектуры коммутатора с общим буфером. В узле функции управления трафиком для каждого виртуального канала реализованы с низкими затратами за счет централизованного управления записью и чтением буфера.
На коммутаторе с общим буфером каждый выходной порт совместно использует буфер в коммутаторе, что позволяет повысить производительность при потере ячеек. чем другие схемы буферизации, такие как буферизация ввода и буферизация вывода 3, 4. Переключатель общего буфера выполняет управление записью и чтением буфера централизованно и может снизить стоимость реализации сложных функций управления трафиком по сравнению с реализацией для каждого порта. схемы буферизации [9]. Мы разработали крупномасштабный корпоративный банкомат на основе архитектуры коммутатора с общим буфером. В узле функции управления трафиком для каждого виртуального канала реализованы с низкими затратами за счет централизованного управления записью и чтением буфера.
В этом документе мы показываем системную конфигурацию разработанного узла ATM и объясняем детали функций управления трафиком для каждого виртуального канала, т. е. управление параметрами использования (UPC), отбрасывание на уровне ячеек, отбрасывание на уровне пакетов, маркировка управление и управление чтением буфера. Мы также показываем результаты производительности управления ABR (доступной скоростью передачи данных) в среде WAN с использованием узла.
Мы также показываем результаты производительности управления ABR (доступной скоростью передачи данных) в среде WAN с использованием узла.
Остальная часть этого документа организована следующим образом. В разделе 2 мы описываем системную конфигурацию разработанного узла ATM и коммутатора с общим буфером. В разделе 3 мы объясняем детали UPC, управления записью в буфер, управления маркировкой и управления чтением буфера. Результаты производительности управления АБР с помощью узла показаны в разделе 4. В заключение делается вывод в разделе 5. Система состоит из соединительной части, общих буферных коммутаторов, линейных интерфейсов (LIF) и управляющей части. Коммутатор с общим буфером основан на архитектуре коммутатора с общей буферной памятью 4, 5, 6, 7, 8, 9., 10, а пропускная способность 5 Гбит/с. Путем подключения коммутаторов с общим буфером с помощью соединительной части пропускная способность системы увеличивается до 20 Гбит/с масштабируемым образом. Соединение
В этом разделе мы объясняем детали функций управления трафиком в коммутаторе с общим буфером.
Одной из основных проблем службы ABR является производительность в среде с большой задержкой в оба конца, такой как WAN. При управлении с обратной связью ABR уведомления о перегрузке принимаются исходным терминалом с определенной задержкой. Поэтому необходимо выделить достаточный размер буфера и настроить параметры ABR, чтобы минимизировать потери при перегрузке. Однако задержка прохождения туда и обратно довольно велика в среде WAN, так что может случиться так, что сеть станет несколько перегруженной.
Мы оценили
На магистральном узле корпоративной сети, который обрабатывает данные и голосовой трафик, требуются сложные возможности QoS, эффективность передачи и высокая надежность. Технология ATM удовлетворяет этим требованиям, и узел ATM является кандидатом на роль магистрального узла предприятия. Мы разработали крупномасштабный корпоративный банкомат на основе архитектуры коммутатора с общим буфером. В узле функция управления трафиком для каждого виртуального канала реализована с низкими затратами с использованием централизованного управления буфером 9. 0419
0419
Нобору Эндо получил BE, ME и DE. степени Университета Тохоку, Сендай, Япония, в 1981, 1983, 1986 годах соответственно. В 1986 году он присоединился к Центральной исследовательской лаборатории Hitachi, Ltd., где в настоящее время является старшим научным сотрудником отдела исследований сетевых систем. С тех пор он занимается исследованием и разработкой сетей с быстрой коммутацией пакетов и сетей ATM. С января 1990 г. по август 1991 г. он был приглашенным инженером Bell Communications Research, Red Bank, New 9.0419
Ссылки (12)
В полной текстовой версии этой статьи есть дополнительные ссылки.
Нобору Эндо получил награды B.E., M.E. и D.E. степени Университета Тохоку, Сендай, Япония, в 1981, 1983, 1986 соответственно. В 1986 году он присоединился к Центральной исследовательской лаборатории Hitachi, Ltd., где в настоящее время является старшим научным сотрудником отдела исследований сетевых систем. С тех пор он занимается исследованием и разработкой сетей с быстрой коммутацией пакетов и сетей ATM. С января 1990 г. по август 1991 г. он был приглашенным инженером Bell Communications Research, Red Bank, Нью-Джерси. Его исследовательские интересы включают управление трафиком и оценку производительности высокоскоростных мультимедийных сетей. Доктор Эндо является членом IEEE, Института инженеров по электронике, информации и связи (IEICE) Японии и Японского общества обработки информации.
Доктор Эндо является членом IEEE, Института инженеров по электронике, информации и связи (IEICE) Японии и Японского общества обработки информации.
Такеши Аимото получил награду B.E. и степени ME Токийского университета, Токио, Япония, в 1980 и 1982 годах соответственно. В 1982 году он присоединился к Центральной исследовательской лаборатории Hitachi, Ltd., где в настоящее время является старшим научным сотрудником отдела исследований сетевых систем. С тех пор он занимается исследованиями и разработками в области архитектуры высокоскоростных пакетных сетей и управления трафиком, включая ATM. Г-н Аймото является членом Института инженеров по электронике, информации и связи (IEICE) Японии и Японского общества обработки информации.
Такеки Ядзаки получил B.S. степень Токийского технологического института, Токио, Япония, в 1993 году, и степень магистра. получил степень в Токийском университете, Токио, Япония, в 1995 году. С тех пор как он присоединился к Центральной исследовательской лаборатории Hitachi, Ltd. в 1995 году, он занимается исследованиями и разработками в области управления трафиком в сетях с быстрой коммутацией пакетов и сетях ATM.
получил степень в Токийском университете, Токио, Япония, в 1995 году. С тех пор как он присоединился к Центральной исследовательской лаборатории Hitachi, Ltd. в 1995 году, он занимается исследованиями и разработками в области управления трафиком в сетях с быстрой коммутацией пакетов и сетях ATM.
Томихиса Нисидзима родился в 1947 году. Он начал работать в компании Hitachi, Ltd. в 1965 году, где в настоящее время является старшим инженером системного отдела подразделения компьютеров общего назначения. С тех пор он в течение тридцати лет занимается исследованием и разработкой новейших систем связи, то есть обмена данными с временным разделением, системы коммутации пакетов, корпоративной системы, системы коммутации банкоматов и процессора управления связью для мейнфреймов. Его исследовательские интересы включают алгоритмы маршрутизации пакетов и новейшие системы связи в фургоне новой эры. Г-н Нисидзима является членом Института инженеров по электронике, информации и связи (IEICE) Японии. Просмотреть полный текст
Просмотреть полный текст Copyright © 1999 Elsevier Science B.V. Все права защищены.
Калькулятор пробега Tachosoft 23.1 Скачать бесплатноAuto Repair Technician Home
Что такое калькулятор Tachosoft?
Калькулятор пробега TachoSoft в настоящее время является одним из крупнейших в мире цифровых калькуляторов одометра. Он охватывает более 2246 моделей автомобилей! Он прост в использовании для всех, от новичка до профессионала.
Tachosoft Calculator V23.1 Free Download:
https://mega.nz/#!hLRnQIib!fxDC2UnXr0lleYTRqy72e9h5AoHfdTPuwGkXi7QVsKY
Tachosoft Mileage Calculator V21.5 ( Tested Work 100% )
http ://www.uobdii.com/wholesale/tachosofts-mileage-calculator.html
Tachosoft Calculator Полезные советы:
более одного типа, необходимо искать тот, который находится ближе к дисплею или микропроцессору.
2. Некоторые микросхемы имеют защиту от чтения, используйте программаторы, которые могут обходить эту защиту.
3.После того, как вы прочитали дамп с микросхемы памяти, посмотрите его содержимое. Если есть только нули или FF, это означает, что дампы были неправильно прочитаны.
4.После чтения чипа ОБЯЗАТЕЛЬНО делайте резервную копию файла дампа.
5. Попробуйте записать откалиброванный дамп в новый чип, чтобы у вас всегда был оригинальный чип для бекапа.
6.Прежде чем менять пробег, посчитайте на калькуляторе первоначальный пробег и сравните его с тем, который записан в оригинальном дампе.
7.Рассчитанные и считанные пробеги могут отличаться в следующих случаях:
а.Возможно, необходимо поменять местами старший и младший байты (сделать SWAP)
Пример: ABCD -> CDAB
б.Поскольку Как правило, методы расчета пробега являются коммерческой тайной производителей приборных панелей, поэтому представленные здесь алгоритмы являются формулами, рассчитанными лично нами, и иногда имеют точность +- 250 км (миль). Это не обязательно при калибровке, но вы должны учитывать этот факт при сравнении исходного и расчетного пробега.
Это не обязательно при калибровке, но вы должны учитывать этот факт при сравнении исходного и расчетного пробега.
c.Производитель приборной панели иногда может менять оффсеты, где пробег хранится в микросхеме памяти, поэтому в случае несоответствия смотрите весь дамп целиком.
Tachosoft Calculator Support Vehicle List:
Acura
Acura 3.5 LTR – 2x 93c46 – 1997 year
Acura 3.5 LTR – 2x 93c56
Acura CL – 96c56 – 2001-2003 years
Acura MDX – 93c56 – 2002 год
Acura MDX — 93c66 — 2006 год
Acura MDX — 93c76 — 2007-2008 годы
Acura RDX – 93c66 – 2007 year
Acura RL – 93c66
Acura RSX Type S – 93c46 – 2002 year
Acura RSX – 93c56
Acura TL – 93c46
Acura TL – 93c56 – 2003 year
Acura TL – 93c66
Acura TSX – 93c46
Acura TSX – 93c66 – 2006 year
Acura TSX – 93c86 – 2008 year
Admiral
Admiral – 24c01
Alfa Romeo
Alfa Romeo 145/146 – ST6249 C6/N4 – 1995-1996 years
Alfa Romeo 145/146 — 68HC(7)05B16 — 1998 год
Альфа Ромео 147 — ST6249
Alfa Romeo 147-NEC-2001 год
Alfa Romeo 147-93C86-2001-2002 годы
Alfa Romeo 147-93C86-с 2002 года
Alfa Romeo 156 Type 1-68HC711KG4-до 2001 года
6646. – from 2002 year
– from 2002 year
Alfa Romeo 159 – 93c86 – 2006 year
Alfa Romeo 164 – 68HC05B6 – 1994-1995 years
Alfa Romeo 164/166 – 68HC11
Alfa Romeo 166 – 93c56
Alfa Romeo 166 – 93c56 – 2000 year
Alfa Romeo 166 — 68HC11KG4 — 1999 год
Альфа Ромео Брера — 93c86 – 2007 year
Alfa Romeo GTV – 68HC05B6 – 1995 year
Alfa Romeo MiTo – 24c16
Alfa Romeo Spider – 93c86 – 2001 year
Alfa Romeo Spider – 93c86 – 2006 year
Audi
Audi A2 VDO – 93c86 – 2001 year
Audi A3 UK NSI — 93c56
Audi A3 / A4 Jaeger — 68HC912
Audi A3 Type 1 — 93c66 — 1997-1999 гг.
Audi A3 Type 2 — 93c66 — 1997-1999 гг. 68HC912 — 2003 год
Audi A3 — 93c86 — 2003 год
Audi A3 — 93c86 — 2004 г.в.
Audi A4 Bosch — 24c08 — 2001 г.в.
Audi A4 VDO (без MFA) — 93c46 — 1994-1997 гг. UK NSI – 93c56 – 1995-1997 гг.
Audi A4 UK NSI – 93c56 – 1997-1998 гг.
Audi A4 UK NSI new – 93c56
Audi A4 Type 1 – 93c66 – 1997-1999 гг. -1999 г.р.
-1999 г.р.
Audi A4 – 93lc86 – мод. 2000 г.в.
Audi A4 — 93c86 — мод. 2000 год
Ауди А4 — 68HC912
Audi A4 – 68HC912DG128A
Audi A6 VDO – 93c46 – 1994-1997 гг.
Audi A6 UK NSI – 93c56 – 1995 г.в.
Audi A6 UK NSI – 93c56 – 1997-1998 гг. years
Audi A6 Type 2 – 93c66 – 1997-1999 years
Audi A6 VDO – 93c86 – 1999-2001 years
Audi A6 – 68HC912DG128 – 2000-2001 years
Audi A6 – 68HC912DG128A
Audi A6 Type 2 – 68HC912DG128A
Audi A6 – 24c32 — 2007 год
Audi A8 VDO — 93c56 — до 10.1996
Audi A8 VDO — 93c66 — 1998 год
Audi A8 VDO — 93c86 — 2001 год
Audi A8 VDO — 93c86 — 2003 год
Audi A8 — 24c17 — 1999 год
Audi A8 — 24c17 — 2001 год
Audi A8 — 892 — 93c46 986 984 -2000 years
Audi TT- 68HC912DG128A
Audi 100 TDI – 93c46 – 1995 year
BMW
BMW CAS MODULES
BMW CAS2 (old) – 9s12DG256
BMW CAS2 (new) – 9s12DG256
BMW CAS3 – 9s12DG256
BMW CAS3 – 9S12XDP
МОДУЛИ BMW EWS
BMW EWS3 SW ?? — 68HC11EA9– 1997-2006 years
BMW EWS3 SW 08 – 68HC11EA9 – 1997-2003 years
BMW EWS4 – MC9S12DG64
BMW EWS 4. 3 – MC9S12D64
3 – MC9S12D64
BMW LCM MODULES
BMW LCM – 68HC11PH8 – 2003 year
BMW LCM2 – 68HC711P2
BMW LCM3 – 68HC912D60
BMW LCM4 – 9S12D64 – 2006 year
BMW 316-320 VDO – 93lc56 – 1991-1995 year
BMW 318 – 93c56
BMW 320 Coupe – 93c56 – 1994 year
BMW 325 TDS – 93c56
BMW 525i – 93c46
BMW 3xx Compact Innen — 93c46 — 1995 год
BMW 3XX Compact Aussen-93C46-1995 год
BMW 3XX E36-93C46-1998 год
BMW 3XX-M35080-2001-2002 годы
BMW 3XX-M35080-от 2002 года
46 BMW 5x 5XX, 7x, 7x, 7x, 7x46-9x306-9x46-9x46-9x46-9x46-9x46-9x46-9x46-9x46-9x46-9x46. 7xx СИНИЙ – 93c56
BMW 5xx ЗЕЛЕНЫЙ – 24c02
BMW 5xx – M35080 – 2001-2002 годы
BMW 5xx – M35080 – с 2002 года
BMW E36 – 93c56 – до SW 20 — 93c46 — SW 24 innen
BMW E36 — 93c46 — SW 24 Aussen
BMW E39 Low — 93c56 – до SW 10
BMW E39 Low – 93c56 – SW 11
BMW E39 Low – 93c56 – SW 12
BMW E39 Low – 93c56 – SW 15
BMW E39 Low – 93c66 – SW 16
BMW E38/E39 IKE SW 12 – 93c56
BMW E38/E39 IKE SW 13 – 93c56
BMW E38/E39 IKE SW 14 – 93c56
BMW E38/E39 IKE SW 15 – 93c56
BMW E38/E39 High – 93c56 – SW 05 / SW 07 BMW E High – 93c56 – SW 11
BMW E38/E39 High – 93c56 – до SW 12
BMW E38/E39 High – 93c56 – SW 13
BMW E38/E39 High – 93c56 – SW 14
BMW E38/E39 High – 93c56 – SW 15
BMW E38/E39 High – 93c66 – SW 12, SW 13
BMW E46 – (Dash+LCM+EWS) – 2003 год
BMW E46 – (Dash+LCM+EWS) – 2004 год
BMW E53 X5 – (Dash+CAS2)
BMW E60 5xx – (Dash+CAS) – 2005 год
BMW E63 6xx — (Dash+CAS) — 2005 год
BMW E65 7xx — (Dash+CAS) — 2003 год
BMW Z3 салон — 93c46
BMW Z3 салон — 93c56 — SW 9, 10
BMW Z3 Aussen — 93C46
Brilliance
Brilliance M2 - 24C04
Buick
Buick Allure - 9S12H228
Buick Anclave - 93–66
Buick Lacrosse - 24C16 - 2010 год
6666. 1466 - 246 - 2010 год. Buick Park Century – 25010
1466 - 246 - 2010 год. Buick Park Century – 25010
Buick Regal –
– 1998 year
Buick Rendezvous – 25020
Buick Riviera – TC
P – 1996 year
Cadillac
Cadillac All – 68HC11E9 – 1992-1996 years
Cadillac CTS – 93c66 – 2003-2006 years
Cadillac CTS — 93c86 — 2008-2009 г.в.
Cadillac Deville Type 1 — 93c46 — с 2000 г.в. 2004 Годы
Cadillac DTS Тип 1-93C46-2000-2003 годы
Cadillac DTS Тип 2-93C46-2000-2003 годы
Cadillac DTS-93C56-2002 год
Cadillac DTS-93C46-2005-2006 годы
Cadillac-93C46-2005-2006 годы
. 2008-2009 гг.
Cadillac Escalade –
– 2000-2002 years
Cadillac Escalade –
– 2003 year
Cadillac Escalade – 25020 – 2005 year
Cadillac Escalade (hours) – 25020 – 2005 year
Cadillac Escalade – 93c46 – 2007 year
Cadillac Eldorado – 68HC11E9 – 1994-1998 Годы
Cadillac Seville - 68HC11F1 - с 1997 года
Cadillac Seville Тип 1 - 93C46 - с 2000 года
Cadillac Seville Type 2 - 93C46 - с 2000 года
Cadillac SRX - 93C66 - 2005 год
Cadillac - 93c66666666666 годы - 2006 - 2006 год - 93 - 2006 - 2006 год - 2006 - 2006 - 2006 год. СТС – 93C46-2005 год
СТС – 93C46-2005 год
Cadillac STS-93C86-2008 год
CHERY
CHERY ECU
ECU BOSCH 797-
ECU BOSCH 797 (часы)-
Chery A15. 93c66
Chery A15 Cowin – 93c66
Chery A21 Fora – 93c66
Chery A21 Fora – 93c66 – 2007 year
Chery MS25 – 93c66 – 2005 year
Chery S14 – 93c66 – 2002 year
Chery T11 Tiggo – 93c66
Chevrolet
Chevrolet Alero –
Chevrolet Astro — 25020 — 1999-2000 гг.
Chevrolet Avalanche —
— 2007 г.в.
Chevrolet Avalanche (часы) —
— 2007 г.в. Chevrolet Aveo — 24c08 — 2007-2008 гг.
Chevrolet Blazer — 42926 — 1997-2000 гг. - 24с16
Шевроле Камаро —
Шевроле Камаро —
— 1999-2001 гг.
Шевроле Каприс — NEC — 1999-2002 гг. — 2007-2008 гг.
Chevrolet Captiva — 9s12HZ256
Chevrolet Captiva — 93c86 — 2010 г.
Chevrolet Cavalier — 68HC11E9 — 1999 г.4646 Шевроле Кобальт –
– 2004-2005 гг.
Шевроле Кобальт –
– 2006 г. в.
в.
Шевроле Колорадо – 93c56 – 2004 г.в. 25020 — 1998 год
Шевроле Корвет — 93c76 — 2005 год
Шевроле Корвет — 68HC11A8
Шевроле Круз — 24c16
Шевроле Круз (BCM) — 24c16 93c56 – 2009 year
Chevrolet Epica – 68HC05h22
Chevrolet Equinox BCU – 68HC908AZ60
Chevrolet Equinox BCU – 68HC908AZ60 – 2005 year
Chevrolet Equinox – 93c66 – 2007-2008 years
Chevrolet Evanda – 68HC05h22 – 2003-2005 years
Chevrolet Express – 68HC11E9 – 2001-2003 гг.
Шевроле Экспресс — 24c04
Шевроле Экспресс (часы) — 24с04
Шевроле Экспресс — 25020
Шевроле Импала — 68HC912B32 — с 2000 г.в.
Шевроле Импала —
Шевроле Джимми — 42926 – 1997-2000 гг.
Chevrolet HHR BCU – 25080 – 2007-2008 гг.
Chevrolet Kalos – 68HC05h22
Chevrolet Lacetti – 93c46 – 2004-2007 гг. —
— 2003 г.в.
Chevrolet Lumina — 93s56 — 1999-2002 гг.
Chevrolet Lumina — NEC — 1999-2002 гг. – 1998-2000 г.в.
Шевроле Малибу — 68HC912B32 — с 2000 г. в. Монтана-68HC912B32-1999-2002 годы
в. Монтана-68HC912B32-1999-2002 годы
Chevrolet Monte Carlo-68HC912B32-с 2000 года
Chevrolet Nubira-93C46
Chevrolet Optra-93C46-2005-2006 годы
Chevrolet Optra-93C46-2005-2006 годы
Chevrolet Optra-93C46-2005-2006 годы
-–946-
-93c46-2005-2006 годы.4646 Шевроле Омега —
— 2008 г.в.
Шевроле Пикап — 25020 — 1999-2002 гг. Chevrolet Savana — 68HC11E9 — 2001 г.в.
Chevrolet Silverado — 93c46
Chevrolet Silverado —
— 2004-2007 гг. ) –
-2007-2008 годы
Chevrolet Spark-68HC05H22-2007
Chevrolet Suburban-
-2007 год
Chevrolet Suburban (Hours)-
-2007 год
Chevrolet Tacuma-68HC05H22-Год
.
Chevrolet Tahoe —
— 2004-2005 г.в.
Chevrolet Tahoe —
— 2007 г.в.5080-2007 год
Chevrolet Trailblazer (часы)-
-2007 год
Chevrolet Traverse-24C04-2009-2010 лет
Chevrolet Uplander-9S12H28-2005-2007 годы
Chevrolet Uplander-9S12H356-2007-годы
. -2002 years
Chevrolet Vivant – 68HC05h22 – 2003-2005 years
Chrysler
Chrysler 300C – 9S12DG256 – 2005-2007 years
Chrysler 300C (hours) – 9S12DG256 – 2005-2007 years
Chrysler 300M BSI Type 1 – 68HC11K4 – until 2000 9 год4646 Chrysler 300M BSI Type 2 – 68HC11K4 – until 2000 year
Chrysler 300M BSI – 68HC912B32 – until 2004 year
Chrysler Cirrus BSI – 68HC11E9 – 1995 year
Chrysler Concorde BSI – 68HC912B32
Chrysler Crossfire – 93c66
Chrysler Interpid – 68HC12B32 – 2004 year
Chrysler Neon - 68HC11E9 - 2001 год
CHRYSLER NEON - 68HC912 - 2001 год
CHRYSLER NEOON - 68HC908AS60 - 2002 год
Chrysler Pacifica BSI - 68HC912B32
Chrysler Plycila BSI - 68HC912B32
Hrysler Plycla Plycla - 68HC912B32
Hrysler Plycla Plycla - 68HC912B32
Hrysler Plycla Plycla PLICICLA - 68HC912B32
Plysler PLICLISLA PLICLISL– 2001 year
Chrysler PT Cruiser – 68HC912B32 – 2002 year
Chrysler Sebring BSI – 68HC912B32
Chrysler SRI – 25040
Chrysler SRI – 25040
Chrysler Stratus BSI – 68HC11E9 – 1996-1998 years
Chrysler Town Country BSI – 68HC912B32 – 2003 year
Chrysler Voyager BSI-68HC11E9-1996-1998 годы
Chrysler Voyager BSI-68HC11K4-1998-1999 годы
Chrysler Voyager BSI-68HC912B32-2000-2004 года
16.
-2000-2004 годы
16.
-2000-2004 годы
16646-2000-2004 годы
646-2000-2004 годы
.4646 Citroen C2 – (Dash+BSI) – 2003-2004 гг.
Citroen C2 – (Dash+BSI) – 2006 г.в. 2004 года
Citroen C3 Dash Type 1 – 93c56
Citroen C3 Dash Type 2 – 93c56
Citroen C3 – (Dash+BSI) – 2006 год
Citroen C3 – (Dash+BSI) – 2007 год
Citroen C4 – (Dash+BSI) ) — 2005 г.
Citroen C4 Type 1 — (Dash+BSI) — 2006 г.
Citroen C4 Type 2 — (Dash+BSI) — 2006 г.
Citroen C4 — (Dash+BSI) — 2007 г.
Citroen C4 Picasso — (Dash+BSI) — 2008 г.в.
Citroen C5 — (Dash+BSI) — 2000-2001 гг. — 2002 год
Citroen C5 — (Dash+BSI) — 2003 год
Citroen C5 — (Dash+BSI) — 2004 год
Citroen C5 Dash — 68HC908AZ60 — 2001-2006 годы
Citroen C5 BSI —
— 2004 год Citroen C5 9456 BSI Type 1 —
— 2006 г.
Citroen C5 BSI Type 2 —
— 2006 г.
Citroen C6 — (Dash+BSI) — 2006 г.
Citroen C8 — (Dash2+Dash3+BSI) — 2003-2004 гг.
Citroen C8 — (Dash2+Dash3+BSI) — 2006 г.
Citroen Dispatch — 68HC05h22 — 2003 г. BSI) — 2001-2002 гг.
Citroen Berlingo — (Dash+BSI) — 2000-2003 гг.
Citroen Berlingo — (Dash+BSI) — 2001-2006 гг.
Citroen Evasion — 68HC05h22 — 2000 г. Jumpy — 68HC08AZ32 — 2003-2004 годы
Citroen Jumper — ST
– 2002- 2003 гг.
Citroen Picasso (Dash+BSI) – 2000-2003 гг.
Citroen Picasso (Dash+BSI) – 2000-2002 гг.
Citroen Xsara — (Dash+BSI) — 93c66 — 2000-2003 гг.
Citroen Xsara — (Dash+BSI) — 2001 г.
Citroen Xsara — (Dash+BSI) — 2000-2003 гг. ) — 2005
Citroen Xsara Picasso — 2003 год
Citroen Xsara Picasso — (Dash+BSI) — 2001-2003 годы
Citroen Xsara Picasso — (Dash+BSI) — 2003-2005 гг.
Citroen Xsara Picasso — (Dash+BSI) — 2006 г. – 25020 – 2007-2009 years
Dacia Sandero – 25020 – 2009 year
Daewoo
Daewoo Evanda – 68HC05h22
Daewoo Kalos – 68HC05h22
Daewoo Magnus – 68HC05h22 – 2001 year
Daewoo Matiz – 68HC05h22
Daewoo MVM – 93c66
Daewoo Rezzo – 68HC05h22 — 2006 г.
Daewoo Tacuma – 68HC05h22
Daewoo Winstorm – 9S12HZ128 – 2007-2008 years
Daewoo Winstorm – 9S12HZ256
DAF
DAF LDV – 93c46 – 2004 year
Daihatsu
Daihatsu Altis – 93c46
Daihatsu Boone – 93c56
Daihatsu Cuore – 93c46
Daihatsu Delta — 93c56
Daihatsu Mira — 93c46
Daihatsu Mira — 93c56 — 2005 год
Daihatsu Sirion — 93c66 — 2008 год
Daihatsu Storia — 93c46
Daihatsu Terios — 93c46
Daihatsu Terios3c56 – 2008 year
Daihatsu YRV – 93c46
Dodge
Dodge Avenger – 9S12h356 – 2008 year
Dodge Caliber – 9S12h356 – 2007 year
Dodge Caliber – 9S12DG256
Dodge Caravan BCM – 68HC11E9 – 1996-1998 years
Dodge Caravan BCM – 68HC912B32
Dodge Caravan-9S12H356
Dodge Charger-9S12DG256-2005-2007 лет
Dodge Charger (часы)-9S12DG256-2005-2007 лет
Dodge Cherokee Sport-1998 год.S12DG256C-2008 год
Dodge Durango-93C46-1998-2002 годы
Dodge Durango-9S12DG128B-2004-2005 лет
Dodge Durango-9S12DG256-2005-2007 лет
Durango-9S12DG256-2005-2007 лет
DURANGO (9S12DG256-2005-2007 лет
DURANGO (9S12DG256-2005-2007 лет. Caravan BCM – 68HC11E9 – 1996-1998 years
Caravan BCM – 68HC11E9 – 1996-1998 years
Dodge Magnum – 9S12DG256 – 2005-2007 years
Dodge Magnum (hours) – 9S12DG256 – 2005-2007 years
Dodge Neon – 68HC908AS60 – 2002-2003 years
Dodge Ram Pickup – 93c46 – 1998 -2001 год
Пикап Dodge Ram – MC9S12DG256 - 2006 год
Dodge Ram Van BCM - 68HC11KA4
Dodge RAM 1500 Hemi - MC9S12DG256 - 2006 год
Dodge Ram 2500 - 93C46 - 2001 год
Dodge Ram 2500 - MC9S12H356 - 2001 год 9466. 9466. 9466. 9466. 9466. 9466. 9466 Dodge Dodge Dodge 2500 - MC9S12H356 - 2009 год 9466. 9466 Dodge Dodge Dodge 2500 - MC9S12H356 - 2009 год 9466. 9466 Dodge Dodge Dodge. 2001 год
Dodge Stratus BCM-68HC11E9-1996-1998 годы
Dodge Stratus BCM-68HC912B32-2001 год
Dodge TJ/Wrangler-1998 год
FAW
FAW FERMARK-24C0419
FAW
FAW FERMARK-24C0419
FAW
FAW FRAW.
Fiat
Fiat Adventure – ST
– 2004 year
Fiat Adventure –
– 2006 year
Fiat Albea – 25040
Fiat Albea –
Fiat Brava, Bravo, Marea UK NSI Type 1 – 93c56 – 1998 year
Fiat Brava, Bravo , Marea UK NSI Type 2 – 93c56 – 1998 г. в.
в.
Fiat Brava, Bravo – ST6249(5) – 1997 г.в.
Fiat Brava, Bravo — 68HC908AZ60 — 1998-2000 гг.
Fiat Bravo —
– 2007 year
Fiat Doblo Type 1 – ST
– 2001-2006 years
Fiat Doblo Type 2 – ST
– 2001-2006 years
Fiat Doblo – 68HC908AZ32
Fiat Doblo –
– 2007 year
Fiat Ducato –
– 2002 year
Fiat Ducato-
-2007 год
Fiat Ducato-
-2008 год
Fiat Cinquecento-
-2007 год
Fiat Croma-
-2005 год
Fiat Grande Punto-
-2006-2007 годы
Fiat Idea-9508-
-2006-2007 годы
Fiat-9508-
-20066 годы
. 2007 г.в.
Fiat Idea –
– 2007-2008 г.в.
Fiat Marea – ST6249 – 1996-1997 гг.
Fiat Marea – 68HC(7)05E6 – 1996-1999 гг.
Fiat Marea – 68HC908AZ60 – 2000HC г.в. 1999-2001 г.в.
Fiat Marea Exclusive – 68HC08AZ32 – 2004 г.в.
Фиат Палио — ST
Фиат Палио — 25040 — 2004 год
Fiat Palio-ST
-2004-2005 годы
Fiat Palio-
-2005-2007 годы
Fiat Palio-
-2007-2008 годы
Fiat Panda-ST
-2004 год
Fiat Panda-
-2006 год
-2004 год
-
-2006 год 9466-2004 год
.
Fiat Punto - ST
- 2002 год
Fiat Punto 2 типа 1 - ST
- 2002 год
Fiat Punto 2 типа 2 - ST
- 2002 год
Fiat Punto 2 - ST
- 2002 год
Fiat Punto 2–68HC908 - 2002 год
Fiat Punto 2–68HC908 - 2002 год
Fiat Punto 2–68. Фиат Пунто 3 — ST
Фиат Пунто —
-2007 год
Fiat Scudo-ST
Fiat Scudo-68HC05H22
FIAT SCUDO-68HC908AZ32-2000 год
FIAT SCUDO-(DASH+BSI)-2007-2008 годы
FIAT SEDICI-93-93-2006-2006 год. 2002 year
Fiat Seicento – ST25040
Fiat Stilo – 68HC912D60 – 2003-2004 years
Fiat Stilo – 9S12h228 – 2006-2008 years
Fiat Stilo – 9s12h356
Fiat Strada –
– 2005-2006 years
Fiat Strada –
– 2007- 2008 г.в.
Fiat Tempra – 93c06
Fiat Tempra – 93c46
Fiat Tempra Veglia – 93c06
Fiat Tempra Borg – 93c46
Fiat Tipo Veglia – 93c46
Fiat Tipo Borg – 93c46 – 1996 year
Fiat Ulysse – 68HC05h22 – 1998 year
Fiat Ulysse – (Dash2+Dash3+ BSI) — 2002-2004 гг.
Fiat Ulysse — (Dash2+Dash3+BSI) — 2006 г.
Ford
Ford AeroStar — 93c06 — 1992-1997 гг. 2000 год
Форд Курьер — 68HC912D60
Ford Courier-NEC UPD780973
Ford Crown Victoria-68HC11E9-1995-2001 годы
Ford Crown Victoria-9S12DT256-2008 год
Ford E Series-93C06-1992-1997 лет
FORD E250-93C06-1992-1997 лет
FORD E250-93C06-1992-1997 годов
E250-93C06. -9S12H356
FORD ECOLINE-9S12DT256C
FORD ECOSPORT-24U09
FORD ECOSPORT-24U17
FORD ECOSPOR – 2000-2002 годы
Ford Escape-MC9S12H228VFV-2004-2005 годы
Ford Escape-9S12ZH356
Ford Escort-68HC11E9-2000 год
Ford Expedition-68HC11-1999-2001 года
Ford Expediation-68HC91-1999-2001 года
FORD Expediation-68HC91-1999-2001 года
FORD Expediation-68HC911-1999-
Ford Expediation-68HC91-1999-2001 год
FORD. Форд Экспедишн — 93с46 — 2006 г.в.
Форд Экспедишн — 93с86 — 2007-2008 г.в.4646 Ford Explorer — 9S12h356
Ford Explorer — MC9S12DP256 — 2004-2005 г. в.
в.
Ford Explorer — 93c46 — 2005 г.в.
Ford Explorer — 93c86 — 2005-2007 г.в. -1997 г.в.
Ford F-150 – 68HC11E20 – 1999-2004 гг.
Ford F-150 Super Crew – 68HC912D60 – 2002 г.в. — 9С12х228ВФВ — 2004-2005 гг.
Ford F-150 New Body Style — 9S12DP256 – 2004 г.в.
Ford F-150 – 24c16 – 2009 г.в.
Ford F-250 – 9S12DG128 – 2005 г.в. 68HC912D60
Ford F-350 – 9S12h228
Ford F-350 – 9S12DG128 – 2008 year
Ford F-450 – 9S12DG128 – 2008-2009 years
Ford F-500 – 9S12h228
Ford Falcon – 93c46
Ford Fiesta – 68HC11E20 – 1999- 2000 лет
Ford Fiesta — 24c08 — 2002-2003 годы
Ford Fiesta — NEC uPD780973 – 2001-2003 years
Ford Fiesta – 24U09
Ford Fiesta – 24U17 – 2004 year
Ford Fiesta – 24c08 – 2005 year
Ford Fiesta – 9S12h356 – 2005 year
Ford Fiesta – 9S12h356 – 2006 year
Ford Fiesta – 9S12DT256
Ford Fiesta – 24c08 – 2008 г.в.
Ford Fiesta – 9S12HZ256 – 2009-2011 гг.
Ford Flex – 93c66 – 2008-2009 г. в. 2003-2004 годы
в. 2003-2004 годы
Форд Фокус Тип 1 — 24c16 — 2006 год
Форд Фокус Тип 2 — 24с16 — 2006 г.в.
Форд Фокус — 24с16 — 2007 г.в. – MC9S12h356 – 2005 year
Ford Focus – 9S12DT256
Ford Focus – 9s12XHZ512 – 2008-2009 years
Ford Focus Ghia – MC9S12h356
Ford Focus C-Max – MC9S12h228
Ford Focus C-Max Type1 – MC9S12h356 – 2003-2004 years
Ford Focus C-Max Type2 — MC9S12h356 — 2003-2004 гг.
Ford Focus C-Max — MC9S12HP256VPV — 2005-2006 гг.
Ford Focus C-Max- 9s12XHZ512 — 2008-2009 гг.
Ford Freestyle – 9S12h228
Ford Freestyle – 9S12h356
Ford Fusion – 24c08 – 2002-2004 years
Ford Fusion – MC9S12h356 – 2006 year
Ford Fusion – 93c66 – 2006-2007 years
Ford Fusion – 9S12DT256
Ford Fusion – 93c86 – 2010 Год
Форд Гэлакси — 68HC11E9— 1996-1998 гг.
Ford Galaxy — 68HC11E20 — 1997-1998 гг.
Ford Galaxy — 93c86 — 2000 г.
Ford Galaxy — 93c86 — 2002-2003 гг. 9S12DP512-2009 год
Ford GT-24C08-2006 год
Ford KA-NEC UPD780973-2004 год
FORD KA-93C56-2009 год
FORD KUGA-9S12XHZ512-2008-2009 годы
для LINCA-9S12XHZ512-2008-2009 годы 9466 для LINC-68-63HS13-63HS13-63HS11-63-67-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-63-х года. — 24c16 — 2009 год
— 24c16 — 2009 год
Ford Lynx — 93c56
Ford Maverick – 68HC05L28
Ford Maverick – 68HC711KS2
Ford Maverick – 9S12h228
Ford Mondeo – 68HC912D60 – 2001-2006 years
Ford Mondeo – 24c16 – 2006-2007 years
Ford Mondeo – 9s12h356 – 2008-2009 years
Ford Mondeo – 9s12DP512 – 2010 year
Ford Mustang – 68HC11E9 – 1999-2003 years
Ford Mustang – 9s12h228 – 2005-2006 years
Ford Mustang GT – 9s12dj128 – 2006 year
Ford Mustang – 9s12DJ128 – 2005 year
Ford Mustang – 9s12DJ128 – 2008 year
Ford Mustang-24C16-2010 год
Ford Puma-68HC11E9-1999-2001 годы
Ford Ranger-68HC05L28-2000-2001 года
Ford Ranger-93C46-2004 год
FORD RANGE MC9S912DG256 - 2006 год
Ford Ranger - 93C56 - 2007 год
Ford Ranger - 93C66
Ford Scorpio - 68HC11E9 - 1995 год
FORD Super Duty - 68HC912D60 - 2004 год
- 2 -й пошлиной - MCS 2HS92H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2H2HS2HS2HS2012SLEAR 92 -го года 2 -го 2 -го 2 -й обязанности - MCS 2HC912H20 - 2004 год 92 -го 2 -го 2 -го 2 -го обязанности. 2005 год
2005 год
Ford Taurus – MC9S12h228VFV – 2004-2008 years
Ford Thunderbird – 68HC11KA4 – 2001-2002 years
Ford Transit Connect – 68HC912D60
Ford Transit Connect – 9s12h356 – 2007-2008 years
Ford Transit – 93c66
Ford Transit – 24c16 – 2003- 2004 Годы
Ford Transit-NEC UPD780973-2006 год
Ford Transit-93C76-2006-2007 лет
Ford Trucks-93C06-1992-1997 годы
Ford Trucks-68HC11E9-1999-002 года
Ford Trucks-68HC11E9-1999-002 годы
-68HC11E9-1999-1946 год. 68HC912D60
Ford Tourneo-24C16
Ford Van's All-93C06-1992-1997 лет
Ford Windstar Van-68HC11E9-1995-2001 годы
FORD WINDSTAR-68HC11KA4-1999-2002 годы
FORD WINDSTAR-68HC11KA4-1999-2002 годы
FORD WINDSTAR-68HC1KA4-1999-2002 годы
FORD WINDSTAR-68HC1KA4-1999-2002 годы
. - 68HC912B32
FORD WINDSTAR - 9S12DG128
GAZ (Volga)
Volga Chrysler - 25040
Geely
GEEL5020 — 2004 г.
GMC Savana — 24c04
GMC Savana (часы) — 24c04
GMC Sierra 2500 —
— 2007 г.
GMC Sierra Heavy Duty —
— 2007 г. GMC Yukon Denali –
– 2004 г.в.
GMC Yukon – 25020 – 2006 г.в.
GMC Yukon Denali (часы) – 25020 – 2006 г.в. лет
GMC Yukon Denali –
– 2007-2008 годы
GMC Yukon Denali (часов) –
– 2007-2008 гг.
Great Wall
Great Wall Hover – 24c04 – 2006-2007 гг. Lobo – 9s12h228 – 2008 year
Hino
Hino 238 – 93c46
Hino 258 – 93c46
Hino 268 – 93c46
Hino FB – 93c46
Hino Ranger – 93c46
Hino Yazaki – 93c46
Holden
Holden Barina – 93c56
Holden Barina – 68HC05h22
Honda
Honda Accord-93C46
Honda Accord-93C56-2000-2002 годы
Honda Accord V6-68HC05B16-2001 год
Honda Accord-93C56-2004-2005 годы
66666666666 гг. – 93c76 – 2007-2008 years
Honda Accord Torneo – 93c46
Honda Accord – 93c86 – 2008-2009 years
Honda Acty – 93c56
Honda Airwave – 93c66 – 2005 year
Honda Aria – 93c56
Honda ATX – 93c46
Honda Avancier – 93c56
Хонда Капа — 93c46
Honda City — 93c56
Honda City — 93c66 — 2006 г.
Honda City — 93c76 — 2010 г.
Honda Civic — 93c56 — 2000 г.
Honda Civic — 93c56 — мод. 2001
Honda Civic Ferio — 93c56 — 2001 год
Honda Civic — 93c56 — мод. 2002
Honda Civic – 93c66 – 2003 year
Honda Civic – NEC uPD780973 – 2002 year
Honda Civic – 68HC912B32 – 2003-2004 years
Honda Civic – 93c56 – 2005 year
Honda Civic – 93c76 – 2006-2007 years
Honda Civic – 93c66 — 2007 год
Honda Civic (американский) — 93c56 — 2006 г.в.
Honda Civic (американский) — 93c66 — 2006-2008 гг. 2006 г.в.
Honda CRV – 93c76 – 2007-2010 гг. FR-V — 93c66 — 2005 год
Honda HRV — 93c46 — 2000-2003 годы
Honda HRV – 68HC912BE32 – 2001 year
Honda Inspire – 93c56 – 1999 year
Honda Integra – 93c46 – 2003 year
Honda Insight – 93c86 – 2008 year
Honda Jazz – 93c56
Honda Jazz – 93c66 – 2005 year
Honda Legend – 93c46 — 2001 год
Honda Legend — 93c56
Honda Legend — 93c66 — 2009 год
Honda Life — 93�66
Honda Logo — 93c46
Honda Mobilio — 93c56 — 2004-2005 годы
Honda Odyssey — 93c56 Honda Odyssey — 964s46 — 4994s46 год 93c56 – 1999-2002 годы
Honda Odyssey-93C46-2005 год
Honda Odyssey-93C66
Honda Pilot-93C46
Honda Pilot-93C56-2002-2003 годы
Honda Pilot-93C66-2005-2006 годы
HODA-HODA-93C66-2005-2006 годы
HODA-93c66-2005-2006 годы
HODA-93c66-2005-2006 годы
-936-93c66-2005-2006 годы. 1995 год
1995 год
Honda Ridgeline - 9S12H228 - 2005 год
Honda Ridgeline - 9S12H356 - 2007 год
Honda S2000 - 93C56
Honda S2000 - 93C66 - 2004 год
Honda Saber - 93C56 - 93C66 - 2004 год
Honda Saber - 93c56 - 93c66 - 2004 год
Honda Saber - 93c56 - 93c66 - 2004 год. 1997 год
Honda Spike — 93c56 — 2005-2008 годы
Honda Stepwgn (StepWagon) — 93c56 — 2002 год
Honda Stream — 93c56 — 2001-2003 годы
Honda Torneo — 93c46 — 1997 год
Honda 4c3 9 Torneo 93C56
Hummer
Hummer H3-AT2020NB-2004 год
Hummer H3 (часы)-AT2020NB
Hummer H4-(Dash+BCM)-2005-2009 годы
HUMDAI
HYUNDAI-93C566-93C566-93C566-93C566-93C566-93C566-
---
-9466-2005-2009 годы
. — NEC — 2004 год
Hyundai Atos — 93c46
Hyundai Azera – 93s66 – 2006 year
Hyundai Coupe – 93c46
Hyundai Elantra – 93c46 – 2000-2009 years
Hyundai Elantra – NEC – 2002-2006 years
Hyundai Genesis – 93c66
Hyundai Getz – 93c46 – 2004-2007 years
Hyundai Getz — 24c16
Hyundai GL — 93c46 — 2005 г.
Hyundai Grand Starex — 93c46 — 2008 г.
Hyundai Grand Starex — 93c66 — 2009-2011 гг. - 93с56
Hyundai h300 – 93c56 – 2005 year
Hyundai i10 – 24c08 – 2009 year
Hyundai i10 – 9S12HY64V0L – 2010 year
Hyundai i30 – 93c56
Hyundai ix35 – 93c66 – 2010-2011 years
Hyundai Lavita – 93c46 – 2001 year
Hyundai Matrix - 93c46 - 2004-2005 гг.
Hyundai NF - 93c56
Hyundai Porter - 93c56 - 2008 г.в.
Hyundai Santa Fe - 93c46 - 2003-2004 г.в.
Hyundai Santa Fe - 93c46 - 2007 г.в. Хендай Соната – 93c46
Hyundai Sonata — 93c56 — с 2005 г.
Hyundai Sonata — NEC — 2001-2006 гг.
Hyundai Sonata — 93c66 — 2010-2011 гг. Hyundai Trajet – 93c56 – 2004 г.в.
Hyundai Terracan – NEC – 2001-2003 гг.
Hyundai Terracan – 93c56 – 2004 г.в. 93c46 – 2004-2005 years
Hyundai Tucson – 93c66 – 2010 year
Hyundai Verna – 93c56
Hyundai XG25 – 93c46
Hyundai XG30 – 93�46
Hyundai XG 300 – 93c46
Hyundai XG 350 – 93c56
Infiniti
Infiniti – 93c46 -2000 год
Infiniti FX35-93C66-2003-2005 годы
Infiniti FX45-93C66-2003-2005 лет
Infiniti G35-93C66-2002-2003 годы
INFINITI G37-93C66
466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466. Год
Год
Инфинити Q45 – 93c56
Infiniti QX4 – 93c56 – 2000-2003 years
Infiniti QX56 – MC9S12h356VFV – 2004-2007 years
Infiniti QX65 – MC9S12h356VFV – 2004 year
Isuzu
Isuzu Aska – 93c46
Isuzu Aska – 93c56
Isuzu Axiom – 93c46 – 2002 year
Isuzu Bighorn – 93c46
Isuzu Crosswind – 93c56
Isuzu Elf – 93c56 – 1999 year
Isuzu Forward Type 1 – 93c56
Isuzu Forward Type 2 – 93c56
Isuzu D-Max – 93c56 – 2004-2006 years
Isuzu D-Max – 93c66 — 2007 год
ISUZU KB240-93C56-2005 год
ISUZU LORRY-93C56
ISUZU MU-93C46
ISUZU NQR-93C46
ISUZU PIKUP-93C56-2003 9466 ISUZUSU PIKUP-93C56-2003
66-93C56-93C46.
Isuzu Trooper - 93C46 - 2003 год
Wizard Isuzu - 93C46
IVECO
IVECO DAYLAP — 2010 год
Iveco Eurocargo Тахограф — 24c04 — 2007 год
IVECO 3,8 дизеля-
-2006 год
Jaguar
Jaguar XRI6
Jaguar S-Type-68HC11KA4
Jaguar S-Type-68HC711K8-2000 год
-h-type-68HC711K8-2000 год
-h-type-68hc711k8-2000 год
-ype-68hc711ks8-2000 год
-ype-68hc711ks8-2000 год
-ype-68hc711ks8-2000 год
-го. 68HC912D60
68HC912D60
Jaguar X-Type type 2 – 68HC912D60 – 2003 year
Jaguar X-Type – 68HC912DC128
Jaguar X-Type – 9s12DG128
Jaguar XF – 24c64
Jaguar XJ – 9s12DG128
Jaguar XJ8 – 68HC11KA4
Jeep
Jeep Commander – 93c76 - 2006 год
Jeep Cheroke Limited-93C56-1998-1999 годы
Jeep Cherokee-68HC908AS60A-2001-2004 года
Jeep Cherokee Ladado-93C76-2006 год
Jeep Grand Cherokee-68HC11E9-19
1198 годы
6
6
6
6
696
6.9646
6
6
69696
6.9646
6
6
6
6
6
69696
6. Grand Cherokee — 2000 г.
Jeep Grand Cherokee — 93c56
Jeep Grand Cherokee — 68HC705V12 — 2000 г.08AS60
Jeep Liberty Type 2 – 68HC908AS60
Jeep Sport – 68HC908AS60A – from 2006 year
Jeep TJ – 93c56 – 1997-2000 years
Jeep TJ – 68HC11E9 – 2001 year
Jeep Wrangler – 93c56 – 1997-2000 years
Jeep Wrangler – 68HC11E9 – 2001 year
Jeep Wrangler – 68HC912B32
Jeep YJ – 93c56 – 1997-2000 years
KAMAZ
Kamaz VDO – 93c46
KIA
KIA Bongo – 93c56 – 2008-2010 years
KIA Borrego – 93c66
KIA Carens – 93c46 – 2002-2006 годы
Kia Carnival-93C46-2003-2008 годы
Kia C'EED-93C56-2007 год
Kia C'EED-24C16-2009-2010 лет
Kia Cerato-93C46
Kia Clarus-93C46
KiATIS –93C46IS-93C46. -93C56-2008-2010 годы
-93C56-2008-2010 годы
Kia Magentis-NEC
Kia Mohave-93C66
Kia Opirus-93C46
Kia Optima-NEC-2001 год
Kia Optima-24C16-2010-2011 год
Kia Picanto-93c46-2006-966-966-966-2006-966-966-2006-966-966-2006 год. Picanto — 93c56 — 2008-2009 гг.
KIA Picanto — 93c66 — 2010-2011 гг.
KIA Pride – 93c46
KIA Pride – 93c56
KIA Pride – NEC – 2006-2007 years
KIA Rio – 93c46 – 2004-2007 years
KIA Rio – 93c56 – 2006 year
KIA Rondo – 93c46
KIA Rondo – 93c56
KIA Шума-93C46-1997-2004 годы
Kia Sedona-93C46
Kia Sepia-93C46
Kia Sorento-93C46-2002-2008 лет
Kia Sorento-93C56-2008-2009 годы
Kia Sorento-24C16-20096-4066-4066-40646-406-406-406-2966-4046-406-4046-4046-4046-4046-4046-40646-4064 года-2946-40646-4064 года-4046-4046-4046-4046-4046-4064 года-4046-4046-4046-4046-4064 года. Soul — 93c56
KIA Spectra — 93c46 — 2004-2007 гг.
KIA Sportage — 93c46 – 2004 year
KIA Sportage – 93c56 – 2005-2009 years
Lancia
Lancia Dedra Borg – 93c46
Lancia Lybra Jaeger – 68HC11KG4 – 2000 year
Lancia Lybra Veglia Borletti – 68HC11KG4 – 2001 year
Lancia Lybra Veglia Borletti – 68HC11KG4 – 2002 год
Lancia Musa –
– 2005 год
Lancia Phedra – (Dash2+Dash3+BSI) – 2003-2004 годы
Lancia Phedra – (Dash2+Dash3+BSI) – 2006 год
Lancia Thesis – 93s56
Lancia Thesis6 – 93S56
Лянча К Велья Борлетти — 68HC11KG4 — 1997-1999 гг. 2001 г.
2001 г.
Land Rover
Land Rover Discovery — 93c56 — 1999-2000 гг.
Land Rover Discovery — (Dash+BCU) — 1999-2000 гг.
Land Rover Discovery — (Dash+BCU) — 2003 г. BCU Тип 1) – 68HC11P2
Land Rover Discovery (BCU Тип 2) – 68HC11P2
Land Rover Discovery 2 (BCU) — 68HC11PH8
Land Rover Discovery 3 — 35080 — 2007-2008 г.в.
Land Rover Discovery 3 (CJB) — 9s12DG256 — 2007-2008 г.в. Rover Defender — 24c02 — 2000 г.в.
Land Rover FreeLander — 93c46 — 1998-2000 г.в. CJB) — 9с12ДГ256 — 2006 г.в.4646 Land Rover Range Rover — 28c16 — 2000 г.в.
Land Rover Range Rover — 35080 — 2002-2004 гг.
Land Rover Range Rover — 93c86
Land Rover Range Rover — 93c86 — 2004-2007 гг. 68HC11EA9
Land Rover Range Rover (LCM) — 9s12D64
Land Rover Range Rover Sport — 35080
Land Rover Range Rover Sport (CJB) — 9s12DG256
Land Rover Range Rover Supercharged — 93c86
Land Rover Range Rover Supercharged (сервис) — 93c86 93c86 Ленд Ровер Рендж Ровер Вог – 35080
Land Rover Range Rover Vogue (EWS3) – 68HC11EA9
LDV
LDV Convoy – 93c46 – 2002 year
LDV 400 – 93c46 – 2004 year
LDV Maxus – 93c46
Lexus
Lexus ES300 – NDM457C – 1992-1998 years
Lexus ES300-93C46-2002 год
LEXUS ES330-93C46
LEXUS ES350-93C56
LEXUS GS300-NDM457C-1992-1998 годы
LEXUS GS300-93C46-1998-2006 лет
LEXUS GS300-93C46-1998-2006 лет
LEXUS GS300-93C46-1998-2006 лет
LEXUS GS300-93C46-1998-2006 лет
LEXUS GS300-93C46-1998-2006 года
. Лексус GS430 — 93c46 — 2007 год
Лексус GS430 — 93c46 — 2007 год
Lexus GS450 – 93c46
Lexus GX470 – 93c66 – 2003-2008 years
Lexus IS200 – 93c46 – 2000 year
Lexus IS200 – 93c56 – 2004-2005 years
Lexus IS250 – 93c56 – 2007 year
Lexus IS300 – 93c46
Lexus IS350 – 93C56
LEXUS IS F-93C56
LEXUS LS400-NDM457C-1992-1998 годы
LEXUS LS400-
-1992-1998 годы
LEXUS LS430-93C46-2001-2006 Годы
LEXUS LS430-93C46-2001-2006 Годы
6-93c46-2001-2006 годы
6-93c46-2001-2006 лет
-LS430-93C46-2001-2006 лет
-LS430-93C46-2001-2006 лет
-LS430-93C46-2001-2006 год — 2008 год
Lexus LX400 — 93c56 — 2000 год
LEXUS LX430-93C46-2006 год
LEXUS LX470-93C46-1998-1999 годы
LEXUS LX470-93C66-2003-2007 годы
LEXUS LX570-93C86-2008 год
-LEXUS LX570-93C86-2008 год
-Lexus LX570-93C86-2008 год
-930-93c86-2008 год
-93.66-93C86-2008 год
-93c46-2008 год
-93c86-2008 год
-93c46-2008 год
-93c86-2008 год
-93c86-2008 год. 2001-2005 лет
2001-2005 лет
Lexus RX330-93C46-2002-2003 годы
Lexus RX350-93C46-2005 год
Lexus RX350-93C66-2009-2010 лет
LEXUS RX400H-93C46-2005-
46646 LEXUS RX400H-93C46-2005-
464646.11999999999999999999999999999999999999 годы.
Лексус SC400 – NDM457C
Лексус SC430 – 93c46 – 2002-2005 years
Lexus SC430 – 93c56 – 2007 year
Ligier
Ligier X-Too – 93c46
Lincoln
Lincoln LS – 68HC711K4
Lincoln MKS – 93c66
Lincoln MKX – 93c66
Lincoln Navigator – 68HC11KA4
Lincoln Navigator -93C46-2005 год
Lincoln Navigator-68HC912DG128-2003 год
Lincoln Navigator-9S12H228-2004-2005 годы
CAR LINCOLN TOWN-68HC11-1998 год
LICKOLN CAR. - 2003 год
Lincoln Town Car Type2 – 68HC711E20 – 2003 year
Lincoln Town Car – 9s12h228
Lincoln Zephyr – 93c66 – 2007 year
MAN
MAN All Tachograph – 24c04
MAN TGA – 93LC86 – from 2006 year
Maserati
Maserati Quartoporte –
-2005-2006 годы
Mazda
Mazda ECU
Mazda ECU EDC16-
Mazda 121-68HC11E20-1998-1999 годы
Mazda 2-93C56-1998-1999 годы
2-947-годы 9464 года. 3 – 93c56 – 2005-2007 гг.
3 – 93c56 – 2005-2007 гг.
Mazda 5 – 93c56 – 2007 г.
Mazda 6 – 93c56 – 2003-2006 гг.
Mazda 6 – 93c66 – 2007-2008 гг. 626 – 93c56 – 2001-2002 гг.
Mazda 323 – 93c56 – 2000-2003 гг.
Mazda 626 – 93c56 – 2000-2003 гг.
Mazda 326/636 – 93c56 – 2002 г.в. 93c56
Mazda B2200 — 68HC05L28 — 2002-2005 годы
Mazda B2500 — 68HC05L28 — 2002-2005 годы
Mazda B2900 — 68HC05L28 — 2002-2005 гг.
Mazda Bongo — 93c46 — 2004 г.
Mazda BT-50 — 93c56 — 2006-2007 гг. CX-7 – 93c56 – 2007 г.в.
Mazda CX-7 – 93c66 – 2005-2008 гг.
Mazda Demio – 93c56
Mazda Demio – 93c56 – 2002-2003 г.в.
Mazda Familia Type1 — 93c56 — 2000 год
Mazda Familia Type2 — 93C56-2000 год
Mazda Lantis-93C46
Mazda M3-93C56-2005 год
Mazda M6-93C56-2003-2007 лет
Mazda Millenia-93C46
MAZDA MPV-93C46-1994-1946-93-93C46
MAZDA-93C46-1994-1946-93-93C46
MAZDA-93C46-93C46
MAZDA-93C46-1994-1946-93C46
MSDA-93C46-1994-1946-93C46
MAZDA-93C46-93C46
. -2000 г.в.
-2000 г.в.
Mazda Premacy – 93c56
Mazda Premacy – 93c56 – 1998-1999 гг. Дань — 68HC11KA4 — 2000-2003 годы
Mazda Tribute – MC9S12h228 – 2005 г.в.
Mazda Titan – 93c56 – 2001 г.в.
Mazda Verisa – 93c56 – 2004 г.в. 2000
Mercedes W220 Service — 93c66
Mercedes W220 Service — 24c04 — мод. 2000
Mercedes W203 Service – 93c86
Mercedes A Class W168 – 68HC711KG4 – 1998 год
Mercedes A Class W168 – 68HC912D60 – 2000-2004 годы4646 Mercedes A Class W169 — (Dash+EZS) — 2005-2007 гг.
Mercedes C Class VDO — 93c56 — до 09.1995 г.
Mercedes C Class — 93c56 — с 09.1995 г.
Mercedes C Class – 93c86 – 2000 г.в.
Mercedes C Class – 24c04 – mod 2000 г.в.
Mercedes C Class W203 – (Dash+EZS) – 2000-2002 гг. Mercedes C Class W203 — (Dash+EZS) — 2003-2004 годы
Mercedes C Class W204 Dash — 24c128 — 2007 год
Mercedes SLK/CLK – 93c56
Mercedes CLK – 93c66 – 1999 г.в.
Mercedes CLK Class W208 – (Dash+EZS) – 2002 г. в. – (Dash+EZS)
в. – (Dash+EZS)
Mercedes E Class W210 – 93c56
Mercedes E Class – 93c66
Mercedes E Class W212 – 24c17
Mercedes E Class W210 – 93c86 – 1999-2001 годы
Mercedes E Class W210 – (Dash+EZS) – 2002 г.
Mercedes E Class W211 — (Dash+EZS) — 2002-2005 годы
Mercedes E Class W211 — (Dash + EZS) — 2003 г.
Mercedes E Class W219 — (Dash+EZS) — 2004-2005 гг.
Mercedes G-Class W463 — (Dash+EZS) — 2004 г. W163 — 93c66
Mercedes ML Class W164 — (Dash+EZS) — 2006 год 2000 год
Mercedes S Class W220 — (Dash+EZS) — 2003 год
Mercedes S Class W221 — 24c08 — 2007 год
Mercedes Actros – 93lc76 – 2001 г.в.
Mercedes Actros Тахограф – 24c04
Mercedes Atego Тахограф – 93c66
Mercedes Atego Тахограф – 93c86
Mercedes Smart – 93c66
Mercedes Sprinter – 93s46 – 1995 г.в.
Mercedes Sprinter Kienzle — 24c02
Mercedes Sprinter — 24c04 — 2000 г.в. с FS
Mercedes Sprinter VDO — 93c66 — 2000-2001 гг.
Mercedes Sprinter/Vito — 24c02 — с тахометром 1996 г. в.06 Тип 1 – 25640 – 2007-2008 гг.
в.06 Тип 1 – 25640 – 2007-2008 гг.
Mercedes Sprinter W906 Тип 2 – 25640 – 2007-2008 гг.
Mercedes Sprinter W906 Тип 3 – 25640 – 2007-2008 гг. – 68HC912D60
Мерседес Вито Тип 1 – 93с46 – 1995-1998 годы
Мерседес Вито Тип 2 – 93с46 – 1995-1998 годы
Мерседес Вито – 24c02
Мерседес Вито – 24c04
Мерседес Вито – 68HC9194AZ922 Мерседес ST
Mercedes Vito — (Dash+EZS) — 2004 год
Mercury
Mercury Cougar – 68HC711K4
Mercury Grand Marquiz – 9s12h228VFV – 2006 year
Mercury Mariner – 9s12h228
Mercury Milan – 93c66 – 2007 year
Mercury Montego – 9S12h228 – 2006 year
Mercury Mountaineer – 9s12h228
Mini
Mini Cooper Dash — 68HC912DG128
Mini Cooper Dash — 35080
Mini Cooper BCU — 68HC912DG128
Mini Cooper BCU — 93c76 — 2004-2005 годы
Mini Cooper CAS3 — 9s12DP512
Mitsubishi Airtrek
3c56 — 2002 год
Mitsubishi ASX — 93c86 — 2010-2011 годы
Mitsubishi Canter — 93c46 — 2006-2007 год
Mitsubishi Colt — 93c46 — 2001 год
Mitsubishi Colt — 93c56 — 2005 год
Mitsubishi Delica — 93c46 — 1995-1999 годы
Mitsubishi Diamante — 93c46 — 1996 год
Mitsubishi Dingo — 93c56 Mitsubishi Dion —
3c56
Mitsubishi Eclipse – 93c46 – 2000 year
Mitsubishi Eclipse – 93c56
Mitsubishi eK Wagon – 93c46
Mitsubishi eK Sport – 93c56
Mitsubishi Endeavor – 93c66 – 2004-2007 years
Mitsubishi Endeavor – 93c66
Mitsubishi FTO – 93c46
Mitsubishi Fuso – 93c46
Mitsubishi Fuso — 93c56 — 2002 г. в.
в.
Mitsubishi Galant — 93c46 — 1995-2000 г.в.
Mitsubishi Galant — 93c46 — 2001-2002 г.в.3C46-2005-2006 гг.
Mitsubishi Lancer — 68HC705B6 — с 2002 года
Mitsubishi Lancer — 93c56 — 2002-2006 гг.
Mitsubishi Lancer — 93c86 — 2007-2009 годы Миника – 93c46
Mitsubishi Mirage — 93c46 — 1996-1999 годы
Mitsubishi Mirage — 93c56 — 1997-2000 годы
Mitsubishi Montero — 93c46 — 1997-2003 годы
Mitsubishi Montero — 93c56 — Yazaki
Mitsubishi Outero6 — 93c66 год 93cs56
Mitsubishi Outlander — 2 x 93cs56 — 2003-2006 гг.
Mitsubishi Outlander — 93c86 — 2006-2008 гг.
Mitsubishi Outlander — 93c76 — 2007 г.3c56 – 2001-2005 гг.
Mitsubishi Pajero – 93c66 – 2006-2007 г.в. Space Star – 93c46 – 1999-2000 г.в.
Mitsubishi Space Wagon – 93c46 – 1997-2000 г.в.0419
Nissan
Nissan ALL vs Miles – 93c56
Nissan ALL vs Miles – 93c66
Nissan 350Z – 93c66 – 2004 year
Nissan AD – 93c56 – 2000 year
Nissan AD – 93c66 – 2003-2005 years
Nissan Almera – 93c46 – 1998-1999 гг.
Nissan Almera — 93c56 — 1998-2000 гг. - 93c66 - 2004-2010 гг.
Nissan Almera Tino — 93c66 — 2003 г.в.
Nissan Altima — 93c56 — 2000 г.в.
Nissan Altima — 93c66 — 2004-2007 гг. MC9S12h356
Nissan Atlas – 93c56 – 2000-2003 years
Nissan Atleon – 68HC908AZ60
Nissan Avenir – 93c56 – 1999-2001 years
Nissan Avenir – 93c66 – 2003-2005 years
Nissan Bassara – 93c56
Nissan Bluebird – 93c46 – 1997-1998 лет
Nissan Bluebird — 93c56 — 1999-2002 гг.
Nissan Bluebird — 93c66 — с 2003 г.
Nissan Caravan — 93c46 — 2000-2002 гг. Cefiro – 93c46 – 1997-2000 гг.
Nissan Cefiro – 93c56 – с 2000 г.в.
Nissan Cefiro Brougham – 93c46 – 2000 г.в.
Nissan Cube-93C66
Nissan Datsun-93C46-1997 год
Nissan Datsun-93C56-1999 год
Nissan Double Cab-93C56-2001 год
-93cless
666666666666-93-й 9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-9466-93-го года-93cles. -2003 год
Nissan Expert-93C56-1999-2002 годы
Nissan Expert-93C66
Nissan Extera-9S12H356
Nissan Fairlady-93C56
Nissan Fairlady-93c66
nissan –9366-9366-9366-9366-9366-9366-93-й. 4646 Nissan Frontier – 24c08 – 2007-2008 years
4646 Nissan Frontier – 24c08 – 2007-2008 years
Nissan Frontier – 9s12h356
Nissan Fuga – 93c66 – 2005 year
Nissan Juke – 93c86 – 2010 year
Nissan Gloria – 93c46 – 1998 year
Nissan Gloria – 93c56
Nissan Homy Elgrand – 93c46
Nissan Homy Elgrand — 93c66
Nissan Laurel — 93c46 — 1996-2001 гг.
Nissan Liberty — 93c46 — 1999 г.
Nissan March — 93c56 — 2000-2002 гг. - 2000 год
Nissan Maxima – 93c46 – 1997-1999 гг.
Nissan Maxima – 93c56 – 2000-2005 гг.
Nissan Maxima – 93c66 – 2003 г.в.
Nissan Micra – 93c46 – до 03.2002 г. — 93c66 — 2002-2003 годы
Nissan Moco — 93c46
Nissan Moco — 93c66 — 2006 год
Nissan Montera — 93c46
Nissan Murano — 93c66 — 2002-2009 годы
Nissan Murano (мили) Тип 1 — 943c46 Nissan Murano
) Тип 2 — 93c66
Nissan Navara — 93C46
Nissan Navara-93C56-1999 год
Nissan Navara-9S12H228-2006-2008 годы
Nissan Navara-9S12H356
Nissan Note-93C56-2006 год
Nissan Note-93C66-93C56-2006 год
Nissan Note-93c66-93c56-2006 год
Nissan-93-2008-93c56-2006 год
Nissan-93-2008-93c56-2006 год. Nissan Pathfinder – 93c46 – 1998 г.в.
Nissan Pathfinder – 93c46 – 1998 г.в.
Nissan Pathfinder – 93c66 – 2001-2003 гг.
Nissan Pathfinder – MC9S12h356 – 2004 г.в.3c66 – 2003-2007 years
Nissan Pickup – 93c46
Nissan Pickup – 93c56 – 1999-2001 years
Nissan Pickup –
Nissan Platina – uPD780973 – 2004-2005 years
Nissan Prairie – 93c46
Nissan Primastar – 93c66
Nissan Presia / Presea – 93c46 – 1997 г.в.
Nissan Pressage – 93c56 – 1997-2001 гг.
Nissan Primera – 93c46 – 1996-1999 гг. Тип2 – 93C66-2001-2007 лет
Nissan Pulsar-93C46-1997-2000 лет
Nissan Qashqai-93C66-2007 год
Nissan Qashqai-9S12XHZ256-2010 год
Nissan Quest Quest – 9s12h356 – 2006 year
Nissan Quest – 9s12h356 – 2007 year
Nissan Regulus – 93c46
Nissan Rnessa – 93c56 – 1997-2000 years
Nissan Rogue – 93c66 – 2008 year
Nissan Roniz – 93c56
Nissan Safari – 93c56
Nissan Sentra – 93c56 – 2000-2002 гг.
Nissan Sentra – 93c66 – 2005-2007 гг.
Nissan Serena – 93c46 – 1997-1999 гг.
Nissan Serena – 93c56 – 2000-2002 гг. Nissan Skyline – 93c56 – 1998 г.в.
Nissan Skyline – 93c66 – 2003-2011 гг.
Nissan Stagea – 93c46 – 1996 г.в.
Nissan Sunny — 93c66 — 2004-2005 гг.
Nissan Sunny – 93c66 – 2007 г.в.
Nissan Teana – 93c66 – 2003-2009 гг.
Nissan Terrano Regulus – 93c46 – 1997 г.в.
Nissan Terrano – 93c66 – 2001 г.в.
Nissan Tino — 93c56 — 1998-2001 годы
Nissan Titan — 9S12h356
Nissan Titan — 9S12DG256 — 2005-2006 годы
Nissan Urvan — 93c46 — 2003 год
Nissan Vanette — 93c46 — 593 Wing64 — 1999-2004 годы 1999-2001 годы
Nissan Wingroad – 93c66 – 2001-2002 years
Nissan Xterra – 93c46 – 1998 year
Nissan Xterra – 93c56 – 1999-2000 year
Nissan Xtrail – 93c56 – 2003-2004 years
Nissan Xtrail – 93c66 – 2002-2008 years
Oldsmobile
Oldsmobile Alero-
Oldsmobile Aurora-
Oldsmobile Delta 88-
Opel
Opel Agila-NEC D780828A-2001-2002 годы
Opel Agila-NEC D780828A-2001-2002 годы
Opel Agila-NEC D780828A-2001-2002 годы
Opel Agila-NEC D780828A-2001-2002 годы
. -2009 г.в.
-2009 г.в.
Опель Астра ВДО – 93c46 – до 2000 г.в.
Opel Astra VDO – 93c56 – до 2003 г.в.
Opel Astra H VDO – M35080 – 2003 г.в.
Opel Corsa – NEC uPD780828 – 2001-2002 гг.
Opel Combo – NEC uPD780828 – с 2001 г.в. NEC D780826 — 2002-2008 гг.
Опель Монтери — 93C46-1999 год
Opel Movano Tachograph-93C66-2004 год
Opel Omega-93C46-1999 год
Opel Senator-93C46
Opel Signum-93C66-2003 год
Opel VDECTRA B-VDO-93C66-1966-1966 года. -93C66-2002-2006 годы
Opel Vectra-24C04-2001-2004 годы
Opel Vivaro-M
-2000-2002 годы
Opel Vivaro L-93C66-2005 год
Opel Vivaro L-93C66-2006 год
46666666666666 год. — 1999-2001 гг.
Опель Зафира — 24c02 — 2000 г.в.
Opel Zafira - M35080 - 2007 год
Peugeot
Peugeot 106 - NEC
Peugeot 106 - 93C56 - 2005 год
Peugeot 107 - 93C56 - 2005 год
Peugeot 1007 - (Dash+BSI) –2946 - 2006 год. — 1998 г.
Peugeot 206 — (Dash+BSI) — 2002-2006 гг.
Peugeot 207 Dash Type 1 — 93c66 — 2007-2008 гг.
Peugeot 207 BSI Тип 2 –
Peugeot 306 VDO Тип 1 – 93C56
PEUGEOT 306 VDO Тип 2 - 93C56
PEUGEOT 306 VDO Тип 3 - 93C56
PEUGEOT 306 SAGEM 1 - 93C56
PEUGEOT 306 SAGEM тип 2 - 93C56
PEUGET 307 - (DANGET+BSI) - 68HC96. – (Dash+BSI) – NEC – 2002-2003 годы
Peugeot 307 – (Dash+BSI) – NEC – 2003-2004 годы
Peugeot 307 – (Dash+BSI) – 2005 год
Peugeot 307 Dash –
– 2006 год
Peugeot 307 Dash —
— 2006-2007 гг.
Peugeot 307 BSI Type 1 —
— 2006-2007 гг.
Peugeot 307 BSI Type 2 —
— 2006-2007 гг.
Peugeot 307 BSI Type 3 —
— 2006-2007 гг.
Peugeot 307 BSI Type 4 —
— 2006-2007 гг. 2007 Годы
Peugeot 307 BSI тип 6-
-2006-2007 годы
Peugeot 308 Dash-
Peugeot 308 BSI 1-
Peugeot 308 BSI тип 2-
Peugeot 308 BSI Type 3–
9466 4 4464646466 4 4464666 4 44646466 4 446464666 4 4466 4 44666 4 44666 4 44666 4 4466666666 4 44666 4 4466666666 4. 9566. 93c56 — с 2003 года
9566. 93c56 — с 2003 года
Peugeot 406 Sagem — 93c46 — 1996-1997 years
Peugeot 406 VDO – 93c66 – 1999-2002 years
Peugeot 406 Jaeger – 68HC05X16 – 1997 year
Peugeot 406 TDI – 93c66 – 1999 year
Peugeot 406 Dash – 93c46
Peugeot 406 Dash – 93c66 – 2000 year
Peugeot 406 BSI Тип 1 Siemens – 93c66 – 1999-2001 гг.
Peugeot 406 BSI Тип 2 Siemens – 93c66 – 1999-2001 гг.
Peugeot 406 BSI Valeo – M
– 2000-2001 гг. 407 — (Dash+BSI) — 2005 год
Peugeot 407 BSI Valeo —
-2004 год
Peugeot 407 BSI Valeo-
-2005 год
Peugeot 407 BSI Valeo-
-2006 год
Peugeot 407 BSI Magnetti Marelli-
-2007 год
Peugeot 407 Dash-93c66-
-2007 год
Peugeot. -
- 2006 год
Peugeot 407 BSI Тип 1 -
- 2007 год
Peugeot 407 BSI Тип 2 -
- 2007 год
Peugeot 407 BSI тип 1 -
- 2008 год
Peugeot 407 BSI Тип 2 -
- Год
года 407 BSI тип 2 -
- Год
года. Peugeot 607 VDO — 93c66 — 2000-2001 годы
Peugeot 607 BSI – 93c66 – 2000-2001 years
Peugeot 607 – (Dash+BSI) – 2004 year
Peugeot 607 Dash – 93c66 – 2004-2006 years
Peugeot 607 BSI –
– 2004 year
Peugeot 607 BSI –
– 2005-2006 гг.
Peugeot 607 BSI —
— 2007 г.
Peugeot 806 Jaeger — 68HC05h22 — 2000 г. 2006 г.в.
Peugeot Bipper –
– 2008 г.в.
Peugeot Boxer – (Dash+BSI) – 2000-2003 гг.
Peugeot Boxer 2-
-2002-2003 годы
Peugeot Boxer-
-2006 год
Peugeot Expert Jaeger-68HC908AZ32-2001 год
Peugeot Expert (DASH)-
-2007 год
Peugeot Pars-93C56
46466464646464664646464646464646464646464646464646464646464646464646464646. – 2001 г.в.
Peugeot Partner – (Dash+BSI) – 2000-2003 гг.
Peugeot Partner – (Dash+BSI) – 2001-2004 гг.
Понтиак
Понтиак Ацтек –
Pontiac Bonneville-
-2003 год
Pontiac G5 BCU-25080-2007-2008 годы
Pontiac G6 BCU-25040-2004-2006 годы
Pontiac G6 BCU-25080-2006-2007 годы
Pontiac G6-9506-9506-9506-9506-9506-9506-9506-9506-9506. -2001 года
Гран-при Pontiac-
-2004 год
Pontiac HHR BCU-25080
Pontiac Montana-68HC912B32
Pontiac Sunfire-93C66-2000-2003 год
Pontiac Torrent Bcu-68S66-2000-2003 годы
Pontiac Torrent Bcu –68S66.
Понтиак Вайб – 93C46-2003 год
Волна Pontiac-68HC05H22
Pontiac Wave-93C56
Porsche
Porsche 928 All-93C46-1991-1995 лет
Porsche 996-93C56-1991-1995 лет
996-946-9466-9466-9466 лет
-946-946-9466-9466-9466-9466-9466-9466-9466-9466-9466-9464 года
-946-946 лет
-946-946 лет
-946-946 лет
-946-946 лет
. 93C86-2003 год
Porsche 991-93C86
Porsche 997-93C86
Porsche Boxster-93C56-1996-2001 года
Porsche Boxster-93C86-от 2001
Porsche Boxster-93c86-93c86-2001
Porsche Boxster-93c86-93c86-2001
Porsche-93c86-93c86-2001
Porsche-93c86-93c86-2001
Porsche-93c86-93c86-2001
. 24c08 – 2001-2005 годы
Porsche Panamera –
– 2010 year
Renault
Renault Clio – 93c46 – 1996-2000 years
Renault Clio – 68HC908AZ60 – 1999-2001 years
Renault Clio Jaeger Type 1 – 68HC908AZ32 – 2000 year
Renault Clio Jaeger Type 2 – 68HC908AZ32 — 2000 год
Renault Clio Sagem — ST
— 2002 год
Renault Clio — NEC uPD780973 — 1999-2002 годы
Renault Clio — 93c56 — 2004-2005 годы
Renault Clio — 93c66 — 2004 год 945-200 Renault Clio4 — 2004-2004 год 945-200 Clio4 лет
Renault Espace Type 1 – TMS370 – 1997-1999 годы
Renault Espace Type 2 – TMS370 – 1997-1999 годы
Renault Espace – (Dash+BSI) – 1998-2001 годы
Renault Espace – 93c56 – 2002 год
Renault Espace – 93c56 – 2003-2004 years
Renault Espace – 93c66 – 2006 year
Renault Kangoo – 93c46 – 1998-2000 years
Renault Kangoo –
– 1999-2003 years
Renault Kangoo Jaeger – 68HC908AZ32 – 2002 year
Renault Kangoo – 93c66 – 2006 Год
Рено Кангу – 93c76 – 2008 г. в.
в.
Renault Koleos – 24c16 – 2008-2009 гг. Laguna – 68HC12DG128 – 2000 year
Renault Laguna – 68HC908AZ60 – 2001-2003 year
Renault Laguna – 68HC12DG128A – 2005 year
Renault Laguna – 9s12h356
Renault Laguna – 24c16 – 2008-2010 years
Renault Logan – 93c56 – 2005 year
Renault Logan – 25020 – 2008-2009 гг.
Renault Master — 93c66 — 2002 год
Renault Mascott тахограф — 93c66
Renault Master —
— 2001 год
Renault Master — NEC uPD780973 — 1999-2002 годы
Renault Master — 93c60 — 2003 Renault Master — 903 Master — 6 2004 946 год 946 -2007 г.в.
Renault Master тахограф – 93c66
Renault Maxity – 93c66 – 2010-2011 гг.
Renault Megane Type 1 – 93c46 – 1996-1997 гг.08AZ60 — 1999-2001 гг.
Renault Megane Visteon — 93c56 — 2002-2004 гг.
Renault Megane Visteon Type 1 — 93c56 — 2003 г.
Renault Megane Type 2 — 68HC(7)11Kxx
Renault Megane Jaeger — 68HC08AB32
Renault Megane — NEC uPD780973 — 1999-2002 гг.
Renault Megane Type 1 — 93c56 — 2004 г. Меган — 24c04 — 2005-2007 гг.
Renault Modus – 93c56 – 2004 г.в.
Renault Modus – 93c56 – 2005 г.в.
Renault Modus – 93c56 – 2006 г.в. SAFRANE-93C56
Renault Sandero-25020-2008 год
Renault Scenic-93C46-1998 год
Renault Scenic-93C56-2004 год
Renault Scenic-68HC11KG4
Renault Scenic-68HC908AZ32-2000-2001 DES
RENAULT SCENIC-68HC908AZ32-2000-2001 DEN
.73 — 1999-2003 гг.
Renault Symbol — NEC — 2004-2008 гг.
Renault Trafic — M
— 2000-2004 гг.
Renault Trafic — 93c66 — 2004 г.
Renault Twingo-ST6245-1996-2000 гг. СААБ
СААБ 9-3 – 93c46 – 1995-2000 гг.
SAAB 9-3 – 24c02 – 2003 г.
SAAB 9-3 – 24c04
SAAB 9-3 – 24c08
SAAB 9-5 – 93c46 – 1995-2000 гг. -93C56
SAAB 9-5-24C04-2004 год
SAAB 9-5-93C66-2006-2209 годы
SAAB 9000-93C56
SAAB SPORT SEDAN-24C02-2004 год
9466 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046 9046.
9046.
9046.
9046 9046.
9046 9046.
9046 9046.
Samand – 93s56 – 2006-2007 гг.
Samand Soren – 93c56 – 2007 г.в.
Samsung
Samsung SM3 – 93c56 – 2005-2006 гг.
Samsung SM5 – 93c56 – 2005-2006 гг.
Samsung QM5 – 24�16
Saturn
Saturn – 93c66 – 2000-2003 гг. 25080
Saturn Ion BCM-
-2003 год
Saturn L200 BCM-68HC908AS60-2003 год
Saturn L300 BCM-68HC908AS60
SATURN-93C66-2007-2008 Годы
SATRUNE-93C66-2007-2008 Годы
SATURN-93C66-2007-2008 LISES
SATURN-93C66-2007-2008 год. – 68HC908AS60
Сатурн Вью БКМ – 68HC908AS60 – 2003 year
Saturn Vue BCM – 68HC912
Saturn Vue – 93c86
Scion
Scion xA – 93c56
Scion xA – 93c66 – 2002-2005 years
Scion xB – 93c46 – 2002 year
Scion xB – 93c56 – 2004 year
Scion TC-93C56
SEAT
ECU
EDC15-24C08-2000-2004 года
SEAT ALHAMBRA-68HC11E20-1996 год
SEAT ALHAMBRA-68HCC11E9-1997-1999-годы
SEAT ALHAMBRA-68HCC11E9-1997-1999 годы
.
. – 2002-2003 годы
SEAT ALTEA-24C16-2005 год
SEAT ALTEA-24C32-2005 год
SEAT AROSA-24C02
SEAT CORDOBA VDO-93C46
SEAT CORDOBA VDO-93C66-2000 год
SEAT FODOBA VDO VDO-93C66-2006-2000 год
SEAT SEATOBA VDO VDO-93C66-2006-2000 год
SEAT SEAT VDO VDO-93C66-2006-2000 год
SEAT VDO VDO-93C66-2000-го года
SEAT VDO-93C66-2000-го года
. VDO - 93C86 - 2002 год
SEAT CODOBA VDO - 93C86
SEAT CORDOBA - 9S12H356 - 2008 год
SEAT IBIZA VDO - 93C46 - 1999 год
SEAT IBIZA VDO - 93C66 - 2000 год
SEED IBIZA VDO - 93C66 - 2000 год
SEAT TRW – 24c08 – 2000-2003 годы
SEAT Ibiza – 93c86
SEAT Ibiza – 9s12h356
SEAT Inca – 93c46 – 1997-2001 year
SEAT Inca – 93c66
SEAT Inca – 93c66 – 2000 year
SEAT Leon – 93c66
SEAT Leon Type 1 – 93c86
SEAT Leon Type 2 — 93c86
SEAT Leon Type 3 — 93c86
SEAT Leon Type 1 — 93c86 — 2000 г.
SEAT Leon Type 2 — 93c86 — 2000 г.
SEAT Leon — 93c86 — 2003 г. — 2005 г.в.
SEAT Toledo — 93c66 — 1999 г.в.
SEAT Toledo – 93c86 – 2001 year
SEAT Toledo – 24c16 – 2005 year
Skoda
ECU's
EDC15 – 24c08 – 2000-2004 years
Skoda Fabia VDO – 93c86 – 2001-2002 years
Skoda Fabia VDO – 93c86 – 2003 year
Skoda Felicia-93C66
Skoda Felicia-93C86-2002 год
Skoda Laura-24C32-2006 год
Skoda Oktavia Type 1-93C66-1997-1999 года
Skoda Oktavia Type 2-93C66-19999 года
666. — 2000 г.в.
Шкода Октавия — 93c86 – 2001 year
Skoda Oktavia – 93c86 – 2002-2003 year
Skoda Octavia – 24c16 – 2004-2005 years
Skoda Oktavia – 24c32 – 2003-2006 years
Skoda Oktavia2 – 93c86
Skoda Superb – 93c86 – from 2002 year
Skoda Superb – 93c86 – с 2003 г.в.
Skoda Superb – 93c86 – 2004 г.в.
Smart
Smart – (Dash+BSI) – 2004-2005 гг. BSI) — 68HC05X32 — 2000-2001 годы
Smart For Two (Dash+BSI) — 2006 год
Smart Roadster - (Dash+BSI) - 2006 год
Ssang Young
Ssang Yong Action - 93C56
Ssang Yong Kiron - 93C56
Ssang Yong Musso - 93C56
Ssang yong rexton - 9sxxt6 - 93c56
Ssang yong - 9sxxt6 - 93c56
Ssang yong - 9sxxt6 - 93c56
yong - 93 - 93c56
- 93 - 93c56
- 93 - 93c56
. 2001-2006 years
2001-2006 years
Ssang Yong Rexton RX 290 – 93c46
Ssang Yong Rodius – 93c46
Subaru
Subaru R1 – 93c56 – 2005-2008 years
Subaru R2 – 93c56 – 2003-2007 years
Subaru R2 – 93c66 – 2008 year
Subaru Baja — 93c56 — 2003-2006 годы
Subaru Forester — 93c46 — до 2000 г.в.
Subaru Forester Type 1 — 93c56 — 2001-2007 гг.
Subaru Impreza-93C56-2000-2007 годы
Subaru Impreza-93C76-2008-2009 годы
Subaru Justy-93C66-2008 год
Subaru Legacy-93c56-2000 год
Subar - 93c56 - 2004-2005 гг.
Subaru Legacy Lancaster – 93c56 – 2000 year
Subaru Legacy – 93c66
Subaru Legacy – 93c76 – 2008-2009 years
Subaru Outback – 93c56 – 2001 year
Subaru Outback – 93c56 – 2005-2006 years
Subaru Outback – 93c76 – 2007 year
Subaru Outback – 93�66 – 2008 year
Subaru Tribeca – 93c66 – 2006 year
Suzuki
Suzuki A Star – 93c66 – 2009 year
Suzuki Aerio – 93c46 – 2001-2002 years
Suzuki Aerio – 93c56 – 2003 year
Suzuki Аерио — 93c56 — 2005 год
Suzuki Alto-93C46
Suzuki Alto-93C46-с 2005 года
Suzuki Alto-93C66-2010-2011 лет
Suzuki APV-93C56
Suzuki Eskudo-93C46
Suzuki-9446. Веселье-93C56-2005 год
Веселье-93C56-2005 год
Suzuki Fun-93C56-2007 год
Suzuki Ignis-93C46-2001 год
Suzuki Ignis-93C56-2003-2005 годы
Suzuki Ignis-93C66-2007 год
Suzuki-93c66-2007 год
Suzuki-93c66-2007 год
. 93с46 – 1995-2003 года
Suzuki Grand Vitara-93C46-2002 год
Suzuki Grand Vitara-24C16-2006 год
Suzuki Grand Vitara-24C16
Suzuki Grand Vitara-24C16-2010 год
Suzuki Jimny-68HC0808080808080808080806666666666666666666666. – 93c46 – 1998 year
Suzuki Jimny – 93c56 – 2009 year
Suzuki Kei – 93c46
Suzuki Liana – 93c46
Suzuki Liana – 93c56 – 2004-2007 years
Suzuki Liana – 93c56
Suzuki MR Wagon – 93c46
Suzuki Solio – 93C56
Suzuki Solio-93C66
Suzuki Splash-93C46-2008 год
Suzuki Swift-93C46
Suzuki Swift-93C66-2005 год
-Suzuki Swift-93C66-2006-
46-Suzuki Swift-93C66-2006 год
46-Suzuki-93C66-2006-
46-Suzuki-93C66-2006 год
-Suzuki-93C66-2006-
-Suzuki Swift-93C66-2006-
-Suzuki Swift-93C66-2006 год. – 2008-2009 years
– 2008-2009 years
Suzuki Verona – 68HC05h22 – 2007 year
Suzuki Wagon R Type 1 – 93c46
Suzuki Wagon R Type 2 – 93c46
Suzuki Wagon R – NEC
Suzuki XL7 – 93c66 – 2007 year
Toyota
Toyota 4Runner – 93c56 – 1998-2000 годы
Toyota 4Runner – 93c66
Toyota 4Runner – 93c66 – 2003-2004 years
Toyota Ace – 93c46
Toyota Allex – 93c46
Toyota Allion – 93c56
Toyota Allion – 93c66 – 2003 year
Toyota Alphard – 93c56
Toyota Alteza – 93c46
Toyota Altiz – 93c46
Toyota Ardeo – 93c46
Toyota Aristo – 93c46 – Denso
Toyota Auris – 93c86 – 2007-2008 гг.
Toyota Avalon – 93c46 – 1998 г.в.4646 Toyota Avalon – 93c56 – 2008-2009 years
Toyota Avensis – 93c46
Toyota Avensis – 93c56 – 1998-1999 years
Toyota Avensis – 93c46 – 2004-2008 years
Toyota Avensis – 93c66 – 2009 year
Toyota Aygo – 93c56 – 2005 Год выпуска
Toyota BB – 93c46 – 2000-2002 гг. 93c46 - Ядзаки
Toyota Camry — 93c46 — 1996-2003 гг.
Toyota Camry — 93c56 — 2005-2010 гг.
Toyota Camry — 93c86 — 2007 г.
Toyota Chaser - 93C46
Toyota Chaser VDO - 93C46
Toyota Corolla - 93C46
Toyota Corolla - 93C46 - 1999 год
Toyota Corolla - 93C46 - от 2000 года
666 - 93c46 - 93 -й годы
- 93c46 - 93 - 946 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46 - 93c46. Тойота Королла – 93c86 – 2007-2008 years
Toyota Corolla – 93c46 – 2007 year
Toyota Corolla – 93c56 – 2008 year
Toyota Corolla Runx – 93c46
Toyota Corolla Verso – 93c46 – 2006 year
Toyota Corona – 93c46
Toyota Corona Premio – 93c66 – 2002
Toyota Cresta – 93c46 – 1997-1999 гг.
Toyota Cresta – 93c46 – 1997-1999 гг.3c46
Toyota Dyna – 93c56
Toyota Echo – 93c46 – 2000-2005 years
Toyota Emina – 93c46
Toyota Enigma – 93c66
Toyota Estima – 93c46 – 1996 year
Toyota Estima – 93c56 – 2007 year
Toyota Fielder – 93c46 – 2001- 2002 г. в.
в.
Toyota Fielder – 93c56 – 2007 г.в.
Toyota FJ Cruiser – 93c66 – 2007-2008 г.в.
Toyota Forerunner – 93c56 – 1998-2000 г.в. 2008 год
Toyota Funcargo-93C46-1999-2001 год
Toyota Funcargo-93LC46
Toyota Gaia-93C46
Toyota Gracia-93C46
Toyota Granvia-93C46-1996 год. — 1998-1999 гг.
Toyota HDJ100 Yazaki — 93c56
Toyota Hiace — 93c46 — 2002 г.
Toyota Hiace — 93c66 — 2007 г.
Toyota Hiace — 93c56 — 2008 г.3c66
Toyota Hilux – 93c46
Toyota Hilux – 93c56 – 2004-2006 years
Toyota Hilux – 93c66 – 2009-2010 years
Toyota Ipsum – 93c46 – 1996-1998 years
Toyota Ipsum – 93c46 – 1999 year
Toyota Isis – 93c66
Toyota IST — 93c66 — 2002 г.в. 1995 г.в.
Toyota Landcruiser 100 — 93c66 — 2004-2006 гг.
Toyota LandCruiser — 93c86 — 2007 г.
Toyota LandCruiser LC200 (Европа) — 93c86 — 2007-2009 гг.
Toyota LandCruiser LC200 (США) — 93c86 — 2007-2009 гг. Lucida — 93c46
Toyota Mark II — 93c46 — 1996-1999 гг.
Toyota Mark X — 93c57 — 2005 г.
Toyota Matrix — 93c46 — 2004 г. 93c46
Тойота Надя – 93C46
Toyota Noah-93C56-1999 год
Toyota Noah-93C46-2000 год
Toyota Noah-93C66-2002-2004 годы
Toyota Odyssey-93C46-1998 год
Toyot Odysey-93c56-93-2006-
год. Passo — 93c56
Toyota Picnic Yazaki — 93c46 — 1996-1998 гг.
Toyota Picnic — 93c46 — 2002 г. 93c66 – 2004-2008 гг.
Toyota Prada / Prado – 93c86 – 2010 year
Toyota Premio – 93c46
Toyota Premio – 93c66
Toyota Previa – 93c46
Toyota Previa – 93c57 – 2008 year
Toyota Prius – 93c46
Toyota Prius – 93c66 – 2004-2006 years
Toyota Probox - 93C46
Toyota Progres - 93C46
Toyota Sonard - 93C46
Toyota Qualis - 93C46
Toyota Ractis - 93–56 - 2005 год
Toyota Raum - 93C46
Toyota Raum - 93LC46OTA 93LC46OTA 93LC46OTA 93LC46OTA 946. 93c56 – 2002 г.в.
Toyota RAV 4 – 93c46 – 1996-2005 годы
Toyota RAV4 – 93c57 – 2006-2007 гг. 93C56-2006 год
93C56-2006 год
Toyota Spacio-24C02
Toyota Spacio-93C46
Toyota Sequoia-93C46-2001-2002 года
Toyota Sequoia-93C56-2002 год
Toyota Sequoia-93C5646-2002 год
Toyota Sequoia-93c5666-2002 год
Toyota Sequoia-93c566-2002 год
Toyota Sequia-93c56-2002 год
-
-2002 год
-93c56-2002 год
.
Toyota Sienna — 93c46 — 1999-2006 гг.
Toyota Sienna — 93c66 — 2010 г.
Toyota Sienta — 93c46
Toyota Soarer — TC
— 1993-1999 гг. -2000 г.в.
Toyota Spacio – 93c46 – 2001-2002 гг. 93c56 – 1998-2000 годы
Toyota Tacoma — 93c56 — 2006 год
Toyota Town Ace Noah — 93c46 — 1996-1998 годы
Toyota Town Ace Noah — 93c56 — 2000 год - 93C66
Toyota Uiris - 93C46
Toyota UZJ200 - 93C86 - 2008 год
Toyota Venza - 93C56
Toyota Venza - 93C66 - 2010 год
Toyota Verossa - 93C46
- 2010 год
-6666666666666666666666 - 9466. 93c56
Toyota Visra – 93c46
Toyota Vista – 93c46
Toyota Vista Ardeo – 93c46
Toyota Vitz – 93c46 – 2002 year
Toyota Vitz – 93c56 – 2006 year
Toyota Voltz – 93c46
Toyota Voxy – 93c56
Toyota Voxy – 93c66 – 2002
Toyota WiLL Vi – 93c46 – 2000 год
Toyota WiLL Cypha – 93c46
Toyota WiLL VS – 93c46
Toyota Windom – 93c46 – 2003 год - 2002 год
Toyota Yaris-93C56-2006-2007 годы
UAZ
UAZ Hunter-24C08
UAZ Simbir-24C08
VAZ (LADA)
VAZ (LADA) 21099 SCHETMASH-24C02
46464646464646464646464646464646.
ВАЗ (LADA) 2110 VDO — 93c56
ВАЗ (LADA) 2110 Счетмаш — 24c02
ВАЗ (LADA) 2110 Счетмаш — 25lc04 — 2007 г.в. (LADA) 2115 Счетмаш — 24lc02
ВАЗ (LADA) 2115 Счетмаш — 25lc04
ВАЗ (LADA) Калина — 93S56
Vaz (Lada) Kalina - 25LC04
Vaz (LADA) Kalina - 24LC65
VAZ (Chevrolet Niva) 2123 - 93S46
VAZ LADA LADA PROWA -NIVA) 2123 - 93S56
VAZA LADA LADA PriorA -niva) 2123 - 93S56
6 VAZA LADA LADA
Volvo
Volvo 850 Type 1 – 93c46
Volvo 850 Type 2 – 93c46
Volvo 850 – 93c56
Volvo 970 – 93c56 – 1996 year
Volvo S40 – 93c56 – 1996-2003 years
Volvo C30 – 9s12HZ256
Volvo S60 – 68HC908AZ32
Volvo S60 — 68HC912D60 — 2000-2001 годы
Volvo S60 – 68HC912DG128 – 2002 year
Volvo S60 – 68HC912DG128B – 2004 year
Volvo S70 – 93c56 – 1996-1997 years
Volvo S70 – 93c56 – 1998 year
Volvo S70 – 68HC908AZ32 – 1999-2000 years
Volvo S70 – 68HC912D60 – 2000 year
Volvo S70 – 68HC912DG128 – 2001 year
Volvo S80 – 68HC908AZ32 – 1999-2000 years
Volvo S80 – 68HC912D60 – 2000 year
Volvo S80 – 68HC912DG128 – 2001 year
Volvo S80 – 68HC912DG128B – 2004 year
Volvo S80 – 9s12DG128
Volvo S80 – 9s12h356
Volvo V40 – 93c56 – 1996-2003 years
Volvo V50 – 68HC912DG128B – 2004 year
Volvo V70 – 93c56 – 1996-1997 years
Volvo V70 – 93c56 – 1998 year
Volvo V70 – 68HC08AZ32 – 1998-2000 years
Volvo V70 – 68HC912D60 – 2001 year
Volvo V70 – 68HC912DG128 – 2001 year
Volvo V70 – 68HC912DG128B – 2003 year
Volvo XC70 – 9s12h356
Volvo XC90 – 68HC912DG128 – 2003 year
Volvo XC90 – 68HC912DG128B – 2005 year
VW
ЭБУ
EDC15-24C08-2000-2004 годы
VW VDO Generic-24C16 или 24C32
VW BORA-93C66
VW BORA 1-93C86
VW BORA 2-93C86
VW BORA BORA 3-936. 1999 year
1999 year
VW Bora – 93c86 – 2001 year
VW Bora – 93c86 – 2004 year
VW Bora – 24c02 – 2000-2001 year
VW Bora – 24c08 – 2001 year
VW Bora – 24c32 – 2006 year
VW Bora – 93c86 – 2007 г.
VW Caddy — 93c46
VW Caddy — 93c56 — 2002 г.
VW Caddy — 24c16 — 2004 г.
VW Corrado VDO — 24c32 — 2004-2007 гг.
VW Corrado VDO — 93c46 — 1993 г.
VW Corrado Motometer — 93c56 — 1991-1995 гг.
VW Crafter (EZS) — 9S12DT256 — 2007-2008 гг.
WV Fox — 93c66 — 2005 г.
VW Fox — MC9S12h356 — 2005 г.
Фольксваген Гол Тип 2 — 93s46
Фольксваген Гол — 68HC08AZ32
Фольксваген Гол — 68HC(7)05B16
VW Gol ws Тахометр — 68HC(7)05B16
VW Gol — 24c08 — 2004 г.в.
VW Gol 3 —
— 2006 г.в.
VW Gol 4 —
— 2006 г.в. — 2008 год
VW Gol Trend — 24c16 — 2009 год
VW GOLF 3 VDO — 93c46 — 1995 год
VW GOLF 3 VDO — 93c46 — SW 3.9 6.4
Мотометр для VW GOLF 3 — 93c56 — SW 5.6
Мотометр для VW GOLF 3 — 93c56 — SW 5. 8
8
VW GOLF 3 TRW — 93(l)c46 – 1991-1996 годы
VW GOLF 4 VDO – 93c46
VW GOLF 4 – 93c56
VW GOLF 4 VDO – 93c66
VW GOLF 4 – 24c04 – 1999 год
VW GOLF 4c04 – mod 9406 4 VDO VW GOLF 4 VDO – 93c86 – мод 2001
VW GOLF 4 VDO – 93c86 – 2002-2003 гг.
VW GOLF 4 Type 1 – 24c02 – 1999-2001 г.в. 4 GTI — 93c86 — 2002 г.в.
VW GOLF 4 — 24c08 — 2001-2002 гг.
VW GOLF 5 VDO — 24c16 — 2003-2005 гг.
VW GOLF 5 VDO — 24c32 — 2003-2006 гг.4646 VW Jetta-93C46-1994-1996 лет
VW Jetta-93C86-2001 год
VW Jetta-93C86-2002 год
VW Jetta-93C86-2003 год
VW Jetta-24C32-2005 год
46-2003 год
VW Jetta-24C32-2005 год
46-2003 год. Новый Жук-68HC912D60-1998 год
VW Новый жук-68HC912D60-2000 год
VW Новый жук-68HC912DG128-2003 год
VW New Beetle-9S12DG128-2003-го года
VW-NET-NEW-
.ETS
VW-9SEL -ET-
VW-9SET-
VW-9SET-
. 9С12х356 — 2006-2007 гг.
VW PASSAT VDO — 93c56 – 1991 г.в.
VW PASSAT VD202 – 93c46 – 1993 г. в. – 2000 г.
в. – 2000 г.
VW PASSAT B5 Тип 2 – 93c86 – 2000 г.
VW PASSAT B5 Тип 1 – 93c86 – 2001 г.
VW PASSAT B5 Тип 2 – 93c86 – 2001 г.
VW PASSAT B6 VDO Тип 1 – 93c86 VW PASSAT 9464 9464 Тип 2 – 93c86
VW PASSAT B6 VDO Тип 3 – 93c86
VW PASSAT VDO – 93C86-2003-2004 годы
VW Passat GT-93C46
VW Passat GT-93C56
VW Passat-93C56-1993-1996 года
VW Passat Motometer-93C56-SW 1,4
VW Passat Motometer-93C56-93C56-SW 1,4
VW Passat Motometer-93C56-93C56-SW 1,4
VW Passat-93C56-93C56-SW 1,4
VW Passat-93C56-93C56-SW 1,4
VW Passat-93C56-93C56-SW 1,4
VW. Motometer-24C08
VW Passat Jaeger Тип 1-68HC711KG2
VW Passat Jaeger Тип 2-68HC711KG2
VW Passat Jaeger-68HC711KG4
VW Passat Magneti-68HC711KG4–1
6666666666666666.6666.6666666.6666.666666.66666666666666666.666666666666666666.6666666666666666666.6666666666.6666666666666666666666666666666666666666666. Мотометр – 93c46
VW Polo Motometer-93C56-1995-1996 год
VW Polo Motometer-93C66-1996 год
VW Polo Motometer-24C02-1999 год
VW Polo Motometer-24C02-2002 год
VW VDO VDO-93C46-1996-198 год. VW POLO VDO – 93c86 – 2001 г.в.
VW POLO VDO – 93c86 – 2001 г.в.
VW POLO VDO Тип 1 – 93c86 – 2002-2003 гг.
VW POLO VDO Тип 2 – 93c86 – 2002-2003 г.в. VW Polo — 68HC912 — 2007 год
VW Sharan VDO Type 1 — 93c86 — 2000-2003 годы
VW Sharan VDO Type 2 — 93c86 — 2000-2003 гг.
VW Sharan — 68HC11A20 — 1996 г.
VW Sharan — 68HC11E9 — 1997-1998 гг.
VW Touran – 24c32 – 2004-2005 годы
VW T4 Мотометр – 93c56 – 1996-1997 годы
VW T4 VDO – 93c66 – 1996-1998 годы
VW T4 VDO – 93c86 – 11/1998-2006 годы VW T4 VDO лет – 93c86 – 2001 г.в.
VW T4 Тахограф – 24c04 – 2001 г.в.
VW T5 VDO – 93c86
VW T5 VDO - 93C86 - 2002 год
VW T5 VDO - 93C86 - 2003 год
VW T5 VDO - 93C86 - 2006 год
VW TUAREG - 93C46
VW TUAREG - 24C16 - 2003 год
. – 2004-2005 гг.
VW Tuareg – 24c08 – 2006 г.
VW Tuareg – 24c16 – 2007 г. – 93s46 – 1998-1999 годы
VW LT 35 – 24c02
VW Lupo – 24c02 – 1998 year
VW Phaeton Type 1 – 24c08
VW Phaeton Type 2 – 24c08
VW Pointer – 25040 – 2004-2005 year
VW Pointer – 93c66 – 2006 year
VW Santana – 93c46
VW Saveiro –
– 2004 year
VW Suran -
-2005-2007 годы
VW Suran-
-2007 год
VW VENTO TRW-93C46-1996-1997 лет
VW VENTO VDO-93C46-1992-1994 года
VW Volt-93C46-2005 год
voyage-946-946-n. 946-wyage-946-
946-wyage-946-6-wyage-93C46-2005 год
VOYAGE. — 2009 г.в.
VW xxxx Мотометр — 24c02
ЗАЗ
Таврия — 24c08
!ATV!
Honda Foreman — 93c46
Honda Foreman — 93c56
Honda Rubicon — 93c46
Honda Rubicon — 93c56
Polaris Sportsman — 93c66
!ВЕЛОСИПЕДЫ!
Aprilia
Aprilia Caponord – 24c02 – 2004 year
Aprilia Atlantic 500 – 24c01 – 2004 year
BMW
BMW GT1200 – 35080 – 2007-2009 years
Cagiva
Cagiva Raptor – 93c46
Harley Davidson
Harley Davidson – 93c46
Харлей Дэвидсон Спорт – 93c46
Harley Davidson — 25020 — 2005-2007 гг.
Harley Davidson — 93c66 — 2007 г.
Harley Davidson Night Rod — 93c66 — 2007-2008 гг. 2007-2008 годы
Hyosung
Hyosung 250-24C02
Honda
Honda 919 CB-93C56
Honda FR-V-93C66-2005 год
Honda CB400 Super Four-93C46-1994-9464 года
. Хонда CB1300 - 93c46
Honda CB1300 – 93c56
Honda CBF-600 – 93c56 – 2004 г. в.
в.
Honda CBR-600 – 93c56
Honda CBR-600 F4i – 93c56 – 2003 г.в. 900-93C56
Honda CBR-929-93C56-2001 год
Honda CBR-954-93C56-2001 год
Honda CBR-1000RR-93C56
Honda CBR1000RR-93C66-2008 Год. — 93c66 — 2006 год
Honda Dylon — 24LC02
Honda Deauville 700 — 93c56 — 2006 год
Honda FireBlade CBR-900 – 93c46
Honda FireBlade CBR-900RR – 93c46 – 2000 г.в.
Honda Hornet – 93c56 – 2005 г.в.
Honda Hornet – 93c66 – 2005-2006 гг. Honda SH-300 – 93c56 – 2007 year
Honda Shadow – 93c46
Honda Shadow 750 – 93c56 – 1999-2005 years
Honda ST1300 – 93c56
Honda Tornado – 24lc02
Honda Twister – 24c02 – 2000 year
Honda Twister – 24lc02
Honda Варадеро 1000 XL – 93c46 – 1999-2000 гг.
Honda Varadero – 24c02 – 2001 г.в.
Honda VFR-800 – 93c46
Honda VFR-800 Shadow – 93c56 – 2006 г.в. – 2001 year
Honda VTR-1000 Firestorm – 93c46
Honda VTX 1800 – 93c46
Honda Wildstar – 93c46
Honda X4 – 93c46
Honda X-11 – 93c46
Kawasaki
Kawasaki ER6 – 93c56
Kawasaki Ninja – 93c46
Kawasaki Z750 - 93c56 - 2004-2006 гг.
Kawasaki Z1000-93C56-2004 год
Kawasaki ZX-6R Ninja-93C46
Kawasaki ZX-6R-93C56
Kawasaki ZX-6R-93C56-2006 год
Kawasaki Zx-6r. -12R -93C46 -2004 год
KTM
KTM Adventure -93C56 -2005 год
KTM LC8 -93C56
KTM 690SM -24C02 -2007 год
MV AGUSTA
4 6C02 -2007 год
MV AGUSTA
464C02 -2007 год -
MV
464. Beverly 500 — 24c01
Piaggio Vespa 250 — 24c04 — 2007 год
Piaggio X9 – 24c01
Piaggio X9 200 Evolution – 24c02 – 2003 year
Suzuki
Suzuki Bandit – 93c56
Suzuki Burgman 400 – 93c46 – 1999 year
Suzuki Burgman 650 – 93c56 – 2004 year
Suzuki Djebel 250XC – 93c46
Suzuki DRZ400S - 93C46
Suzuki Freewind 650- 93C46- 2001 год
Suzuki GSF 600- 93C56
Suzuki GSF 1200- 93C56- 2001 год
Suzuki GSR 600- 93C56- 2006-
Suzuki GSR 600- 93C56- 2006-го года
Suzuki GSR 600- 93C56- 2006-го года
Suzuki GSR 600- 93C56- 2006-го года. 2005 год
Suzuki GSXR 650 – 93c56
Suzuki GSXF 750 – 93c46
Suzuki GSXR 750 – 93c56
Suzuki GSXR 750 – 93c56 – 2008 year
Suzuki GSXR 1000 – 93c56 – 2005-2006 years
Suzuki GSX 1300R – 93c56
Suzuki Hayabusa – 93c56
Suzuki Intruder-93C46
Suzuki R-1000-93C56
Suzuki R-1000-93C56-2008 год
Suzuki Raider 150-93C56-2005 год
Suzuki Skywave-93C46
-Suzuki 40046-93c44 Slaveave 400-93c44 Slabave 400-93c44 Slabave 400-93C46. 650 – 93C46-1997-2000 лет
650 – 93C46-1997-2000 лет
Suzuki SV 650-93C46-1999 год
Suzuki SV 650-93C46-2000-2002 годы
Suzuki TL 1000-93C46
Suzuki XV 650-93C46-2002 год
4646. Sym
Sym Joyride 200 - 93C46
Triumph
Triumph Sprint St - 93C66 - 2006 год
Triumph Tiger - 93c46
Yamaha
Yamaha Aprill
Ямаха ФЗ16 – 93c46 — 2010-2011 гг.
Yamaha FZS-300 Fazer — 93c46
Yamaha FZS-600 Fazer — 93c46 — 1999 г. 93C46
Ямаха Величество 400 - 93C56 - 2005 год
Yamaha R1 - 93C56 - 2003 год
yamaha R6 - 93C56 - 2008 год
Yamaha TDM 900 - 93C56
Yamaha TMAX - 93c46 - 2003 - 946 - 946 - 93 - 946 - 93 - 946 - 93 - 946 - 946 - 93 - 93c56
yamaha - 93 - 93 - 93 - 93c569
yamaha - 93 - 93 - 93 - 93c56
yamax - 93 - 93 - 93 - 93c56
. — 2008 год
Yamaha Tmax 500 — 93c66 — 2008 год
Yamaha TDM-850 — 93c46
Yamaha YZF-R1 — 93c46
Yamaha YZF-R6 — 93c46 — 2000-2001 гг.
Yamaha YZF-R6 — 93c56 — 2001-2003 гг. Yamaha X-Max 250 —
Yamaha X-Max 250 —
Yamaha XT660 — 24c02
Yamaha XV 1900 Midnight Star — 93c66 — 2008 год
!СНЕГОХОДЫ!
Bombardier Grand Touring – 93c46 – 1998-2000 годы
Bombardier – 24c01
Bombardier Type 1 – 9s12hz64 – 2009 год
Bombardier Type 2 – 9s12hz64
Bombardier Type 3 – 9s12hz64
Bombardier Type 4 – 9s12hz64
Bombardier Type 5 – 9s12hz64
Polaris – 93c46
Polaris – 93c66 – 2008-2009 years
Yamaha Apex – 93c66 – 2006 year
Yamaha Phaser – 93c66
Yamaha Rage – 93c56 – 2005 year
Yamaha RX1 – 93c56
Yamaha RX10 – 93c66
Yamaha RX Warrior – 93c56
!ДРУГИЕ ТРАНСПОРТНЫЕ СРЕДСТВА!
Беларусь
Беларусь — 24c08 — 2004 год
Беларусь — 93c66
Bobcat
ЭБУ Bobcat (часы) — X5083
CAMC
CAMC — 93c66
CASE
Case 210B (hours) – 93c46 – 2006 year
Dong Feng
Dong Feng – 93c66
Fendt
Fendt – 93c56 – 2003 year
Fendt – 24c04 – 2006 year
Fendt – 24c16 – 2008 year
Fendt Vario - 24C32 - 2008 год
Hitachi
Hitachi 16 - 93C56
JCB
JCB 3CX (часы) - PCF8582
JCB 3CX (часы) - PCF8582 - 2003 год
66666666666666666.
Тамрок
Тамрок – 93c66
Valmete
Valmete (часы) – 93c56
Terex
Terex (часы) – PCF8582E
(посещено 4990 раз, 1 посещение сегодня) и алгоритм лечения | Orphanet Journal of Rare Diseases
Orphanet Journal of Rare Diseases том 13 , номер статьи: 6 (2018)
Процитировать эту статью
Abstract
Наследственный ATTR (ATTRm) амилоидоз (также называемый семейной амилоидной полинейропатией транстиретинового типа [ATTR-FAP]) представляет собой аутосомно-доминантное, редкое системное заболевание, возникающее во взрослом возрасте, преимущественно характеризующееся необратимым, прогрессирующим и стойким поражением периферических нервов. . Мутации гена TTR (например, замена валина метионином в положении 30 [Val30Met (p.Val50Met)]) приводят к дестабилизации и диссоциации тетрамеров TTR на варианты мономеров TTR, которые образуют амилоидные фибриллы, откладывающиеся в периферических нервах и различных органах, вызывая периферическую и вегетативную невропатию и несколько неспецифических для заболевания симптомов.
Фенотипическая и генетическая изменчивость и неспецифические для заболевания симптомы часто задерживают диагностику и приводят к ошибочному диагнозу. Кластеры симптомов, вызывающих тревогу, упрощают диагностику во всем мире. Однако в Японии типы вариантов TTR, возраст начала, пенетрантность и клинические симптомы Val30Met более разнообразны, чем в других странах. Следовательно, развитие специфического для Японии кластера красных флажков является оправданным. Наличие прогрессирующей периферической сенсорно-моторной полинейропатии и ≥1 настораживающего признака/симптома (например, семейный анамнез, вегетативная дисфункция, поражение сердца, синдром запястного канала, желудочно-кишечные расстройства, необъяснимая потеря веса и резистентность к иммунотерапии) предполагают ATTR-FAP. За пределами Японии фармакотерапевтические варианты являются терапией первой линии. Однако из-за положительных результатов (более высокая ожидаемая продолжительность жизни и более высокие показатели выживаемости) при трансплантации от живого донора в Японии трансплантация печени остается терапией первой линии, что требует специфического для Японии алгоритма лечения.
В данном документе мы представляем сводный обзор ландшафта ATTR-FAP Val30Met в Японии и обобщаем результаты совещания медицинского консультативного совета, состоявшегося в Токио 18 августа 2016 г., на котором специфический для Японии кластер симптомов ATTR-FAP с красными флажками и разработан алгоритм лечения. Помимо трансплантации печени, вариантом лечения является препарат, стабилизирующий TTR (например, тафамидис). Ранняя диагностика и своевременное лечение с использованием специфичного для Японии кластера симптомов и алгоритма лечения могут помочь клиницистам правильно и разумно использовать доступные методы лечения.
Исходная информация
Семейная амилоидная полинейропатия транстиретинового типа (ATTR-FAP) или наследственный транстиретиновый амилоидоз (ATTRm-амилоидоз) представляет собой аутосомно-доминантное, редкое системное заболевание, возникающее во взрослом возрасте, преимущественно характеризующееся необратимым, прогрессирующим и персистирующим поражением периферических нервов. повреждения [1, 2]. ATTR-FAP может проявляться как прогрессирующая, аксональная, сенсорная вегетативная и моторная нейропатия, рестриктивная кардиомиопатия (транстиретиновая кардиомиопатия) или как церебральная амилоидная ангиопатия; однако большинство случаев классифицируются как нейропатические [1]. При анализе данных Министерства здравоохранения, труда и социального обеспечения Японии (MHLW) за 2003–2005 гг. было обнаружено 110,8–135,4 случая семейного амилоидоза, что соответствует расчетной распространенности 0,87–1,1 на 1 000 000 человек; самая высокая распространенность была в префектуре Нагано, за которой следуют Кумамото и Исикава (11,0–15,5, 10,1–10,3 и 3,5–4,2 на 1 000 000 человек соответственно) [3].
повреждения [1, 2]. ATTR-FAP может проявляться как прогрессирующая, аксональная, сенсорная вегетативная и моторная нейропатия, рестриктивная кардиомиопатия (транстиретиновая кардиомиопатия) или как церебральная амилоидная ангиопатия; однако большинство случаев классифицируются как нейропатические [1]. При анализе данных Министерства здравоохранения, труда и социального обеспечения Японии (MHLW) за 2003–2005 гг. было обнаружено 110,8–135,4 случая семейного амилоидоза, что соответствует расчетной распространенности 0,87–1,1 на 1 000 000 человек; самая высокая распространенность была в префектуре Нагано, за которой следуют Кумамото и Исикава (11,0–15,5, 10,1–10,3 и 3,5–4,2 на 1 000 000 человек соответственно) [3].
TTR — гомотетрамерный транспортный белок плазмы, несущий тироксин и ретинол-связывающий белок, — продуцируется в основном в печени, но также в сосудистом сплетении и пигментном эпителии сетчатки и секретируется в кровь, спинномозговую жидкость и глаза, соответственно. 1, 4,5,6,7,8,9].
Во всем мире выявлено более 130 различных мутаций гена TTR , из которых >40 мутаций связаны с ATTR-FAP в Японии (таблица 1). Однако замена валина на метионин в положении 30 (ATTR-FAP Val30Met [p.Val50Met]) является наиболее часто наблюдаемой мутацией, единственной, обнаруживаемой в крупных очагах больных, и ассоциированной в первую очередь с нейропатией [1, 10]. Мутации гена TTR дестабилизируют TTR, приводя к диссоциации тетрамеров и частичному разворачиванию образующихся мономеров. Различные мономеры TTR агрегируют с образованием амилоидных фибрилл [1, 11, 12, 13]. Из-за диффузного отложения амилоидных фибрилл (например, во внеклеточном пространстве периферических нервов, сердца, желудочно-кишечного тракта, почек, глаз, мозговых оболочек, сосудов и соединительной ткани поперечной связки запястья) [14] ATTR-FAP связан с различными симптомами. , многие из которых неспецифичны [1, 11, 15]. Начало заболевания в период между 10 и 90s, как правило, классифицируется как раннее начало (<50 лет) и позднее начало (≥50 лет) [16, 17]. Примерно в течение 10 лет от начала заболевания происходит прогрессирующая органная дисфункция и смерть (из-за сердечной дисфункции, инфекции или кахексии) [1, 18,19,20,21]. Несколько исследований показали, что начало симптомов ATTR-FAP в Японии является бимодальным, с одним пиком, приходящимся на период от 30 до 40 лет (раннее начало), и другим отчетливым пиком в 60 лет (позднее начало) [1, 3, 16, 22]. ,23,24]. Напротив, в других странах наблюдается один пик появления симптомов (например, между 25 и 35 годами со средним значением 33,5 года в Португалии и в 50-х или 60-х годах в Швеции) [25, 26, 27] (рис. 1; Pfizer Inc. ., данные в файле).
Примерно в течение 10 лет от начала заболевания происходит прогрессирующая органная дисфункция и смерть (из-за сердечной дисфункции, инфекции или кахексии) [1, 18,19,20,21]. Несколько исследований показали, что начало симптомов ATTR-FAP в Японии является бимодальным, с одним пиком, приходящимся на период от 30 до 40 лет (раннее начало), и другим отчетливым пиком в 60 лет (позднее начало) [1, 3, 16, 22]. ,23,24]. Напротив, в других странах наблюдается один пик появления симптомов (например, между 25 и 35 годами со средним значением 33,5 года в Португалии и в 50-х или 60-х годах в Швеции) [25, 26, 27] (рис. 1; Pfizer Inc. ., данные в файле).
Таблица 1 Генетические мутации, связанные с ATTR-FAP, в Японии Полноразмерная таблица
Рис. 1 Кумулятивное начало симптоматического заболевания: Val30Met в четырех странах
Полноразмерное изображение
В дополнение к гетерогенности амилоида 3978TR19 мутации и вариабельность возраста начала заболевания, фенотипическая гетерогенность на различных уровнях затрудняют диагностику ATTR-FAP. Носители одной и той же точечной мутации TTR могут иметь очень разные клинические проявления даже среди членов семьи [1]. Кроме того, отсутствие семейного анамнеза в неэндемичных районах и спорадические случаи представляют дополнительные диагностические проблемы [28,29].,30,31]. Поскольку ATTR-FAP является прогрессирующим заболеванием и может вызывать в значительной степени необратимое повреждение тканей, своевременное распознавание и диагностика имеют решающее значение для надлежащего лечения и оптимальных результатов [32,33,34]. К сожалению, диагностика ATTR-FAP часто задерживается из-за фенотипической и генетической изменчивости, разнообразной клинической картины и неспецифического характера большинства симптомов [1, 19, 30, 31, 35]. Неправильный диагноз также может возникать по аналогичным причинам (см. Общие диагностические ошибки).
Носители одной и той же точечной мутации TTR могут иметь очень разные клинические проявления даже среди членов семьи [1]. Кроме того, отсутствие семейного анамнеза в неэндемичных районах и спорадические случаи представляют дополнительные диагностические проблемы [28,29].,30,31]. Поскольку ATTR-FAP является прогрессирующим заболеванием и может вызывать в значительной степени необратимое повреждение тканей, своевременное распознавание и диагностика имеют решающее значение для надлежащего лечения и оптимальных результатов [32,33,34]. К сожалению, диагностика ATTR-FAP часто задерживается из-за фенотипической и генетической изменчивости, разнообразной клинической картины и неспецифического характера большинства симптомов [1, 19, 30, 31, 35]. Неправильный диагноз также может возникать по аналогичным причинам (см. Общие диагностические ошибки).
За последнее десятилетие ситуация с ATTR-FAP и его лечением резко изменилась в Японии: по сообщениям, благодаря повышению осведомленности о заболевании число пациентов с ATTR-FAP в этой стране увеличилось со 110,8 до 135,4 [3]. примерно до 300 (Sekijima et al., неопубликованные наблюдения). Что касается лечения, трансплантация печени (ТП) была единственным стандартом лечения с 19 века.90-е [1, 36,37,38,39,40,41]; однако в начале 2010-х годов возможности лечения были расширены с появлением минимально инвазивной, модифицирующей заболевание фармакотерапии, такой как тетрамерный стабилизатор TTR [1, 35, 42]. Тем не менее, ряд пациентов с ATTR-FAP до сих пор остаются невыявленными и, следовательно, не лечатся из-за разнообразных клинических проявлений и различных неспецифических симптомов заболевания; особенно в Японии, наличие различных типов пациентов (например, Val30Met с ранним началом в эндемичных районах, Val30Met с поздним началом в неэндемичных районах, варианты без Val30Met, основными симптомами которых являются кардиомиопатия, синдром запястного канала или церебральная амилоидная ангиопатия) часто затрудняет точную диагностику [15, 16, 24, 43,44,45].
примерно до 300 (Sekijima et al., неопубликованные наблюдения). Что касается лечения, трансплантация печени (ТП) была единственным стандартом лечения с 19 века.90-е [1, 36,37,38,39,40,41]; однако в начале 2010-х годов возможности лечения были расширены с появлением минимально инвазивной, модифицирующей заболевание фармакотерапии, такой как тетрамерный стабилизатор TTR [1, 35, 42]. Тем не менее, ряд пациентов с ATTR-FAP до сих пор остаются невыявленными и, следовательно, не лечатся из-за разнообразных клинических проявлений и различных неспецифических симптомов заболевания; особенно в Японии, наличие различных типов пациентов (например, Val30Met с ранним началом в эндемичных районах, Val30Met с поздним началом в неэндемичных районах, варианты без Val30Met, основными симптомами которых являются кардиомиопатия, синдром запястного канала или церебральная амилоидная ангиопатия) часто затрудняет точную диагностику [15, 16, 24, 43,44,45].
Ввиду огромной вероятности ошибочного диагноза или отсроченного диагноза Conceição и его коллеги сообщили о кластерах симптомов с красными флажками, наводящих на мысль о ATTR-FAP и алгоритмах лечения [46]. Однако эти кластеры и алгоритмы не обязательно применимы к Японии, поскольку ситуации, характерные для этой страны (например, наличие различных типов пациентов), не полностью отражены. Здесь мы представляем сводный обзор мировой картины ATTR-FAP и нашего опыта лечения японских пациентов с ATTR-FAP, чтобы предложить пересмотренные кластеры симптомов красного флага и алгоритм лечения.
Однако эти кластеры и алгоритмы не обязательно применимы к Японии, поскольку ситуации, характерные для этой страны (например, наличие различных типов пациентов), не полностью отражены. Здесь мы представляем сводный обзор мировой картины ATTR-FAP и нашего опыта лечения японских пациентов с ATTR-FAP, чтобы предложить пересмотренные кластеры симптомов красного флага и алгоритм лечения.
Методы
Авторы (YS, MU, HK, SM и YA) провели собрание медицинского консультативного совета в Токио, Япония, 18 августа 2016 г. с целью продвижения ранней диагностики и достижения консенсуса в отношении диагностики и лечения ATTR. -FAP Val30Met в Японии. Кластеры тревожных симптомов и алгоритм лечения, представленные в этой статье, разработаны в соответствии с выводами этого заседания медицинского консультативного совета.
Клинические признаки
ATTR-FAP Val30Met может быть эндемичным (т. е. локализованным на небольшой территории, с прослеживаемой семейной историей и ранним началом заболевания) или неэндемичным (т. е. рассеянным, часто без семейного анамнеза и поздним началом заболевания). начало заболевания) [3, 16, 29,30,31, 34, 47]. Клиническая картина ATTR-FAP различается у пациентов из эндемичных и неэндемичных районов [1, 15, 16, 48]. Как правило, у пациентов из эндемичных районов болезнь начинается рано, а у пациентов из неэндемичных районов болезнь проявляется поздно [15, 16, 20, 44, 49]. Однако в Японии, несмотря на идентичный генотип TTR и в целом однородную этническую принадлежность, были идентифицированы два основных фенотипа ATTR-FAP Val30Met: ранний и эндемичный (Нагано и Кумамото) и поздний и неэндемичный [16]. , 20, 31]. Общие клинические признаки раннего и эндемического фенотипа в Японии напоминают таковые у португальских пациентов с FAP [10, 27, 50, 51], в то время как клинические признаки позднего фенотипа в неэндемичных районах отличаются от этих фенотипов [16]. , 20, 31]. Различия в клинических признаках между заболеванием с ранним и поздним началом представлены в таблице 2.
е. рассеянным, часто без семейного анамнеза и поздним началом заболевания). начало заболевания) [3, 16, 29,30,31, 34, 47]. Клиническая картина ATTR-FAP различается у пациентов из эндемичных и неэндемичных районов [1, 15, 16, 48]. Как правило, у пациентов из эндемичных районов болезнь начинается рано, а у пациентов из неэндемичных районов болезнь проявляется поздно [15, 16, 20, 44, 49]. Однако в Японии, несмотря на идентичный генотип TTR и в целом однородную этническую принадлежность, были идентифицированы два основных фенотипа ATTR-FAP Val30Met: ранний и эндемичный (Нагано и Кумамото) и поздний и неэндемичный [16]. , 20, 31]. Общие клинические признаки раннего и эндемического фенотипа в Японии напоминают таковые у португальских пациентов с FAP [10, 27, 50, 51], в то время как клинические признаки позднего фенотипа в неэндемичных районах отличаются от этих фенотипов [16]. , 20, 31]. Различия в клинических признаках между заболеванием с ранним и поздним началом представлены в таблице 2. ATTR-FAP с ранним началом обычно начинается в период от 20 до 40 лет и характеризуется преимущественной потерей поверхностной чувствительности, включая ноцицепцию и температурную чувствительность ( сенсорная диссоциация), наличие семейного анамнеза, высокий уровень пенетрантности, тяжелая вегетативная дисфункция и блокада атриовентрикулярной проводимости, требующая имплантации кардиостимулятора [15, 16, 49]., 52,53,54]. С другой стороны, заболевание с поздним началом начинается после 50 лет и характеризуется сенсомоторными симптомами, начинающимися в дистальных отделах нижних конечностей, первоначальным вовлечением как поверхностной, так и глубокой чувствительности, потерей всех сенсорных модальностей, а не сенсорной диссоциацией, низкой скоростью пенетрантности. относительно легкая вегетативная дисфункция, частое наличие кардиомегалии и крайнее преобладание мужского пола [15, 16, 24, 31, 55]. Генетическое предвосхищение часто считается отличительной чертой из-за его присутствия при раннем начале заболевания и его отсутствия при позднем начале заболевания [43, 56].
ATTR-FAP с ранним началом обычно начинается в период от 20 до 40 лет и характеризуется преимущественной потерей поверхностной чувствительности, включая ноцицепцию и температурную чувствительность ( сенсорная диссоциация), наличие семейного анамнеза, высокий уровень пенетрантности, тяжелая вегетативная дисфункция и блокада атриовентрикулярной проводимости, требующая имплантации кардиостимулятора [15, 16, 49]., 52,53,54]. С другой стороны, заболевание с поздним началом начинается после 50 лет и характеризуется сенсомоторными симптомами, начинающимися в дистальных отделах нижних конечностей, первоначальным вовлечением как поверхностной, так и глубокой чувствительности, потерей всех сенсорных модальностей, а не сенсорной диссоциацией, низкой скоростью пенетрантности. относительно легкая вегетативная дисфункция, частое наличие кардиомегалии и крайнее преобладание мужского пола [15, 16, 24, 31, 55]. Генетическое предвосхищение часто считается отличительной чертой из-за его присутствия при раннем начале заболевания и его отсутствия при позднем начале заболевания [43, 56]. Однако возникновение ожидания может быть переоценено, поскольку не все бессимптомные люди проходят молекулярно-генетическое тестирование, и, следовательно, некоторые бессимптомные люди с вариантом Val30Met могут быть не идентифицированы [57].
Однако возникновение ожидания может быть переоценено, поскольку не все бессимптомные люди проходят молекулярно-генетическое тестирование, и, следовательно, некоторые бессимптомные люди с вариантом Val30Met могут быть не идентифицированы [57].
Таблица 2. Сравнение клинических признаков ATTR-FAP с ранним и поздним началом Полноразмерная таблица
Клинические и параклинические признаки ATTR-FAP представлены на рис. 2. сенсорно-моторная невропатия является отличительной чертой ATTR-FAP [1, 15]. В ряде ранее опубликованных исследований обсуждались начальные симптомы у пациентов с ATTR-FAP в Японии [15, 16, 20, 31, 45, 46, 50]. Начальные симптомы у японских пациентов с ATTR-FAP представлены в Таблице 3. Симптомы ATTR-FAP можно в целом разделить на нейропатические симптомы и другие системные симптомы, как описано ниже.
Рис. 2 Клинические и параклинические особенности ATTR-FAP. BNP Натрийуретический пептид мозга, TC-PYP TC-пирофосфат Сцинтиграфия, MIBG Метаоидобензилгуанидин.
При классическом заболевании с ранним началом поражение сначала наблюдается в дистальных отделах мелких миелинизированных и немиелинизированных нервных волокон, что связано с болью и температурой и проявляется парестезиями, дизестезиями, аллодиниями, гипералгезией или спонтанными болями в стопах [15, 16] и нарушением теплового режима. чувствительность со снижением ощущения покалывания при клиническом осмотре [1, 15, 16]. В последующие годы поражаются более крупные миелинизированные чувствительные и двигательные нервные волокна, что приводит к нарушению легкого прикосновения, вибрации и ощущения положения. Дальнейшее прогрессирование в зависимости от длины приводит к моторному дефициту дистальных отделов нижних конечностей, что приводит к затруднению ходьбы и слабости [15]. При позднем дебюте сохраняются немиелинизированные нервные волокна и наблюдается прорастание аксонов [15]. Вегетативная дисфункция проявляется половым бессилием; нарушения моторики желудочно-кишечного тракта, чаще всего диарея, чередующаяся с запорами, а также запоры, диарея, тошнота и рвота; ортостатическая гипотензия; и нейрогенный мочевой пузырь [16, 20, 58]. Эти вегетативные симптомы относительно легкие при позднем начале заболевания, особенно в ранней фазе невропатии [16, 20]. Симптомы нижних конечностей обычно предшествуют симптомам верхних конечностей на несколько лет при раннем начале заболевания, в то время как поражение верхних и нижних конечностей может проявляться одновременно при позднем начале заболевания [20]. Иногда синдром запястного канала (CTS) может появиться у пациентов с не-Val30Met и привести к диагнозу при прогрессировании системной невропатии после операции по освобождению запястного канала [1, 59].,60,61,62].
Эти вегетативные симптомы относительно легкие при позднем начале заболевания, особенно в ранней фазе невропатии [16, 20]. Симптомы нижних конечностей обычно предшествуют симптомам верхних конечностей на несколько лет при раннем начале заболевания, в то время как поражение верхних и нижних конечностей может проявляться одновременно при позднем начале заболевания [20]. Иногда синдром запястного канала (CTS) может появиться у пациентов с не-Val30Met и привести к диагнозу при прогрессировании системной невропатии после операции по освобождению запястного канала [1, 59].,60,61,62].
Другие системные симптомы
Помимо нервной ткани, амилоидные фибриллы могут откладываться в различных органах и тканях, что приводит к прогрессирующей дисфункции [1, 14, 15, 63, 64, 65, 66]. Отложение амилоида в медии и адвентиции средних и мелких артерий, артериол и, иногда, вен субарахноидального пространства, лептоменинх и коры головного мозга приводит к транзиторным очаговым неврологическим эпизодам, инфаркту и кровоизлиянию в мозг, гидроцефалии, атаксии, спастическому параличу. , судороги и деменция [1, 61, 62, 64, 67]. Инфильтрация амилоидными фибриллами в сердечно-сосудистые структуры, такие как проводящая система, может привести к блокаде ножек пучка Гиса, а иногда и к атриовентрикулярной и синоатриальной блокаде [15]. Инфильтрация миокарда может привести к кардиомиопатии с гипертрофическим фенотипом и рестриктивной патофизиологией [1, 68]. Отложение амилоидных фибрилл в глазу может вызывать глазные проявления, такие как аномальные сосуды конъюнктивы, сухой кератоконъюнктивит, аномалии зрачка, помутнение стекловидного тела и глаукому [69].]. Отложение амилоидных фибрилл в почках может привести к микроальбуминурии, которая часто предшествует субъективным симптомам ATTR-FAP. Поражение почек, включая нефритический синдром и прогрессирующую почечную недостаточность, встречается примерно у трети пациентов в Португалии [70]; однако тяжелая почечная дисфункция редко возникает у японских пациентов с ATTR-FAP. Кроме того, поскольку почки являются основным местом выработки эритропоэтина, может развиться анемия из-за значительно более низких уровней эритропоэтина в сыворотке [71].
, судороги и деменция [1, 61, 62, 64, 67]. Инфильтрация амилоидными фибриллами в сердечно-сосудистые структуры, такие как проводящая система, может привести к блокаде ножек пучка Гиса, а иногда и к атриовентрикулярной и синоатриальной блокаде [15]. Инфильтрация миокарда может привести к кардиомиопатии с гипертрофическим фенотипом и рестриктивной патофизиологией [1, 68]. Отложение амилоидных фибрилл в глазу может вызывать глазные проявления, такие как аномальные сосуды конъюнктивы, сухой кератоконъюнктивит, аномалии зрачка, помутнение стекловидного тела и глаукому [69].]. Отложение амилоидных фибрилл в почках может привести к микроальбуминурии, которая часто предшествует субъективным симптомам ATTR-FAP. Поражение почек, включая нефритический синдром и прогрессирующую почечную недостаточность, встречается примерно у трети пациентов в Португалии [70]; однако тяжелая почечная дисфункция редко возникает у японских пациентов с ATTR-FAP. Кроме того, поскольку почки являются основным местом выработки эритропоэтина, может развиться анемия из-за значительно более низких уровней эритропоэтина в сыворотке [71].
Неспецифические симптомы
Потеря веса, истощение и атрофия мышц, охриплость, похолодание, снижение температуры кожи, дискория, дизестезия, диссоциированная анестезия, аритмия, отек, жжение и сустав Шарко также могут присутствовать у пациентов с ATTR-FAP [1, 16].
Специфические для Японии кластеры симптомов красного флага
Характерными признаками ATTR-FAP являются наследуемость и мультисистемное вовлечение [46]. Кластеры симптомов красного флага, наводящие на размышления о ATTR-FAP, о которых сообщил Conceição и его коллеги, включали: семейный анамнез; ранняя вегетативная дисфункция; желудочно-кишечные жалобы; необъяснимая потеря веса; сердечная гипертрофия, аритмии, желудочковые блокады или кардиомиопатия; двусторонний КТС; почечные аномалии; и помутнения стекловидного тела [46]. В свете опубликованной литературы и экспертного мнения медицинского консультативного совета кластеры симптомов с красными флажками, предполагающие ATTR-FAP в Японии, рассмотрены и представлены ниже (рис. 3). Наличие прогрессирующей периферической сенсорно-моторной полинейропатии и ≥1 из следующих настораживающих признаков и/или симптомов свидетельствует о ATTR-FAP.
3). Наличие прогрессирующей периферической сенсорно-моторной полинейропатии и ≥1 из следующих настораживающих признаков и/или симптомов свидетельствует о ATTR-FAP.
Рис. 3 Кластеры симптомов, вызывающих тревогу, специфичные для ATTR-FAP Val30Met в Японии. E early-onset Val30Met, L late-onset Val30Met, N non-Val30Met, BNP brain natriuretic peptide, Tc-PYP Tc-pyrophosphate scintigraphy, MIBG metaiodobenzylguanidine
Full size image
Желудочно-кишечные симптомы
Желудочно-кишечные симптомы, такие как тошнота, раннее чувство насыщения, периодическая рвота, водянистая диарея, тяжелый запор и/или чередование диареи и запора, возникающие как проявления вегетативной невропатии, документированы на ранних стадиях ATTR-FAP [1] и начальные симптомы почти в половине случаев с ранним началом в эндемичных районах [16, 72, 73]. У пациентов из неэндемичных районов в основном наблюдаются симптомы со стороны нижних отделов желудочно-кишечного тракта, такие как диарея и/или запор [20]. Примечательно, что у японских пациентов желудочно-кишечные расстройства начинаются раньше, чем у шведских пациентов [74], что делает это важным тревожным симптомом у японских пациентов.
Примечательно, что у японских пациентов желудочно-кишечные расстройства начинаются раньше, чем у шведских пациентов [74], что делает это важным тревожным симптомом у японских пациентов.
Синдром запястного канала
CTS является ранним, но неспецифическим ортопедическим проявлением ATTR-FAP. Часто пациентам с ATTR-FAP изначально ошибочно ставят диагноз идиопатического CTS, а прогрессирующие симптомы или отсутствие улучшения после операции по освобождению часто приводят к правильному диагнозу. Таким образом, CTS без очевидной причины, особенно двусторонний CTS, который требует хирургического освобождения, должен вызвать подозрение на ATTR-FAP [1]. В ретроспективном обсервационном исследовании с участием 76 итальянских пациентов с ATTR-FAP CTS был первым симптомом у 33% пациентов без каких-либо других клинических проявлений в течение среднего периода 4,6–5,6 лет [75]. Аналогичным образом, в исследовании с участием 31 японского пациента с диагнозом системный транстиретиновый амилоидоз дикого типа в университетской больнице Шиншу, CTS был наиболее частым начальным симптомом, что указывает на то, что тщательное обследование пациентов с CTS может привести к более ранней диагностике [76].
Необъяснимая потеря веса
Непреднамеренная потеря веса часто наблюдается у пациентов с ATTR-FAP из-за желудочно-кишечных расстройств [1]. Кахексия является основной причиной смерти у пациентов с ранним началом ATTR-FAP Val30Met из эндемичных очагов в Японии и Португалии [50, 73, 77].
Вегетативная дисфункция
Хотя сенсорные и двигательные проявления обычно являются симптомами, вегетативная дисфункция может быть первым клиническим проявлением в случаях с ранним началом [49].]. В общенациональном опросе, проведенном Исследовательской группой по наследственной невропатии (под эгидой MHLW), вегетативная дисфункция была первоначальной жалобой в 48% случаев с ранним началом и 10% случаев с поздним началом [16]. Вегетативные симптомы при ATTR-FAP с поздним началом обычно слабо выражены на ранней стадии заболевания [31]. Однако вегетативная дисфункция обычно становится очевидной на более поздней стадии заболевания, даже в случаях с поздним началом [20]. Кроме того, поскольку недостаточное внимание неврологов к вегетативным симптомам является серьезной диагностической ошибкой при ATTR-FAP, особое внимание следует уделять пациентам с одновременной вегетативной дисфункцией, CTS и поражением сердца [1, 19]. , 31].
, 31].
Поражение сердца
Приблизительно у 50% пациентов с ATTR-FAP возникают заболевания сердца [1], и сердечная дисфункция является основной причиной смерти, особенно среди пациентов из неэндемичных районов [20, 78]. Хотя признаки и симптомы заболеваний сердца обычно появляются на поздних стадиях ATTR-FAP, ранние оценки могут выявить поражение сердца [20]. Обнаружение субклинического поражения сердца (например, кардиомегалия на рентгенограмме грудной клетки, утолщение межжелудочковой перегородки и зернистое мерцание на эхокардиографии [31]) может помочь диагностировать ATTR-FAP Val30Met с поздним началом у пациентов без семейного анамнеза заболевания [79].]. Кроме того, обнаружение поглощения технеция-99m-пирофосфата с помощью сцинтиграфии сердца помогает ранней диагностике TTR-сердечного амилоидоза с высокой чувствительностью и специфичностью [80, 81].
Семейный анамнез
В вышеупомянутом общенациональном исследовании, проведенном в Японии, семейный анамнез ATTR-FAP Val30Met был обнаружен в 94% случаев с ранним началом и 48% случаев с поздним началом [16]. Несмотря на более низкую частоту семейного анамнеза среди пациентов с поздним началом заболевания и в неэндемичных районах [16, 24, 79], кластеры симптомов красного флага должны вызывать подозрение на ATTR-FAP, особенно у лиц с семейным анамнезом. Кроме того, опытные неврологи в эндемичных районах могут диагностировать ATTR-FAP исключительно на основании семейного анамнеза и клинических признаков [1, 46].
Несмотря на более низкую частоту семейного анамнеза среди пациентов с поздним началом заболевания и в неэндемичных районах [16, 24, 79], кластеры симптомов красного флага должны вызывать подозрение на ATTR-FAP, особенно у лиц с семейным анамнезом. Кроме того, опытные неврологи в эндемичных районах могут диагностировать ATTR-FAP исключительно на основании семейного анамнеза и клинических признаков [1, 46].
Резистентность к иммунотерапии
Отсутствие ответа на иммуномодулирующее лечение помогает дифференцировать ATTR-FAP от хронической воспалительной демиелинизирующей полинейропатии (ХВДП), которая является наиболее распространенным ошибочным диагнозом, если связана с неуклонным прогрессированием невропатии, аксональным паттерном и вегетативной дисфункцией. 31, 46].
Знание и осведомленность врачей Японии о вышеуказанном кластере симптомов, вызывающих тревогу, может дать практическое руководство и способствовать раннему выявлению и диагностике заболевания в этой стране.
Диагностика
Диагностика ATTR-FAP включает два основных этапа [82]:
Рис. 4 Средства диагностики и последующие оценки для ATTR-FAP. BNP мозговой натрийуретический пептид, ЭКГ электрокардиограмма, NDS балл неврологической инвалидности, NIS балл нейропатии, PND инвалидность полиневропатии, SSR симпатическая кожная реакция, TTR транстиретин. a Rowczenio DM, et al. 2014 [94]
a Rowczenio DM, et al. 2014 [94]
Изображение в натуральную величину
Анамнез пациента и физикальное обследование
Необходимо тщательно собрать анамнез пациента для выявления наличия семейного анамнеза и мультисистемных настораживающих признаков и/или симптомов [1, 82 ]. При отсутствии семейного анамнеза амилоидоза диагноз ATTR-FAP следует рассматривать у пациентов с прогрессирующей, зависящей от длины, аксональной полинейропатией, преимущественно поражающей температуру и болевые ощущения [1] (рис. 4). После постановки диагноза модифицированный индекс массы тела (mBMI) как мера статуса питания полезен для мониторинга прогрессирования или прогноза ATTR-FAP [1, 83].
Гистопатология
Биопсия ткани: Демонстрация отложений амилоида с помощью биопсии ткани необходима для подтверждения диагноза ATTR-FAP, особенно у пациентов без семейного анамнеза [1, 84, 85]. Биопсия ткани с использованием красителя Конго красный [85] непосредственно выявляет отложения амилоида в пораженных тканях, включая губную слюнную железу и подкожную жировую ткань брюшной полости, желудочно-кишечный тракт, нервную ткань и другие органы с признаками поражения [18, 31, 86,87, 88,89,90]. Иммуномаркирование TTR амилоидных отложений помогает идентифицировать TTR-амилоидоз [82], но не способствует дифференциации между ATTR дикого типа (ATTRwt) и мутантным ATTR (ATTRm). Кроме того, при наличии типичных признаков и симптомов отрицательные результаты биопсии не исключают ATTR-FAP [1] (рис. 4).
Иммуномаркирование TTR амилоидных отложений помогает идентифицировать TTR-амилоидоз [82], но не способствует дифференциации между ATTR дикого типа (ATTRwt) и мутантным ATTR (ATTRm). Кроме того, при наличии типичных признаков и симптомов отрицательные результаты биопсии не исключают ATTR-FAP [1] (рис. 4).
Генетическое тестирование
У пациентов с подозрением на ATTR-FAP следует провести генотипирование TTR для документирования специфических патогенных TTR мутаций; генотипирование является наиболее надежным диагностическим подходом, а отсутствие патогенной мутации исключает диагноз ATTR-FAP [1, 82]. Генопозитивность TTR должна быть установлена с помощью анализа ДНК во всех подозрительных случаях [1, 30, 91,92,93]. У пациентов, имеющих семейный анамнез с предыдущим диагнозом, можно использовать целенаправленный подход для выявления патогенной мутации. При отсутствии семейного анамнеза и у пациентов с атипичными симптомами 9Секвенирование гена 7188 TTR может потребоваться для выявления подозреваемых и новых патогенных мутаций [35, 57]. Кроме того, онлайн-реестр окажется полезным для исследования амилоидогенных мутаций TTR [94] (рис. 4).
Кроме того, онлайн-реестр окажется полезным для исследования амилоидогенных мутаций TTR [94] (рис. 4).
Сывороточный вариант белка TTR
Белок TTR обычно циркулирует в сыворотке как растворимый белок с тетрамерной структурой. Нормальная концентрация TTR в сыворотке составляет от 0,20 до 0,40 мг/мл (от 20 до 40 мг/дл) [57, 95, 96]. После иммунопреципитации антителом против TTR и диссоциации тетрамерной структуры TTR (на проамилоидогенные мономеры) сывороточный вариант белка TTR можно обнаружить с помощью масс-спектрометрии [9].7,98,99,100]. Приблизительно 90% вариантов TTR идентифицируются этим методом, и они демонстрируют сдвиг массы, предсказанный заменой одной аминокислоты варианта TTR [57, 97, 101] (рис. 4).
Неврологическое обследование
На основании имеющихся признаков и симптомов пациенты должны пройти полное неврологическое обследование для выявления, характеристики и оценки тяжести невропатических нарушений, затрагивающих мелкие и крупные нервные волокна [1, 82]. Шкалы, используемые для оценки невропатии, а также локальные варианты и шкалы, которые количественно оценивают неврологическую функцию у пациентов с диабетической полинейропатией, но полезны для пациентов с ATTR-FAP, также должны использоваться для оценки нейропатических симптомов [1]. Точно так же скорость нервной проводимости, сенсорные потенциалы действия и другие тесты для характеристики тонких волокон (обнаружение холода и тепла) и крупных волокон (обнаружение вибрации) периферических сенсорных порогов должны использоваться для оценки прогрессирования ATTR-FAP [1] (рис. 4).
Шкалы, используемые для оценки невропатии, а также локальные варианты и шкалы, которые количественно оценивают неврологическую функцию у пациентов с диабетической полинейропатией, но полезны для пациентов с ATTR-FAP, также должны использоваться для оценки нейропатических симптомов [1]. Точно так же скорость нервной проводимости, сенсорные потенциалы действия и другие тесты для характеристики тонких волокон (обнаружение холода и тепла) и крупных волокон (обнаружение вибрации) периферических сенсорных порогов должны использоваться для оценки прогрессирования ATTR-FAP [1] (рис. 4).
После постановки диагноза и оценки неврологической симптоматики следует определить системное распространение болезни путем оценки состояния сердца, глаз, почек и т. д. [1, 82].
Кардиологическое обследование
Кардиологическое исследование необходимо проводить для выявления инфильтративной кардиомиопатии и серьезных нарушений проводимости, несущих риск внезапной смерти [1] (рис. 4).
Офтальмологическое обследование
Офтальмологическое обследование необходимо для выявления возможных глазных проявлений, таких как сухой кератоконъюнктивит, вторичная глаукома, помутнение стекловидного тела или аномалии зрачка [69, 102] (рис. 4).
4).
Оценка функции почек
В связи с возможной микроальбуминурией и/или легкой азотемией и последующей почечной недостаточностью у пациентов с ATTR-FAP рекомендуется мониторинг параметров протеинурии и нарушений функции почек (клиренс креатинина и альбуминурия) [70, 82, 103] .
Распространенные диагностические ошибки
Хотя сенсорно-моторная полинейропатия, зависящая от длины тела, является отличительной чертой ATTR-FAP, она не является отличительной чертой этого состояния и может присутствовать при более распространенных неврологических состояниях, потенциально приводя к ошибочным диагнозам [82, 9].2].
ХВДП
ХВДП, характеризующийся демиелинизирующей сенсорно-моторной нейропатией, является наиболее частым невропатически ошибочным диагнозом спорадического ATTR-FAP. В одном исследовании у 53% из 15 японских пациентов со спорадическим ATTR-FAP Val30Met первоначально был ошибочно диагностирован ХВДП [31, 34]. Электрофизиологические характеристики ATTR-FAP могут напоминать характеристики CIDP; однако симптомы вегетативной дисфункции отсутствуют [30, 31]. Уровни белка в спинномозговой жидкости повышены в большей степени, чем при ATTR-FAP [30, 9].2]. Кроме того, биопсия нерва, выявляющая конгофильные отложения, позволяет дифференцировать ATTR-FAP от CIDP [1]. ATTR-FAP следует подозревать у пациентов с диагнозом CIDP, которые не реагируют на иммуномодулирующее лечение, если они связаны с неуклонным прогрессированием невропатии, аксональным паттерном и дизавтономией [30, 31, 46, 92].
Уровни белка в спинномозговой жидкости повышены в большей степени, чем при ATTR-FAP [30, 9].2]. Кроме того, биопсия нерва, выявляющая конгофильные отложения, позволяет дифференцировать ATTR-FAP от CIDP [1]. ATTR-FAP следует подозревать у пациентов с диагнозом CIDP, которые не реагируют на иммуномодулирующее лечение, если они связаны с неуклонным прогрессированием невропатии, аксональным паттерном и дизавтономией [30, 31, 46, 92].
AL-амилоидоз
ATTR-амилоидоз часто неправильно диагностировали как AL-амилоидоз из-за высокой частоты моноклональной гаммапатии у пожилых пациентов или ложного иммуномечения амилоидных отложений. Однако этого ошибочного диагноза можно избежать путем тщательного типирования белка-предшественника амилоида и генетического тестирования [1, 30, 9].1,92,93].
Другие распространенные ошибочные диагнозы включают идиопатическую аксональную полиневропатию, другие типы наследственной сенсорной полиневропатии, наследственные сенсорные и вегетативные невропатии, болезнь Фабри, прокаженную невропатию, невропатию, имитирующую диабет или хронический алкоголизм, невропатию Шарко-Мари-Тута или болезнь двигательных нейронов, поясничный отдел спинальный стеноз, беспокойство и дефицит витамина B12 [1, 18, 104].
Управление
Управление ATTR-FAP включает три основных этапа [82]:
В отличие от европейских стран, которые приняли варианты фармакотерапевтического лечения ATTR-FAP, в Японии ТП остается терапией первой линии [42, 106]. Специфический для Японии алгоритм лечения ATTR-FAP [107,108,109], разработанная на заседании медицинского консультативного совета в Токио, предполагает, что пациентов с ATTR-FAP в Японии следует первоначально обследовать на предмет наличия показаний к ТП. Пациентам, не отвечающим этим показаниям, следует назначать тафамидис. При наличии показаний пациентов следует дополнительно обследовать на наличие факторов риска сердечной дисфункции после ТП. Пациенты без факторов риска должны пройти ТП и получать тафамидис до ТП. Пациентам с факторами риска может быть назначена либо ТП (тафамидис может быть назначен до трансплантации), либо может быть назначен только тафамидис (рис. 5). Хотя продолжительность заболевания ATTR-FAP <5 лет является одним из показаний для ТП, некоторые пациенты с легкими симптомами, которые соответствуют другим критериям, могут быть рассмотрены для ТП, даже если продолжительность заболевания (от начала) превышает 5 лет [56, 110, 111].
Специфический для Японии алгоритм лечения ATTR-FAP [107,108,109], разработанная на заседании медицинского консультативного совета в Токио, предполагает, что пациентов с ATTR-FAP в Японии следует первоначально обследовать на предмет наличия показаний к ТП. Пациентам, не отвечающим этим показаниям, следует назначать тафамидис. При наличии показаний пациентов следует дополнительно обследовать на наличие факторов риска сердечной дисфункции после ТП. Пациенты без факторов риска должны пройти ТП и получать тафамидис до ТП. Пациентам с факторами риска может быть назначена либо ТП (тафамидис может быть назначен до трансплантации), либо может быть назначен только тафамидис (рис. 5). Хотя продолжительность заболевания ATTR-FAP <5 лет является одним из показаний для ТП, некоторые пациенты с легкими симптомами, которые соответствуют другим критериям, могут быть рассмотрены для ТП, даже если продолжительность заболевания (от начала) превышает 5 лет [56, 110, 111].
Рис. 5
5 Алгоритм лечения, специфичный для ATTR-FAP Val30Met в Японии. a У большинства пациентов с ATTR-FAP с поздним началом заболевание прогрессирует даже после ТП. Однако наш опыт в Японии и литературные данные свидетельствуют о хорошем исходе после ТП у некоторых пациентов с поздним началом; в частности, женщины с поздним началом показали значительно лучшую выживаемость после ТП, чем их коллеги-мужчины ( p = 0,02, Okamoto S, et al., 2009 [108]; отношение рисков 1,57 [мужчины против женщин, p = 0,014], Ericzon BG, et al. 2015 [33]). b Даже в случаях с поздним началом ТП иногда дает хорошие результаты у женщин (Ericzon BG, et al., 2015 [33]). Исходы ТП у пациентов с невропатическим типом ATTR-FAP без Val30Met сравнительно хорошие, исходя из нашего опыта в университетской больнице Кумамото и университетской больнице Шиншу в Японии (неопубликованные наблюдения). LT трансплантация печени, ATTR-FAP транстиретиновая семейная амилоидная невропатия, Val30Met замена валина на метионин в положении 30 гена TTR
Изображение полного размера
LT
С 1990 г. LT является единственным потенциально излечивающим и модифицирующим заболевание вариантом лечения пациентов с ATTR-FAP [1, 36,37 ,38,39,40,41]. Сывороточный TTR в основном вырабатывается в печени, а LT устраняет первичный источник мутантного TTR, элиминирует примерно 95% вариантов TTR и может замедлять или останавливать прогрессирование заболевания [1, 112, 113, 114]. Исследование, в котором оценивались гистопатологические и биохимические характеристики амилоида абдоминального жира у пациентов, перенесших ТП более 10 лет назад, показало, что тканевые отложения амилоида у пациентов с САП могут постепенно регрессировать в течение длительного времени после ТП [112]. Результаты Всемирного регистра трансплантатов семейной амилоидотической полинейропатии (FAPWTR), инициированного в 1995 показывают отличную выживаемость пациентов (общая 5-летняя выживаемость пациентов 77%, 20-летняя выживаемость 55,3%), что сравнимо с показателями выживаемости, наблюдаемыми при ТП, выполненной при других хронических заболеваниях печени [33, 115].
LT является единственным потенциально излечивающим и модифицирующим заболевание вариантом лечения пациентов с ATTR-FAP [1, 36,37 ,38,39,40,41]. Сывороточный TTR в основном вырабатывается в печени, а LT устраняет первичный источник мутантного TTR, элиминирует примерно 95% вариантов TTR и может замедлять или останавливать прогрессирование заболевания [1, 112, 113, 114]. Исследование, в котором оценивались гистопатологические и биохимические характеристики амилоида абдоминального жира у пациентов, перенесших ТП более 10 лет назад, показало, что тканевые отложения амилоида у пациентов с САП могут постепенно регрессировать в течение длительного времени после ТП [112]. Результаты Всемирного регистра трансплантатов семейной амилоидотической полинейропатии (FAPWTR), инициированного в 1995 показывают отличную выживаемость пациентов (общая 5-летняя выживаемость пациентов 77%, 20-летняя выживаемость 55,3%), что сравнимо с показателями выживаемости, наблюдаемыми при ТП, выполненной при других хронических заболеваниях печени [33, 115]. 20-летний ретроспективный анализ, проведенный FAPWTR, также показал, что раннее начало заболевания, короткая продолжительность заболевания и мутация Val30Met в значительной степени связаны со снижением смертности у пациентов с ТП ( p < 0,001), в то время как пол не влияет на увеличение выживаемости для пациенты с ранним началом ТП ( p = 0,442) [33]. Исследование 80 последовательных пациентов с ATTR-FAP Val30Met, которые посетили больницу Университета Кумамото в период с января 1990 г. по декабрь 2010 г., показало, что японские пациенты, перенесшие ТП, имеют более длительную выживаемость ( p < 0,001) и более высокую (100% против 56,1%) расчетную вероятность выживаемость через 10 лет после начала САП [116]. При раннем начале заболевания у перенесших трансплантацию пациентов наблюдается значительное ( p < 0,001) улучшение выживаемости по сравнению со случаями без трансплантации. Однако при позднем начале заболевания выживаемость пациентов с трансплантацией не отличается от таковой у пациентов без трансплантации [108].
20-летний ретроспективный анализ, проведенный FAPWTR, также показал, что раннее начало заболевания, короткая продолжительность заболевания и мутация Val30Met в значительной степени связаны со снижением смертности у пациентов с ТП ( p < 0,001), в то время как пол не влияет на увеличение выживаемости для пациенты с ранним началом ТП ( p = 0,442) [33]. Исследование 80 последовательных пациентов с ATTR-FAP Val30Met, которые посетили больницу Университета Кумамото в период с января 1990 г. по декабрь 2010 г., показало, что японские пациенты, перенесшие ТП, имеют более длительную выживаемость ( p < 0,001) и более высокую (100% против 56,1%) расчетную вероятность выживаемость через 10 лет после начала САП [116]. При раннем начале заболевания у перенесших трансплантацию пациентов наблюдается значительное ( p < 0,001) улучшение выживаемости по сравнению со случаями без трансплантации. Однако при позднем начале заболевания выживаемость пациентов с трансплантацией не отличается от таковой у пациентов без трансплантации [108]. Кроме того, в то время как в случаях с ранним началом не было выявлено существенной разницы в выживаемости после ТП между пациентами мужского и женского пола, у пациентов с поздним началом заболевания у женщин, перенесших трансплантацию, была значительная (9).7188 p = 0,02) улучшили выживаемость по сравнению с случаями трансплантации у мужчин [108]. Следует также отметить, что 10-летняя выживаемость после ТП была численно (но не достоверно) выше у пациентов, перенесших трансплантат печени от живого донора, чем у тех, кто получил трансплантат от умершего донора (72,3% против 33,8%, p ). = 0,092) [117]. Другое исследование 45 пациентов с симптоматическим ATTR-FAP показало общую 1- и 5-летнюю выживаемость 82% и 60% соответственно, заметное снижение уровней циркулирующих мутированных TTR (2,5% от значений до ТП) и заметное более низкая скорость дегенерации аксонов (0,9/мм 91 121 2 91 122 vs 70/мм 91 121 2 91 122 эндоневральной области/месяц у трансплантированных и нетрансплантированных пациентов) после ТП; Рекомендована ТП при появлении первых симптомов и исключении пациентов с оценкой по шкале Норриса <55 и/или с недержанием мочи [118].
Кроме того, в то время как в случаях с ранним началом не было выявлено существенной разницы в выживаемости после ТП между пациентами мужского и женского пола, у пациентов с поздним началом заболевания у женщин, перенесших трансплантацию, была значительная (9).7188 p = 0,02) улучшили выживаемость по сравнению с случаями трансплантации у мужчин [108]. Следует также отметить, что 10-летняя выживаемость после ТП была численно (но не достоверно) выше у пациентов, перенесших трансплантат печени от живого донора, чем у тех, кто получил трансплантат от умершего донора (72,3% против 33,8%, p ). = 0,092) [117]. Другое исследование 45 пациентов с симптоматическим ATTR-FAP показало общую 1- и 5-летнюю выживаемость 82% и 60% соответственно, заметное снижение уровней циркулирующих мутированных TTR (2,5% от значений до ТП) и заметное более низкая скорость дегенерации аксонов (0,9/мм 91 121 2 91 122 vs 70/мм 91 121 2 91 122 эндоневральной области/месяц у трансплантированных и нетрансплантированных пациентов) после ТП; Рекомендована ТП при появлении первых симптомов и исключении пациентов с оценкой по шкале Норриса <55 и/или с недержанием мочи [118]. Долгосрочную выживаемость после ТП можно предсказать путем расчета 5-летнего риска смерти по шкале полинейропатии, инвалидности (PND), наличию или отсутствию ортостатической гипотензии, функциональному классу Нью-Йоркской кардиологической ассоциации (NYHA), продолжительности QRS и межжелудочковой перегородке. толщина [119].
Долгосрочную выживаемость после ТП можно предсказать путем расчета 5-летнего риска смерти по шкале полинейропатии, инвалидности (PND), наличию или отсутствию ортостатической гипотензии, функциональному классу Нью-Йоркской кардиологической ассоциации (NYHA), продолжительности QRS и межжелудочковой перегородке. толщина [119].
Следует отметить, что ситуация с использованием LT для ATTR-FAP в Японии отличается от ситуации в других регионах мира. Ткань печени от живых доноров используется для ТП в Японии, в то время как ткань трупной печени используется в других странах [1]. Следовательно, лучшие результаты лечения ТП, включая более высокие показатели выживаемости после ТП, достигаются в Японии [116]. Таким образом, несмотря на использование недавно одобренной терапии тафамидисом, который является вариантом лечения первой линии для пациентов с ранней стадией ATTR-FAP в Европе [42], ТП остается вариантом лечения первой линии в Японии, особенно для ранних стадий. начало ATTR-FAP Val30Met [106].
Несмотря на то, что LT является стандартной терапевтической стратегией для ATTR-FAP, у нее есть несколько ограничений [113]. Органные нарушения, возникшие до ТП, не обращаются [1]. Как видно из FAPWTR, исходы ТП зависят от мутации (10-летняя выживаемость составляет 74% для пациентов с Val30Met по сравнению с 44% для пациентов без Val30Met; 20-летняя смертность у пациентов с Val30Met составляет 61% по сравнению с пациентами без Val30Met). больных, p < 0,001) [1, 33]. Кроме того, у некоторых пациентов прогрессирование заболевания происходит даже после ТП [62, 120]. Например, прогрессирование кардиальной амилоидной инфильтрации продолжается после ТП, поскольку TTR дикого типа продолжает откладываться на существующих отложениях амилоида [121, 122, 123, 124]. Точно так же глазные и лептоменингеальные отложения продолжают увеличиваться после ТП из-за локального, мутантного синтеза TTR в эпителии сетчатки и сосудистых сплетениях [61, 62, 113, 125, 126, 127, 128, 129].]. Следовательно, хотя вегетативные расстройства уменьшаются после ТП, нервная функция редко улучшается [1]. Также, помимо хирургических рисков, у этих пациентов требуется длительная пост-ТП иммуносупрессивная терапия [1]. Кроме того, многие пациенты не являются подходящими кандидатами для ТП, в то время как у многих других ТП труднодоступна [82, 130]. Кроме того, нельзя недооценивать риск приобретенного системного TTR-амилоидоза у пациентов, получающих домино ЛТ [131].
Также, помимо хирургических рисков, у этих пациентов требуется длительная пост-ТП иммуносупрессивная терапия [1]. Кроме того, многие пациенты не являются подходящими кандидатами для ТП, в то время как у многих других ТП труднодоступна [82, 130]. Кроме того, нельзя недооценивать риск приобретенного системного TTR-амилоидоза у пациентов, получающих домино ЛТ [131].
Фармакотерапия
Поскольку дестабилизация тетрамера TTR наряду с неправильным сворачиванием и образованием фибрилл вносит свой вклад в его проамилоидогенный потенциал, стабилизация тетрамера TTR была определена как шаг, ограничивающий скорость, и несколько новых фармакологических методов лечения, таких как агенты, стабилизирующие TTR, были оценены для лечения АТТР-ФАП. Их можно назначать на ранней стадии заболевания в ожидании ТП или потенциально отсрочить необходимость ТП [1].
Тафамидис
Тафамидис (Vyndaqel®; Pfizer Inc.), одобренный в Европе в 2011 г. [42] и в Японии в 2013 г., является единственным рецептурным препаратом для ATTR-FAP [132]. В дополнение к улучшенным диагностическим методам доступность тафамидиса способствовала более ранней диагностике случаев из неэндемичных районов, поскольку это ознаменовало превращение ATTR-FAP из неконтролируемого состояния в излечимое заболевание. Тафамидис, модифицирующий болезнь агент, кинетически стабилизирует мутантные тетрамеры TTR и предотвращает их диссоциацию на мономеры, что является критическим, ограничивающим скорость этапом образования фибрилл и амилоидогенеза [1, 133, 134, 135]. В рандомизированном двойном слепом исследовании, в котором пациенты с ATTR-FAP на ранней стадии получали тафамидис меглумин 20 мг (тафамидис 12,2 мг) один раз в день или плацебо в течение 18 месяцев, хотя между группами тафамидиса и плацебо не наблюдалось различий в отношении нарушения нейропатии. Оценка – анализ респондентов нижних конечностей (NIS-LL) (45,3% против 290,5% респондентов; p = 0,068) и изменение общего балла Norfolk Quality of Life Diabetic Neuropathic (TQOL; 2,0 против 7,2; p = 0,116) в популяции, намеревающейся лечиться ( n = 125), значительно большая доля (60,0% против 38,1%; p < 0,041) пациентов, получавших тафамидис, были ответчиками NIS-LL, а пациенты, получавшие тафамидис, имели лучшее сохранение качества жизни (0,1 против 8,9; p = 0,045) в популяции, оцениваемой по эффективности ( n = 87).
В дополнение к улучшенным диагностическим методам доступность тафамидиса способствовала более ранней диагностике случаев из неэндемичных районов, поскольку это ознаменовало превращение ATTR-FAP из неконтролируемого состояния в излечимое заболевание. Тафамидис, модифицирующий болезнь агент, кинетически стабилизирует мутантные тетрамеры TTR и предотвращает их диссоциацию на мономеры, что является критическим, ограничивающим скорость этапом образования фибрилл и амилоидогенеза [1, 133, 134, 135]. В рандомизированном двойном слепом исследовании, в котором пациенты с ATTR-FAP на ранней стадии получали тафамидис меглумин 20 мг (тафамидис 12,2 мг) один раз в день или плацебо в течение 18 месяцев, хотя между группами тафамидиса и плацебо не наблюдалось различий в отношении нарушения нейропатии. Оценка – анализ респондентов нижних конечностей (NIS-LL) (45,3% против 290,5% респондентов; p = 0,068) и изменение общего балла Norfolk Quality of Life Diabetic Neuropathic (TQOL; 2,0 против 7,2; p = 0,116) в популяции, намеревающейся лечиться ( n = 125), значительно большая доля (60,0% против 38,1%; p < 0,041) пациентов, получавших тафамидис, были ответчиками NIS-LL, а пациенты, получавшие тафамидис, имели лучшее сохранение качества жизни (0,1 против 8,9; p = 0,045) в популяции, оцениваемой по эффективности ( n = 87). Кроме того, у пациентов, принимавших тафамидис, TQOL сохранялось лучше (0,1 против 8,9).; p < 0,045) и продемонстрировали на 52% меньше неврологических нарушений с нежелательными явлениями (НЯ) по сравнению с пациентами, получавшими плацебо [32]. Еще одно 12-месячное открытое расширенное исследование, в котором оценивалась долгосрочная безопасность, переносимость и эффективность тафамидиса в дозе 20 мг один раз в день у 86 пациентов, показало снижение частоты неврологического ухудшения у пациентов, получавших тафамидис в течение 30 месяцев. Кроме того, у пациентов, получавших лечение в течение 30 месяцев, сохранение неврологической функции было на 55,9 % выше (по данным NIS-LL), чем у тех, у кого тафамидис был начат позже, что свидетельствует о том, что раннее начало тафамидиса необходимо для замедления прогрессирования заболевания. Инфекция мочевыводящих путей, диарея, термический ожог и назофарингит были одними из наиболее часто наблюдаемых нежелательных явлений в группе тафамидиса.
Кроме того, у пациентов, принимавших тафамидис, TQOL сохранялось лучше (0,1 против 8,9).; p < 0,045) и продемонстрировали на 52% меньше неврологических нарушений с нежелательными явлениями (НЯ) по сравнению с пациентами, получавшими плацебо [32]. Еще одно 12-месячное открытое расширенное исследование, в котором оценивалась долгосрочная безопасность, переносимость и эффективность тафамидиса в дозе 20 мг один раз в день у 86 пациентов, показало снижение частоты неврологического ухудшения у пациентов, получавших тафамидис в течение 30 месяцев. Кроме того, у пациентов, получавших лечение в течение 30 месяцев, сохранение неврологической функции было на 55,9 % выше (по данным NIS-LL), чем у тех, у кого тафамидис был начат позже, что свидетельствует о том, что раннее начало тафамидиса необходимо для замедления прогрессирования заболевания. Инфекция мочевыводящих путей, диарея, термический ожог и назофарингит были одними из наиболее часто наблюдаемых нежелательных явлений в группе тафамидиса. Однако новых проблем с безопасностью или переносимостью выявлено не было, а общая частота НЯ и серьезных НЯ была одинаковой в группах тафамиди и плацебо [42, 136]. Кроме того, продолжающееся долгосрочное открытое расширенное исследование показало, что раннее лечение тафамидисом на срок до 5,5 лет устойчиво замедляло неврологическую прогрессию и сохраняло нутриционный статус (средние изменения по сравнению с исходным уровнем: NIS-LL, 5,3 балла; mBMI, -7,8 балла). кг/м 2 × г/л), без каких-либо новых опасений по поводу безопасности [137].
Однако новых проблем с безопасностью или переносимостью выявлено не было, а общая частота НЯ и серьезных НЯ была одинаковой в группах тафамиди и плацебо [42, 136]. Кроме того, продолжающееся долгосрочное открытое расширенное исследование показало, что раннее лечение тафамидисом на срок до 5,5 лет устойчиво замедляло неврологическую прогрессию и сохраняло нутриционный статус (средние изменения по сравнению с исходным уровнем: NIS-LL, 5,3 балла; mBMI, -7,8 балла). кг/м 2 × г/л), без каких-либо новых опасений по поводу безопасности [137].
В Японии оценивали эффективность и безопасность тафамидиса меглумина в дозе 20 мг (тафамидис 12,2 мг) один раз в день у пациентов с ATTR-FAP ( n = 10, 70% мужчин, средний возраст 60,1 года) в течение 1,5 лет в фазе III, одногрупповое, открытое исследование [138]. Большинство из них имели мутацию Val30Met (90%) и были случаями с поздним началом (70%, средний возраст начала 65,6 лет). На 8-й неделе лечения стабилизация TTR была достигнута у всех 10 пациентов (первичная конечная точка, процент стабилизации ≥32%) и сохранялась в течение 78-й недели у 8 (80%) пациентов. Лечение тафамидисом замедляло прогрессирование нейропатии (среднее [SD] изменение NIS-LL на 78-й неделе, 3,3 [4,7]), поддерживало качество жизни (среднее [SD] изменение TQOL на 78-й неделе, 10,8 [13,7]) и улучшало состояние питания ( среднее [SD] увеличение mBMI на 78 неделе, 53,7 [81,4]) за период исследования. Назофарингит, мышечная слабость, бактериальная пневмония и термический ожог были наиболее распространенными НЯ. Два НЯ (отек десен и внезапная смерть) у двух пациентов были связаны с лечением, но прекращения лечения из-за НЯ не наблюдалось [138]. Эти результаты согласуются с предыдущими исследованиями тафамидиса [32, 136], хотя возможность обобщения ограничена из-за небольшого числа пациентов и несравнимых условий.
Лечение тафамидисом замедляло прогрессирование нейропатии (среднее [SD] изменение NIS-LL на 78-й неделе, 3,3 [4,7]), поддерживало качество жизни (среднее [SD] изменение TQOL на 78-й неделе, 10,8 [13,7]) и улучшало состояние питания ( среднее [SD] увеличение mBMI на 78 неделе, 53,7 [81,4]) за период исследования. Назофарингит, мышечная слабость, бактериальная пневмония и термический ожог были наиболее распространенными НЯ. Два НЯ (отек десен и внезапная смерть) у двух пациентов были связаны с лечением, но прекращения лечения из-за НЯ не наблюдалось [138]. Эти результаты согласуются с предыдущими исследованиями тафамидиса [32, 136], хотя возможность обобщения ограничена из-за небольшого числа пациентов и несравнимых условий.
Дифлунисал
Дифлюнизал, нестероидный противовоспалительный препарат (НПВП), также замедляет скорость амилоидогенеза, предотвращая диссоциацию, неправильное свертывание и неправильную сборку мутировавших тетрамеров TTR. Дифлунисал предпочтительно стабилизирует тетрамеры TTR, увеличивая барьер диссоциации тетрамера за счет связывания малых молекул и связывания с 99% незанятыми сайтами связывания L-тироксина в TTR [139, 140]. Из-за высоких концентраций в сыворотке после перорального введения дифлунизал придает кинетическую стабильность гетеротетрамерам TTR, превышающую кинетическую стабильность гомотетрамера дикого типа, и компенсирует его умеренную аффинность связывания и селективность в отношении TTR по сравнению со всеми другими белками сыворотки. Таким образом, дифлунизал является наиболее перспективным НПВП для лечения TTR-амилоидоза [140]. Дифлунизала, вводимого в дозе 250 мг два раза в день, достаточно для обеспечения кинетической стабилизации тетрамерного нативного состояния TTR и достижения кинетической стабилизации в очень сложных денатурирующих условиях. В международном рандомизированном двойном слепом плацебо-контролируемом исследовании, проведенном среди 130 пациентов с ATTR-FAP в Швеции, Италии, Японии, Англии и США с 2006 по 2012 г., прогрессирование полинейропатии (измеряемое по шкале оценки нейропатии плюс 7 нервов) тестов [ШШ+7]) было значительно меньше (ШШ+7 баллов: 8,7 [95% доверительный интервал (ДИ), 3,3–14,1] по сравнению с 25,0 [95% ДИ, 18,4–31,6]) у пациентов, получающих дифлюнизал.
Из-за высоких концентраций в сыворотке после перорального введения дифлунизал придает кинетическую стабильность гетеротетрамерам TTR, превышающую кинетическую стабильность гомотетрамера дикого типа, и компенсирует его умеренную аффинность связывания и селективность в отношении TTR по сравнению со всеми другими белками сыворотки. Таким образом, дифлунизал является наиболее перспективным НПВП для лечения TTR-амилоидоза [140]. Дифлунизала, вводимого в дозе 250 мг два раза в день, достаточно для обеспечения кинетической стабилизации тетрамерного нативного состояния TTR и достижения кинетической стабилизации в очень сложных денатурирующих условиях. В международном рандомизированном двойном слепом плацебо-контролируемом исследовании, проведенном среди 130 пациентов с ATTR-FAP в Швеции, Италии, Японии, Англии и США с 2006 по 2012 г., прогрессирование полинейропатии (измеряемое по шкале оценки нейропатии плюс 7 нервов) тестов [ШШ+7]) было значительно меньше (ШШ+7 баллов: 8,7 [95% доверительный интервал (ДИ), 3,3–14,1] по сравнению с 25,0 [95% ДИ, 18,4–31,6]) у пациентов, получающих дифлюнизал. Кроме того, у пациентов, принимавших дифлюнизал, наблюдалось значительное улучшение показателей качества жизни по сравнению с пациентами, принимавшими плацебо, у которых качество жизни ухудшилось. Кроме того, большая часть пациентов, получавших дифлюнизал (29,7% против 9,4%), демонстрировала неврологическую стабильность через 2 года (увеличение <2 баллов по шкале NIS+7; p = 0,007) [141]. Ретроспективный анализ применения дифлунизала не по прямому назначению у пациентов с ATTR-FAP показал прекращение лечения у 57% пациентов из-за побочных эффектов со стороны желудочно-кишечного тракта [142].
Кроме того, у пациентов, принимавших дифлюнизал, наблюдалось значительное улучшение показателей качества жизни по сравнению с пациентами, принимавшими плацебо, у которых качество жизни ухудшилось. Кроме того, большая часть пациентов, получавших дифлюнизал (29,7% против 9,4%), демонстрировала неврологическую стабильность через 2 года (увеличение <2 баллов по шкале NIS+7; p = 0,007) [141]. Ретроспективный анализ применения дифлунизала не по прямому назначению у пациентов с ATTR-FAP показал прекращение лечения у 57% пациентов из-за побочных эффектов со стороны желудочно-кишечного тракта [142].
Противопоказание для применения НПВП у пациентов с тяжелой застойной сердечной недостаточностью (класс IV по NYHA) или почечной недостаточностью (оценочный клиренс креатинина <30 мл/мин) может ограничивать их использование у пациентов с ATTR-FAP с поражением сердца или почек [106, 141, 143]. Хотя частота сердечно-сосудистых или почечных осложнений была одинаковой в группах дифлюнизала и плацебо в исследовании фазы III, два пациента в группе дифлунизала прекратили лечение из-за желудочно-кишечного кровотечения и застойной сердечной недостаточности соответственно [141]. Из-за риска желудочно-кишечного кровотечения, нарушения функции почек или задержки жидкости может потребоваться отбор пациентов, управление противовоспалительными препаратами и долгосрочное наблюдение за НЯ [1, 139]., 144].
Из-за риска желудочно-кишечного кровотечения, нарушения функции почек или задержки жидкости может потребоваться отбор пациентов, управление противовоспалительными препаратами и долгосрочное наблюдение за НЯ [1, 139]., 144].
Симптоматическая терапия
Непосредственной целью лечения ATTR-FAP является облегчение симптомов; поэтому симптоматическое лечение сенсорно-моторной невропатии и вегетативной дисфункции следует начинать сразу же после установления диагноза, независимо от имеющихся симптомов [1]. Симптоматическое лечение включает профилактическую имплантацию электрокардиостимулятора для уменьшения серьезных сердечных событий; лекарства для лечения кардиомиопатии, боли, диареи, ортостатической гипотензии, недержания мочи, гипотиреоза и сердечной недостаточности; эритропоэтин или железо при анемии; CTS-релиз операции; гемодиализ при почечной недостаточности; и витрэктомия или трабекулэктомия при глазном амилоидозе [1, 82, 145]. В 45-месячном исследовании профилактическая имплантация электрокардиостимулятора уменьшала выраженность серьезных сердечных событий у пациентов с полинейропатией и нарушениями проводимости [146]. Аналогично, у пожилых пациентов с ATTR-FAP и кардиомиопатией стабилизация водного баланса с целью снижения давления наполнения была достигнута с помощью очень низких доз петлевых диуретиков [106, 147].
Аналогично, у пожилых пациентов с ATTR-FAP и кардиомиопатией стабилизация водного баланса с целью снижения давления наполнения была достигнута с помощью очень низких доз петлевых диуретиков [106, 147].
Генетическое консультирование
Учитывая, что генетическое тестирование является основным инструментом диагностики и помогает выявить носительство в условиях генетического консультирования, родственникам следует настоятельно рекомендовать пройти генетическое тестирование и биопсию тканей (в случаях генопозитивности TTR) [1]. , 34]. Однако, поскольку генетическое тестирование у пациентов с семейным анамнезом ATTR-FAP может привести к серьезному беспокойству, необходимо генетическое консультирование и психологическая поддержка пациентов и членов их семей [1, 34]. Прогностическое генетическое тестирование следует проводить у взрослых (в возрасте ≥20 лет) родственников пациентов с ATTR-FAP, как только они смогут понять медицинские, социальные и психологические последствия положительного генетического теста [1]. Также при генетическом консультировании лица с положительным результатом должны быть осведомлены о вариабельной пенетрантности заболевания и различиях в возрасте появления симптомов [24, 148, 149].].
Также при генетическом консультировании лица с положительным результатом должны быть осведомлены о вариабельной пенетрантности заболевания и различиях в возрасте появления симптомов [24, 148, 149].].
Поддерживающая терапия
Поскольку ведение ATTR-FAP чрезвычайно сложно, важно предоставить пациентам и их семьям всю возможную социальную и моральную поддержку. Необходимо активизировать усилия по раннему выявлению и диагностике. Следует немедленно начать симптоматическое лечение и разработать долгосрочную стратегию. FAPWTR [150] был создан для сотрудничества и обмена опытом, мониторинга международной деятельности по трансплантации и оптимизации отбора пациентов, чтобы обеспечить удовлетворительное последующее наблюдение после трансплантации и служить исследовательским инструментом для лечебных центров. Также должны быть созданы другие сети и центры передового опыта для конкретных стран и регионов для обмена клиническими, патологическими и генетическими данными, а также для обмена опытом и передовыми методами лечения [82].
Новые методы лечения
Ряд экспериментальных фармакологических методов лечения ATTR-FAP находится в разработке. Терапевтические средства на основе антисмысловых олигонуклеотидов и РНК-интерференции представляют собой две разные методологии, направленные на снижение общего производства TTR [106]. ISIS-TTR Rx представляет собой терапию на основе антисмысловых олигонуклеотидов, которая вызывает разрушение транскриптов TTR дикого типа и мутантных. В течение 12 недель лечения лечение ISIS-TTR Rx снижало уровни мРНК печеночного TTR и белка TTR в сыворотке на 80% в моделях на мышах и приматах, отличных от человека [151, 152]. Patisiran (ALN-TTR02) использует малые интерферирующие РНК, нацеленные на TTR, для снижения TTR дикого типа и мутантного типа. В фазе II открытого многодозового исследования с повышением дозы с участием 29у пациентов с h-ATTRm амилоидозом I или II стадии с полинейропатией патисиран в дозе 0,3 мг/кг каждые 3 недели приводил к максимальному среднему снижению уровня TTR на 87%; максимум 96% был достигнут у одного пациента [153]. Аналогичным образом, ревусиран (ALN-TTRsc), вводимая подкожно и нацеленная на TTR миРНК, конъюгированная с трехантенной, снижала экспрессию белка TTR примерно на 80% в моделях приматов, отличных от человека, при дозах всего 2,5 мг/кг [154].
Аналогичным образом, ревусиран (ALN-TTRsc), вводимая подкожно и нацеленная на TTR миРНК, конъюгированная с трехантенной, снижала экспрессию белка TTR примерно на 80% в моделях приматов, отличных от человека, при дозах всего 2,5 мг/кг [154].
Синергическая комбинация доксициклина (разрушитель фибрилл TTR in vitro) и тауроурсодезоксихолевой кислоты (TUDCA; билиарная кислота, действующая как мощный антиапоптоз и антиоксидант) продемонстрировала удаление амилоидных отложений на мышиных моделях [155] и клинические испытания (NCT01855360, NCT01171859) стремятся воспроизвести эти результаты у пациентов. Наконец, эндогенные и экзогенные моноклональные антитела могут быть использованы для нацеливания на отложения амилоида [106, 156]. Гуманизированное антиамилоидное моноклональное антитело NEOD001 и комбинация сывороточного амилоидного P-деплетера (GSK2315698) и антисывороточного моноклонального антитела к амилоидному P (GSK23) тестируются у пациентов с различными формами амилоидоза (NCT01707264, NCT01777243).
Выводы
Фенотипическая и генетическая гетерогенность может задержать диагностику ATTR-FAP в Японии. Предложенные здесь кластеры симптомов красного флага, специфичные для Японии, могут упростить диагностику для врачей и предотвратить ошибочный диагноз или отсроченный диагноз ATTR-FAP. Точно так же наш основанный на консенсусе алгоритм лечения ATTR-FAP, который также был основан на результатах лечения, наблюдаемых в Японии, может направлять клиницистов в отношении правильного и разумного использования доступных методов лечения.
История изменений
Сокращения
Ссылки
"> Ando Y, Coelho T, Berk JL, Cruz MW, Ericzon BG, Ikeda S, Lewis WD, Obici L, Planté-Bordeneuve V, Rapezzi C, et al. Руководство по наследственному амилоидозу, связанному с транстиретином, для врачей. Orphanet J Rare Dis. 2013;8:31.
ПабМед
ПабМед Центральный
Google ученый
Jacobsson B, Collins VP, Grimelius L, Pettersson T, Sandstedt B, Carlstrom A. Иммунореактивность транстиретина в печени человека и свиньи, сосудистых сплетениях и островках поджелудочной железы. J Histochem Cytochem 1989; 37:31–7.
КАС
Google ученый
Омори Х., Андо Ю., Макита Ю., Онучи Ю., Накадзима Т., Сарайва М.Дж., Терадзаки Х., Сур О., Собуэ Г., Накамура М. и др. Общее происхождение мутации Val30Met, ответственной за амилоидогенный транстиретиновый тип семейной амилоидотической полинейропатии. J Med Genet. 2004;41:e51.
КАС
пабмед
ПабМед Центральный
Google ученый
Ihse E, Rapezzi C, Merlini G, Benson MD, Ando Y, Suhr OB, Ikeda S, Lavatelli F, Obici L, Quarta CC, et al. Амилоидные фибриллы, содержащие фрагментированный ATTR, могут быть стандартной композицией фибрилл при ATTR-амилоидозе. Амилоид. 2013;20:142–50.
КАС
пабмед
Google ученый
Koike H, Misu K, Ikeda S, Ando Y, Nakazato M, Ando E, Yamamoto M, Hattori N, Sobue G. Тип I (транстиретин Met30) семейная амилоидная полинейропатия в Японии: ранняя форма против поздней формы . Арх Нейрол. 2002;59: 1771–176.
ПабМед
Google ученый
Араки С., Маватари С., Охта М., Накадзима А., Куроива Ю. Полиневритический амилоидоз в японской семье. Арх Нейрол. 1968;18:593–602.
КАС
пабмед
Google ученый
Холмгрен Г., Коста П.М., Андерссон С., Асплунд К., Стин Л., Бекман Л., Нюландер П.О., Тейшейра А., Сарайва М.Дж., Коста П.П. Географическое распределение носителей TTR met30 в северной Швеции: несоответствие между частотой носителей и коэффициентом распространенности. J Med Genet. 1994; 31: 351–4.
КАС
пабмед
ПабМед Центральный
Google ученый
Капеллари М., Кавалларо Т., Феррарини М., Кабрини И., Тайоли Ф., Феррари С., Мерлини Г., Обичи Л., Бриани К., Фабрици Д.М. Различные проявления семейной амилоидной полинейропатии, связанной с TTR, у семнадцати пациентов. J Периферийная нервная система. 2011;16:119–29.
ПабМед
Google ученый
Койке Х., Андо Ю., Уэда М., Кавагашира Ю., Иидзима М., Фудзитаке Дж. и др. Отличительные характеристики отложений амилоида при семейной амилоидной полиневропатии транстиретина Val30Met с ранним и поздним началом. J Neurol Sci. 2009 г.;287:178–84.
КАС
пабмед
Google ученый
Хараока К., Андо Ю., Андо Э., Сандгрен О., Хирата А., Накамура М., Терадзаки Х., Тадзири Т., Таноуэ Ю., Сан Х. и др. Отложение амилоида в тканях глаза у пациентов с семейной амилоидотической полинейропатией (САП). Амилоид. 2002; 9: 183–9.
КАС
пабмед
Google ученый
Koike H, Sobue G. Диагностика семейной амилоидной полинейропатии: широкий спектр клинико-патологических признаков. Эксперт Мнение Мед Диагн. 2010;4:323–31.
КАС
пабмед
Google ученый
Adams D, Suhr OB, Hund E, Obici L, Tournev I, Campistol JM, Slama MS, Hazenberg BP, Coelho T. Первый европейский консенсус по диагностике, ведению и лечению транстиретиновой семейной амилоидной полинейропатии. Карр Опин Нейрол. 2016; 29 (Приложение 1): S14–26.
КАС
пабмед
ПабМед Центральный
Google ученый
Vital C, Vital A, Bouillot-Eimer S, Brechenmacher C, Ferrer X, Lagueny A. Амилоидная невропатия: ретроспективное исследование 35 биопсий периферических нервов. J Периферийная нервная система. 2004;9: 232–41.
ПабМед
Google ученый
Obici L, Kuks JB, Buades J, Adams D, Suhr OB, Coelho T, Kyriakides T. Рекомендации по досимптомному генетическому тестированию и лечению лиц с риском наследственного транстиретинового амилоидоза. Карр Опин Нейрол. 2016;29(Приложение 1): S27–35.
КАС
пабмед
ПабМед Центральный
Google ученый
Shimojima Y, Morita H, Kobayashi S, Takei Y, Ikeda S. Десятилетнее наблюдение за функцией периферических нервов у пациентов с семейной амилоидной полиневропатией после трансплантации печени. Дж Нейрол. 2008; 255:1220–5.
ПабМед
Google ученый
Зур О.Б., Ларссон М., Эрикзон Б.Г., Вильчек Х.Е. Выживаемость после трансплантации у пациентов с мутациями, отличными от Val30Met: выдержки из FAP World Transplant Registry. Трансплантация. 2016; 100: 373–81.
КАС
пабмед
ПабМед Центральный
Google ученый
Язаки М., Мицухаси С., Токуда Т., Каметани Ф., Такей Й.И., Кояма Дж., Каваморита А., Канно Х., Икеда С.И. Прогрессирующее отложение транстиретина дикого типа после трансплантации печени преимущественно происходит в миокарде у пациентов с САП. Ам Джей Трансплант. 2007; 7: 235–42.
КАС
пабмед
Google ученый
Сандгрен О., Кьельгрен Д., Зур OB. Глазные проявления у реципиентов трансплантата печени с семейной амилоидной полиневропатией. Акта Офтальмол. 2008; 86: 520–4.
ПабМед
Google ученый
Коэльо Т., Майя Л.Ф., да Силва А.М., Круз М.В., Планте-Борденев В., Зур О.Б., Консейсао И., Шмидт Х.Х., Триго П., Келли Д.В. и др. Долгосрочные эффекты тафамидиса для лечения транстиретиновой семейной амилоидной полинейропатии. Дж Нейрол. 2013; 260:2802–14.
КАС
пабмед
ПабМед Центральный
Google ученый
Hellman U, Alarcon F, Lundgren HE, Suhr OB, Bonaiti-Pellié C, Planté-Bordeneuve V. Гетерогенность пенетрантности при семейной амилоидной полиневропатии, ATTR Val30Met, у населения Швеции. Амилоид. 2008; 15:181–186.
КАС
пабмед
ПабМед Центральный
Google ученый
Бенсон М.Д., Клуве-Бекерман Б., Зельденруст С.Р., Сиески А.М., Боденмиллер Д.М., Шоуолтер А.Д., Шлюп К.В. Направленное подавление амилоидогенного транстиретина антисмысловыми олигонуклеотидами. Мышечный нерв. 2006; 33: 609–18.
КАС
пабмед
Google ученый
Скачать ссылки
Благодарности
Авторы хотели бы поблагодарить доктора Лауру Обичи за ее бесценные советы, данные на заседании медицинского консультативного совета. Редакционную поддержку в виде написания медицинских текстов, составления таблиц и создания изображений с высоким разрешением на основе подробных указаний авторов, сопоставления комментариев авторов, редактирования, проверки фактов и ссылок оказали доктор медицинских наук Алина Гомес и Марибет Богуш. , доктор философии, Cactus Communications, и финансируется Pfizer Japan.
Финансирование
Помощь в редактировании этой статьи и проведение заседания медицинского консультативного совета финансировались компанией Pfizer, Япония.
Доступность данных и материалов
Совместное использование данных не применимо к этой статье, поскольку в ходе текущего исследования наборы данных не создавались и не анализировались.
Информация об авторе
Авторы и организации
Авторы
Вклады
Все названные авторы соответствуют критериям авторства Международного комитета редакторов медицинских журналов (ICMJE), несут ответственность за целостность работы в целом и дали окончательное одобрение версии, которая будет опубликовано.
Автор, ответственный за переписку
Переписка с
Юкио Андо.
Декларации этики
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
Не применимо.
Конкурирующие интересы
YS, MU, HK, SM и YA заявляют о получении вознаграждения за консультационные услуги или гонорара, оплаты проезда на встречи и предоставления письменной помощи от Pfizer Japan Inc. TI работает и владеет акциями Pfizer Japan Inc.
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья распространяется в соответствии с условиями международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение, и воспроизведение на любом носителе, при условии, что вы укажете автора(ов) оригинала и источник, предоставите ссылку на лицензию Creative Commons и укажете, были ли внесены изменения. Отказ от права Creative Commons на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
Отказ от права Creative Commons на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
Перепечатки и разрешения
Об этой статье
Эволюционные процессы в специализированном метаболизме растений на примере двух семейств трансфераз различных признаков царства растений (Weng et al., 2012). Химическое разнообразие этих натуральных продуктов обеспечивает различные метаболиты, полезные для жизни человека, в том числе соединения, связанные с ароматом, цветом, вкусом и лекарствами. Сравнительный анализ генома убедительно свидетельствует о том, что дупликации генов играют важную роль в эволюции расходящихся метаболических путей (Fani and Fondi, 2009).). Увеличение числа копий гена, возможно, привело к неразборчивому разнообразию кодируемых ферментов, что привело к синтезу новых метаболитов и обеспечению приспособленности организма, которая усиливает установление путей биосинтеза в линии растений.
 Расширение специализированного метаболизма растений наблюдалось в геноме Selaginella moellendorffii , растения, которое дивергировалось вскоре после образования сосудистых тканей в ходе эволюции растений (Banks et al., 2011). Репрезентативным примером этих расширенных семейств генов являются цитохром Р450-зависимые монооксигеназы, которые составляют 1% предсказанного протеома в Селагинелла . Геном печеночника, Marchantia polymorpha , также кодирует многие ферменты биосинтеза терпеноидов, имеющие общий изопреноидный путь, производное, называемое таксадиеном, для синтеза растительных гормонов, таких как гиббереллин (Bowman et al., 2017). У Physcomitrella patens, дитерпен ent -каурен превращается в дитерпены гиббереллинового типа, которые действуют как регуляторы дифференцировки протонемы (Hayashi et al., 2010).
Расширение специализированного метаболизма растений наблюдалось в геноме Selaginella moellendorffii , растения, которое дивергировалось вскоре после образования сосудистых тканей в ходе эволюции растений (Banks et al., 2011). Репрезентативным примером этих расширенных семейств генов являются цитохром Р450-зависимые монооксигеназы, которые составляют 1% предсказанного протеома в Селагинелла . Геном печеночника, Marchantia polymorpha , также кодирует многие ферменты биосинтеза терпеноидов, имеющие общий изопреноидный путь, производное, называемое таксадиеном, для синтеза растительных гормонов, таких как гиббереллин (Bowman et al., 2017). У Physcomitrella patens, дитерпен ent -каурен превращается в дитерпены гиббереллинового типа, которые действуют как регуляторы дифференцировки протонемы (Hayashi et al., 2010).
Виды голосеменных Taxus синтезируют уникальные дитерпеновые соединения, называемые «таксоиды», которые включают важный противораковый препарат, паклитаксел, производное, обозначенное как таксадиен (Guerra-Bubb et al. , 2012). К 1999 г. было идентифицировано более 350 таксоидов, причем эти соединения имели переменные боковые остатки в положениях C1, C2, C4, C5, C7, C9, C10, C13 и C14 основного таксадиенового скелета (Baloglu and Kingston, 1999). За исключением частичного пути биосинтеза (Croteau et al., 2006), знания о пути биосинтеза таксоидов, которые вносят вклад в химическое разнообразие в Taxus ограничен.
, 2012). К 1999 г. было идентифицировано более 350 таксоидов, причем эти соединения имели переменные боковые остатки в положениях C1, C2, C4, C5, C7, C9, C10, C13 и C14 основного таксадиенового скелета (Baloglu and Kingston, 1999). За исключением частичного пути биосинтеза (Croteau et al., 2006), знания о пути биосинтеза таксоидов, которые вносят вклад в химическое разнообразие в Taxus ограничен.
Благодаря своим точно настроенным ресурсам данных генома виды покрытосеменных растений представляют собой хорошие модельные системы для изучения молекулярных механизмов, лежащих в основе хеморазнообразия метаболитов растений (Kroymann, 2011). Например, меротерпены, в том числе производные фуранокумарина (Bourgaud et al., 2006) и производные шиконина, представляющие собой липофильный красный нафтохинон (Yazaki, 2017), представляют собой специализированные метаболиты, синтезируемые разветвленными путями метаболического пути, общего с общими путями биосинтеза фенилпропаноидов и изопреноидов. (Язаки и др., 2017). Термин «первичный метаболизм» указывает на процессы, необходимые для поддержания жизни, такие как получение энергии из глюкозы. К таким процессам относится, например, биосинтез убихинона, компонента дыхательной цепи в митохондриях. Биосинтез производных шиконина включает этапы, общие для биосинтеза убихинона. Чтобы избежать путаницы при разграничении первичного и специализированного (вторичного) метаболизма, в этой статье используется термин «общий метаболизм», а не «первичный метаболизм» для обозначения путей биосинтеза, сохраняющихся у самых разных организмов.
(Язаки и др., 2017). Термин «первичный метаболизм» указывает на процессы, необходимые для поддержания жизни, такие как получение энергии из глюкозы. К таким процессам относится, например, биосинтез убихинона, компонента дыхательной цепи в митохондриях. Биосинтез производных шиконина включает этапы, общие для биосинтеза убихинона. Чтобы избежать путаницы при разграничении первичного и специализированного (вторичного) метаболизма, в этой статье используется термин «общий метаболизм», а не «первичный метаболизм» для обозначения путей биосинтеза, сохраняющихся у самых разных организмов.
Эта перспектива фокусируется на двух семействах ферментов как примерах событий молекулярной эволюции: семействе ароматических субстратов пренилтрансфераз, которое играет ключевую роль в диверсификации фенольных смол, и BAHD (BEAT-AHCT-HCBT-DAT; инициалы репрезентативных членов) семейство ацилтрансфераз, которое отвечает за дериватизацию основного метаболита.
Эволюция
Цитрусовых Семейство генов пренилтрансфераз Среди надсемейства пренилтрансфераз, включающего ферменты элогации пренильной цепи, ароматические пренилтрансферазы представляют семейство, ответственное за пренилирование ароматических веществ. Ароматическая пренилтрансфераза Citrus limon , ClPT1, отвечает за биосинтез 8-геранилумбеллиферона, производного кумарина специализированного метаболита растений (Munakata et al., 2014). Химическое разнообразие производных кумарина значительно увеличивается за счет участия ароматических пренилтрансфераз, которые были идентифицированы во многих линиях растений в течение последнего десятилетия (Karamat et al., 2014; Munakata et al., 2014). Филогенетический анализ показал, что различные пренилтрансферазы развивались независимо в каждом семействе растений, а не развивались от общего предка в пределах семейства генов пренилтрансфераз (Munakata et al., 2016). Семейство генов пренилтрансфераз растений содержит консервативные подсемейства, ответственные за пути биосинтеза убихинона, пластохинона и витамина Е (Li, 2016).
Ароматическая пренилтрансфераза Citrus limon , ClPT1, отвечает за биосинтез 8-геранилумбеллиферона, производного кумарина специализированного метаболита растений (Munakata et al., 2014). Химическое разнообразие производных кумарина значительно увеличивается за счет участия ароматических пренилтрансфераз, которые были идентифицированы во многих линиях растений в течение последнего десятилетия (Karamat et al., 2014; Munakata et al., 2014). Филогенетический анализ показал, что различные пренилтрансферазы развивались независимо в каждом семействе растений, а не развивались от общего предка в пределах семейства генов пренилтрансфераз (Munakata et al., 2016). Семейство генов пренилтрансфераз растений содержит консервативные подсемейства, ответственные за пути биосинтеза убихинона, пластохинона и витамина Е (Li, 2016).
Филогенетический анализ ранее охарактеризованных пренилтрансфераз и пренилтрансфераз модельных видов P. patens, S. moellendorffii, Arabidopsis thaliana, Glycine max, и Lithospermum erythrorhizon (см. ниже), в дополнение к Citrus sinensis (рис. 1А). Филогенетически эти внутренние мембранные белки можно разделить на три основных подсемейства, т. е. белки, участвующие в биосинтезе витамина Е, пластохинона и убихинона (показаны желтым и серым фоном и черным треугольником соответственно на рис. 1А, с черным треугольником). развернуто на рисунке 1B). Описаны биохимические функции AtVTE2-1 (Savidge et al., 2002), AtVTE2-2 (Venkatesh et al., 2006) и OsPPT1 (Ohara et al., 2006). Как и ожидалось, исходя из их фундаментальной роли, все модельные виды растений имели один или несколько белков в каждом подсемействе. Напротив, поиск 9База данных 7188 C. sinensis выявила девять пренилтрансферазоподобных белков, образующих подсемейство Citrus , специфичное для клады витамина Е (показано красным на рис. 1А). Аналогичный результат был получен при поиске последовательностей генома Citrus clementina . Эти результаты предполагают, что видов Citrus развили уникальное расширенное подсемейство генов для специализированного метаболизма, при этом ClPT1 был охарактеризован биохимически.
ниже), в дополнение к Citrus sinensis (рис. 1А). Филогенетически эти внутренние мембранные белки можно разделить на три основных подсемейства, т. е. белки, участвующие в биосинтезе витамина Е, пластохинона и убихинона (показаны желтым и серым фоном и черным треугольником соответственно на рис. 1А, с черным треугольником). развернуто на рисунке 1B). Описаны биохимические функции AtVTE2-1 (Savidge et al., 2002), AtVTE2-2 (Venkatesh et al., 2006) и OsPPT1 (Ohara et al., 2006). Как и ожидалось, исходя из их фундаментальной роли, все модельные виды растений имели один или несколько белков в каждом подсемействе. Напротив, поиск 9База данных 7188 C. sinensis выявила девять пренилтрансферазоподобных белков, образующих подсемейство Citrus , специфичное для клады витамина Е (показано красным на рис. 1А). Аналогичный результат был получен при поиске последовательностей генома Citrus clementina . Эти результаты предполагают, что видов Citrus развили уникальное расширенное подсемейство генов для специализированного метаболизма, при этом ClPT1 был охарактеризован биохимически. Этот анализ также выявил подобное уникальное расширение подсемейства в G. max (показаны синим цветом на рис. 1А). Первая флавоноид-специфическая пренилтрансфераза SfN8DT1 из бобовых видов Sophora flavescens (Sasaki et al., 2008) относится к этой группе, что позволяет предположить, что флавоноид-пренилтрансферазы в соевых бобах были получены из фермента биосинтеза витамина Е. Все другие, обнаруженные позже флавоноидпренилтрансферазы были отнесены к этой подгруппе (Akashi et al., 2009; Yoneyama et al., 2016). Большинство этих ферментов, участвующих в специализированном метаболизме, проявляют строгую субстратную специфичность по отношению к конкретному пренилдифосфату.
Этот анализ также выявил подобное уникальное расширение подсемейства в G. max (показаны синим цветом на рис. 1А). Первая флавоноид-специфическая пренилтрансфераза SfN8DT1 из бобовых видов Sophora flavescens (Sasaki et al., 2008) относится к этой группе, что позволяет предположить, что флавоноид-пренилтрансферазы в соевых бобах были получены из фермента биосинтеза витамина Е. Все другие, обнаруженные позже флавоноидпренилтрансферазы были отнесены к этой подгруппе (Akashi et al., 2009; Yoneyama et al., 2016). Большинство этих ферментов, участвующих в специализированном метаболизме, проявляют строгую субстратную специфичность по отношению к конкретному пренилдифосфату.
Рисунок 1 . Филогенетический анализ семейства пренилтрансфераз у видов цитрусовых и Lithospermum erythrorhizon , а также у модельных растений. (A) Группировка растительных пренилтрансфераз в три основные клады: клада, представленная гомогентизат-фитилтрансферазой Arabidopsis AtVTE2-1, участвующая в биосинтезе витамина Е (обозначена «витамином Е» и желтым фоном), клада, представленная Arabidopsis AtVTE2-2 для биосинтеза пластохинона (обозначен «Пластохинон» и серый фон) и клада, представленная рисовой полипренилтрансферазой OsPPT1 для биосинтеза убихинона (обозначена «Убихинон» и сжатый черный треугольник). Биохимически охарактеризованные белки обозначены белым фоном. Белки цитрусовых и бобовых показаны красными и синими буквами соответственно, а клады, специфичные для линии, обозначены скобками того же цвета. (B) Подробная информация о филогенетическом дереве полипренилтрансфераз для убихинона на панели (A) . Белки L. erythrorhizon показаны пурпурными буквами. В скобках указаны субклады полипренилтрансфераз, участвующих в биосинтезе убихинона (подсемейство PPT), LePGT-подобные белки (подсемейство LePGT) и неклассифицированные субклады белков (неклассифицированные). Белки других организмов показаны черными буквами. Звездочка указывает на предполагаемый РРТ-подобный белок L. erythrorhizon . Филогенетическое дерево было построено с использованием метода объединения соседей MEGA7 с 1000 бутстрэп-репликатов для выравнивания белков, связанных с полипренилтрансферазой, которые были рассчитаны с помощью алгоритма MUSCLE. Номера доступа показаны рядом с названием организма.
Биохимически охарактеризованные белки обозначены белым фоном. Белки цитрусовых и бобовых показаны красными и синими буквами соответственно, а клады, специфичные для линии, обозначены скобками того же цвета. (B) Подробная информация о филогенетическом дереве полипренилтрансфераз для убихинона на панели (A) . Белки L. erythrorhizon показаны пурпурными буквами. В скобках указаны субклады полипренилтрансфераз, участвующих в биосинтезе убихинона (подсемейство PPT), LePGT-подобные белки (подсемейство LePGT) и неклассифицированные субклады белков (неклассифицированные). Белки других организмов показаны черными буквами. Звездочка указывает на предполагаемый РРТ-подобный белок L. erythrorhizon . Филогенетическое дерево было построено с использованием метода объединения соседей MEGA7 с 1000 бутстрэп-репликатов для выравнивания белков, связанных с полипренилтрансферазой, которые были рассчитаны с помощью алгоритма MUSCLE. Номера доступа показаны рядом с названием организма. Биохимически охарактеризованные белки обозначены желтым фоном. Масштабная линейка представляет 0,1 замены аминокислот на сайт. (C) Ген LePGT кодируется одним экзоном гена в L. erythrorhizon , тогда как LePPT-подобные белки кодируются генами со вставленными интронами в положениях, сходных с положениями авторизованного гена OsPPT и ближайшего гомолога табака, NtPPT-подобного гена (ген = LOC107804153). Показан первый сайт вставки интрона в кодирующую область. Масштабная линейка, 1 КБ последовательности ДНК. Синие прямоугольники представляют кодирующие экзоны.
Биохимически охарактеризованные белки обозначены желтым фоном. Масштабная линейка представляет 0,1 замены аминокислот на сайт. (C) Ген LePGT кодируется одним экзоном гена в L. erythrorhizon , тогда как LePPT-подобные белки кодируются генами со вставленными интронами в положениях, сходных с положениями авторизованного гена OsPPT и ближайшего гомолога табака, NtPPT-подобного гена (ген = LOC107804153). Показан первый сайт вставки интрона в кодирующую область. Масштабная линейка, 1 КБ последовательности ДНК. Синие прямоугольники представляют кодирующие экзоны.
Пренилтрансферазы, участвующие в общем метаболизме, проявляют широкую специфичность в отношении субстратов с разной длиной боковой цепи; они принимают различные пренилдифосфаты с разной длиной цепи (Sadre et al., 2010). Например, путь биосинтеза убихинона в рисе можно модифицировать путем введения декапренилдифосфатсинтазы, что приводит к образованию ненативного UQ10, а не нативного UQ9.(Охара и др. , 2006; Такахаши и др., 2006). Эти расширенные семейства генов и широкая субстратная специфичность пренилтрансфераз могут предоставить возможность для неофункционализации новых ферментов в истории эволюции растений.
, 2006; Такахаши и др., 2006). Эти расширенные семейства генов и широкая субстратная специфичность пренилтрансфераз могут предоставить возможность для неофункционализации новых ферментов в истории эволюции растений.
Эволюция гена геранилтрансферазы
p -гидроксибензойной кислоты для биосинтеза шиконина специфически участвует в биосинтезе шиконина (Yazaki et al., 2002). Обзор эволюционной истории PGT был получен путем оценки геномных последовательностей и транскриптомов L. erythrorhizon из наборов данных GenBank SRP108575 и SRP141330 соответственно, а также путем повторной сборки наших исходных данных (Takanashi et al., 2019). Было обнаружено, что гипотетические PGT-подобные белки тесно связаны с подсемейством убихинонпренилтрансфераз, участвующих в общем метаболизме (пурпурный цвет на рисунке 1B), который был ближе к этим гипотетическим PGT-подобным белкам, чем специализированные цитрусовые пренилтрансферазы (рисунок 1A). Большинство PGT-подобных белков кодируются генами с одним экзоном, тогда как общие полипренилтрансферазы биосинтеза убихинона (PPT) кодируются генами, содержащими несколько экзонов (рис. 1С). Представляет интерес выяснить, как образовалась одноэкзонная структура в процессе эволюции специализированного метаболизма растений.
1С). Представляет интерес выяснить, как образовалась одноэкзонная структура в процессе эволюции специализированного метаболизма растений. Отсутствует убихинонпренилтрансфераза у
L. erythrorhizon Хотя убихинон является общим метаболитом у всех эукариот, а гены, кодирующие PPT, необходимы для выживания широкого круга организмов, ортологичный ген убихинона PPT не был обнаружен у Транскриптом L. erythrorhizon . Эксперименты на дрожжах показали, что LePGT не может синтезировать убихинон (Yazaki et al., 2002), а LePGT, гетерологически экспрессируемый в E. coli , ингибирует биосинтез убихинона (Wu et al., 2015). Геномное секвенирование выявило фрагмент контига, который может кодировать PPT-подобные белки (звездочка на рисунке 1B), и что его аминокислотная последовательность была умеренно сходной с последовательностью OsPPT1, которая отвечает за биосинтез убихинона в рисе. Кроме того, было три контига, которые мы не смогли классифицировать и которые помечены как «неклассифицированные гены» («неклассифицированные» на рис. 1В). В отличие от конкретного PGT, который катализирует биосинтез шиконина, в гипотетическом гене была обнаружена вставка интрона в том же положении, что и в PGT Nicotiana tabacum и Oryza sativa (рис. 1C). Такая консервативная экзон-интронная организация также наблюдалась в генах РРТ арабидопсиса и риса (Ohara et al., 2006). Этот продукт гена является сильным кандидатом на роль убихинонпренилтрансферазы L. erythrorhizon , и его биохимическая характеристика ожидается в будущем.
1В). В отличие от конкретного PGT, который катализирует биосинтез шиконина, в гипотетическом гене была обнаружена вставка интрона в том же положении, что и в PGT Nicotiana tabacum и Oryza sativa (рис. 1C). Такая консервативная экзон-интронная организация также наблюдалась в генах РРТ арабидопсиса и риса (Ohara et al., 2006). Этот продукт гена является сильным кандидатом на роль убихинонпренилтрансферазы L. erythrorhizon , и его биохимическая характеристика ожидается в будущем.
Эволюция семейства генов
Taxus Acyltransferase Ацилтрансферазы также вносят существенный вклад в диверсификацию специализированных метаболитов, представителями которых являются BAHD и SCPL (подобные серинкарбоксипептидазе). Таксоиды, такие как паклитаксел, присутствуют в видов Taxus представляют собой специализированные метаболиты и высокоацилированные соединения. Пять известных таксоидных ацилтрансфераз тесно связаны друг с другом, и все они сгруппированы в кладе V семейства ацилтрансфераз BAHD (D'Auria, 2006). Эти белки Taxus различаются субстратной специфичностью как для доноров, так и для акцепторов ацила; т. е. они могут использовать ацетил-КоА, бензоил-КоА или фенилаланоил-КоА для O - и N -ацилирования различных молекул таксоидов (D'Auria, 2006).
Эти белки Taxus различаются субстратной специфичностью как для доноров, так и для акцепторов ацила; т. е. они могут использовать ацетил-КоА, бензоил-КоА или фенилаланоил-КоА для O - и N -ацилирования различных молекул таксоидов (D'Auria, 2006).
Чтобы понять эволюционное развитие семейства ацилтрансфераз Taxus BAHD, был проведен подробный филогенетический анализ клады V BAHD (желтый фон на рисунке 2A). Аминокислотные последовательности членов Taxus BAHD были получены из данных транскриптома культивируемых клеток Taxus x media (Yukimune et al., 1996). Филогенетический анализ показал, что белки Taxus BAHD образуют Taxus -специфическую кладу (красная скобка на рисунке 2A), содержащую все пять охарактеризованных ацилтрансфераз (белый фон в Taxus -специфическая клада), а также другие белки Taxus с неизвестной функцией (звездочка на рисунке 2A). В этой кладе семейства BAHD O. sativa и A. thaliana образуют уникальную кладу, что позволяет предположить, что расширение подсемейства BAHD ацилтрансфераз, специфичных для линии, играет важную роль в эволюции растений (Fani and Fondi, 2009). . В дополнение к этой подгруппе, специфичной для Taxus , были идентифицированы другие белки BAHD Taxus , которые были классифицированы с другими членами модельных растений BAHD (дополнительный рисунок S1), что позволяет предположить, что видов Taxus обладают генами, кодирующими общие белки клады V BAHD, которые консервативны среди широкого круга видов растений.
thaliana образуют уникальную кладу, что позволяет предположить, что расширение подсемейства BAHD ацилтрансфераз, специфичных для линии, играет важную роль в эволюции растений (Fani and Fondi, 2009). . В дополнение к этой подгруппе, специфичной для Taxus , были идентифицированы другие белки BAHD Taxus , которые были классифицированы с другими членами модельных растений BAHD (дополнительный рисунок S1), что позволяет предположить, что видов Taxus обладают генами, кодирующими общие белки клады V BAHD, которые консервативны среди широкого круга видов растений.
Рисунок 2 . Филогенетический анализ белков ацилтрансферазы BAHD из видов Taxus и анализ LC-MS/MS продуктов реакции неканонического фермента, таксадиенол-5-ацилтрансферазы. (A) Проведение филогенетического анализа с гипотетическими ацилтрансферазоподобными белками Taxus BAHD и родственными белками модельных видов растений. Семейство BAHD было классифицировано на пять клад (D’Auria, 2006), где клада V обозначена желтым фоном, а представители клады I–IV (Vh4MAT1, CER2, BEAT и ACT соответственно) размещены вне желтого фона. Белки Taxus , рис, Arabidopsis показаны красными, пурпурными и синими буквами соответственно, а субклады, специфичные для линии, обозначены теми же цветами. Квадратная скобка «Taxus-специфическая клада» указывает на субклад Taxus , специфичный для линии, содержащий пять охарактеризованных белков, TAT, DBAT, DBTNBT, DBBT и BAPT, обозначенных белым фоном. Звездочками обозначены белков Taxus с неизвестной функцией, а крестиками отмечены белки, биохимически проанализированные в настоящем исследовании. Представитель широко консервативной клады наземных растений с 9 в.7188 Physcomitrella от до Arabidopsis обозначены скобками, при этом четыре других субклада сжаты (расширены на дополнительном рисунке S1) в дополнение к кладе, сохранившейся в семенных растениях, содержащих специфическую кладу Taxus . Номера доступа указаны рядом с названиями организмов. Филогенетическое дерево было построено с использованием метода объединения соседей MEGA7 с 1000 бутстрэп-репликатов для выравнивания, рассчитанного с помощью алгоритма MUSCLE.
Белки Taxus , рис, Arabidopsis показаны красными, пурпурными и синими буквами соответственно, а субклады, специфичные для линии, обозначены теми же цветами. Квадратная скобка «Taxus-специфическая клада» указывает на субклад Taxus , специфичный для линии, содержащий пять охарактеризованных белков, TAT, DBAT, DBTNBT, DBBT и BAPT, обозначенных белым фоном. Звездочками обозначены белков Taxus с неизвестной функцией, а крестиками отмечены белки, биохимически проанализированные в настоящем исследовании. Представитель широко консервативной клады наземных растений с 9 в.7188 Physcomitrella от до Arabidopsis обозначены скобками, при этом четыре других субклада сжаты (расширены на дополнительном рисунке S1) в дополнение к кладе, сохранившейся в семенных растениях, содержащих специфическую кладу Taxus . Номера доступа указаны рядом с названиями организмов. Филогенетическое дерево было построено с использованием метода объединения соседей MEGA7 с 1000 бутстрэп-репликатов для выравнивания, рассчитанного с помощью алгоритма MUSCLE. Масштабная линейка, 0,1 замены аминокислот на сайт. (B) ЖХ-МС/МС хроматограммы продуктов ферментативной реакции ацилтрансфераз Taxus DBAT и TAT с использованием ацетил-КоА и 10-DAB в качестве субстратов. Красная стрелка указывает на пик неканонического продукта реакции. На нижней панели показаны хроматограммы стандартных образцов, 10-DAB и баккатина III. Хроматограммы показывают след репрезентативных ионов m/z=545,5 [M+H]+ и 604,5 [M+Nh5]+ для субстрата 10-DAB (синий) и продукта баккатина III (красный) соответственно. Вертикальная ось указывает значение относительно 5 миллионов ионов. (C) Масс-спектр пиков продуктов реакции in vitro обнаружен при времени удерживания 6,951 мин хроматограммы. Вертикальная ось указывает относительное значение количества ионов максимального сигнала при m/z=604,5. Молекулярные формулы 10-DAB и баккатина III показаны на панели (B) .
Масштабная линейка, 0,1 замены аминокислот на сайт. (B) ЖХ-МС/МС хроматограммы продуктов ферментативной реакции ацилтрансфераз Taxus DBAT и TAT с использованием ацетил-КоА и 10-DAB в качестве субстратов. Красная стрелка указывает на пик неканонического продукта реакции. На нижней панели показаны хроматограммы стандартных образцов, 10-DAB и баккатина III. Хроматограммы показывают след репрезентативных ионов m/z=545,5 [M+H]+ и 604,5 [M+Nh5]+ для субстрата 10-DAB (синий) и продукта баккатина III (красный) соответственно. Вертикальная ось указывает значение относительно 5 миллионов ионов. (C) Масс-спектр пиков продуктов реакции in vitro обнаружен при времени удерживания 6,951 мин хроматограммы. Вертикальная ось указывает относительное значение количества ионов максимального сигнала при m/z=604,5. Молекулярные формулы 10-DAB и баккатина III показаны на панели (B) .
Можно предположить, что неофункционализация индуцируется приобретением беспорядочной ферментативной активности в ходе эволюции растений. Мы исследовали ферментативную активность рекомбинантных белков, полученных из семи выделенных кДНК, кодирующих членов BAHD из Taxus -специфическое подсемейство (крестик на рис. 2А). Каждый неочищенный рекомбинантный фермент получали с использованием pET22a и OrigamiB в качестве системы вектор-хозяин (Novagen) без периплазматической сигнальной последовательности в соответствии с общепринятым методом. Каждый фермент реагировал с ацетил-КоА и 10-деацетилбаккатином III (10-DAB) в качестве субстратов, и продукты реакции анализировали с использованием системы УЭЖХ-МС/МС, оснащенной колонкой BEH C18 (Waters). Клон, кодирующий 5-гидрокситаксадиен 5- O -ацетилтрансферазу (ТАТ), имел 10-DAB:10- O -ацетилтрансферазной (DBAT) активности (Walker et al., 2000), а также канонического фермента DBAT (Рисунки 2B,C; Walker and Croteau, 2000). Количество продукта, образованного субстратом, составляло 1,4 мол.% для ТАТ и 10,4% для ДБАТ, что позволяет предположить, что активность ТАТ составляет 13,2% от активности ДБАТ.
Мы исследовали ферментативную активность рекомбинантных белков, полученных из семи выделенных кДНК, кодирующих членов BAHD из Taxus -специфическое подсемейство (крестик на рис. 2А). Каждый неочищенный рекомбинантный фермент получали с использованием pET22a и OrigamiB в качестве системы вектор-хозяин (Novagen) без периплазматической сигнальной последовательности в соответствии с общепринятым методом. Каждый фермент реагировал с ацетил-КоА и 10-деацетилбаккатином III (10-DAB) в качестве субстратов, и продукты реакции анализировали с использованием системы УЭЖХ-МС/МС, оснащенной колонкой BEH C18 (Waters). Клон, кодирующий 5-гидрокситаксадиен 5- O -ацетилтрансферазу (ТАТ), имел 10-DAB:10- O -ацетилтрансферазной (DBAT) активности (Walker et al., 2000), а также канонического фермента DBAT (Рисунки 2B,C; Walker and Croteau, 2000). Количество продукта, образованного субстратом, составляло 1,4 мол.% для ТАТ и 10,4% для ДБАТ, что позволяет предположить, что активность ТАТ составляет 13,2% от активности ДБАТ. Эта неразборчивость ферментативной активности может представлять собой эволюционный след биосинтетического фермента, который приобретает новую функциональность за счет изменения специфичности субстрата и продукта, что приводит к производству уникального специализированного метаболита.
Эта неразборчивость ферментативной активности может представлять собой эволюционный след биосинтетического фермента, который приобретает новую функциональность за счет изменения специфичности субстрата и продукта, что приводит к производству уникального специализированного метаболита.
Выводы и перспективы
На примере двух подсемейств трансфераз мы показали «наследство» экспансии семейства генов, которое имеет значение для развития специализированных метаболических путей растений. Белок в специфическом подсемействе BAHD видов Taxus проявлял беспорядочную ферментативную активность в отношении неканонических субстратов, содержащих боковые цепи в неканоническом положении углерода. Эти наблюдения соответствуют общему контексту молекулярной эволюции, объясняющей развитие и установление новой канонической ферментативной активности (Weng et al., 2012). Поколение в L. erythrorhizon подсемейства генов PGT, каждый из которых содержит один экзон и участвует в биосинтезе шиконина, предполагает предполагаемое участие обратной транскрипции зрелой мРНК. Если это предположение верно для других семейств ферментов, гены с одним экзоном могут дать ключ к идентификации отсутствующих белков, ответственных за пути биосинтеза других ценных специализированных метаболитов растений.
Если это предположение верно для других семейств ферментов, гены с одним экзоном могут дать ключ к идентификации отсутствующих белков, ответственных за пути биосинтеза других ценных специализированных метаболитов растений.
Есть еще много недостающих звеньев, даже в активно изучаемых путях биосинтеза шиконинов и таксоидов. Применимый диапазон одноэкзонной гипотезы может быть ограничен не только биосинтетическими ферментами, но и регуляторными факторами. Идентификация регуляторных факторов будет иметь важное значение для понимания продукции специализированных метаболитов растений, включая мембранные переносчики. Сравнительная геномика позволит оценить эволюционный след этих генов, например, расширение специфических подсемейств и пролиферацию генов с одним экзоном. Дальнейшие биохимические и молекулярно-генетические исследования могут предоставить экспериментальные доказательства участия гипотетических белков в специализированном метаболизме растений.
Доступность данных
Наборы данных, созданные для этого исследования, можно найти в GenBank.
Вклад авторов
HK и KY написали рукопись и выполнили филогенетический и биохимический анализы. HL участвовала в сборке геномных контигов и анализе экзон-интронной структуры генов Lithospermum erythrorhizon . HM, YK и HT были ответственны за анализ транскриптома Taxus spp.
Финансирование
Эта работа была частично поддержана Организацией по развитию новых энергетических и промышленных технологий (NEDO, № 16100890 до KY). Дополнительную поддержку оказала Исследовательская миссия RISH Киотского университета.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Дополнительный материал
Дополнительный материал к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fpls.2019.00794/full#supplementary-material
РИСУНОК S1 | Расширенное филогенетическое дерево на рисунке 2А. Филогенетический анализ с гипотетическими ацилтрансферазоподобными белками Taxus BAHD и родственными белками модельных видов растений. Звездочками отмечены белки Taxus, обнаруженные в этом исследовании. Функционально идентифицированные белки BAHD выделены желтым фоном.
Филогенетический анализ с гипотетическими ацилтрансферазоподобными белками Taxus BAHD и родственными белками модельных видов растений. Звездочками отмечены белки Taxus, обнаруженные в этом исследовании. Функционально идентифицированные белки BAHD выделены желтым фоном.
Ссылки
Акаши Т., Сасаки К., Аоки Т., Аябе С. и Ядзаки К. (2009). Молекулярное клонирование и характеристика кДНК птерокарпан-4-диметилаллилтрансферазы, катализирующей ключевой этап пренилирования в биосинтезе глицеоллина, фитоалексина сои. Физиол растений. 149, 683–693. doi: 10.1104/pp.108.123679
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Балоглу Э. и Кингстон Д. Г. И. (1999). Таксановые дитерпеноиды. J. Nat. Произв. 62, 1448–1472. doi: 10.1021/np9i
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Бэнкс Дж. А., Нишияма Т., Хасебе М., Боуман Дж. Л., Грибсков М., де Памфилис К. и др. (2011). Геном селагинеллы идентифицирует генетические изменения, связанные с эволюцией сосудистых растений. Наука 332, 960–963. doi: 10.1126/science.1203810
Наука 332, 960–963. doi: 10.1126/science.1203810
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Бурго Ф., Хен А., Ларбат Р., Дорпер С., Гонтье Э., Келлнер С. и др. (2006). Биосинтез кумаринов в растениях: основной путь ферментов цитохрома Р450 еще предстоит разгадать. Фитохим. Ред. 5, 293–308. doi: 10.1007/s11101-006-9040-2
CrossRef Полный текст | Google Scholar
Боуман Дж. Л., Кочи Т., Ямато К. Т., Дженкинс Дж., Шу С., Ишизаки К. и др. (2017). Взгляд на эволюцию наземных растений, полученный из генома Marchantia polymorpha. сотовый 171, 287–304. doi: 10.1016/j.cell.2017.09.030
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Крото Р., Кетчум Р. Э. Б., Лонг Р. М., Каспера Р. и Вильдунг М. Р. (2006). Биосинтез таксола и молекулярная генетика. Фитохим. 5, 75–97. doi: 10.1007/s11101-005-3748-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
D'Auria, JC (2006). Ацилтрансферазы в растениях: хорошее время для БАГ. Курс. мнение биол. растений 9, 331–340. doi: 10.1016/j.pbi.2006.03.016
Ацилтрансферазы в растениях: хорошее время для БАГ. Курс. мнение биол. растений 9, 331–340. doi: 10.1016/j.pbi.2006.03.016
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Фани Р. и Фонди М. (2009). Происхождение и эволюция метаболических путей. Физ. Жизнь. 6, 23–52. doi: 10.1016/j.plrev.2008.12.003
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Герра-Бубб Дж., Крото Р. и Уильямс Р. М. (2012). Ранние стадии биосинтеза таксола: промежуточный отчет о синтезе и идентификации метаболитов раннего пути. Нац. Произв. 29, 683–696. doi: 10.1039/c2np20021j
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хаяши К., Хориэ К., Хиваташи Ю., Кавайде Х., Ямагути С., Ханада А. и др. (2010). Эндогенные дитерпены, полученные из ent-kaurene, обычного предшественника гиббереллина, регулируют дифференцировку протонемы мха Physcomitrella patens . Завод физиол. 153, 1085–1097. doi: 10.1104/pp.110.157909
153, 1085–1097. doi: 10.1104/pp.110.157909
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
Карамат Ф., Олри А., Мунаката Р., Коэдука Т., Сугияма А., Пэрис К. и др. (2014). Кумарин-специфичная пренилтрансфераза катализирует решающую биосинтетическую реакцию образования фуранокумарина в петрушке. Завод J. 77, 627–638. doi: 10.1111/tpj.12409
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Кройманн, Дж. (2011). Природное разнообразие и адаптация вторичного метаболизма растений. Курс. мнение биол. растений 14, 246–251. doi: 10.1016/j.pbi.2011.03.021
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
Ли, В. (2016). Введение биологически активных соединений в мембраны: суперсемейство внутримембранных ароматических пренилтрансфераз UbiA. Тенденции биохим. науч. 41, 356–370. doi: 10.1016/j.tibs.2016.01.007
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Мунаката Р. , Иноуэ Т., Коэдука Т., Карамат Ф., Олри А., Сугияма А. и др. (2014). Молекулярное клонирование и характеристика ароматической пренилтрансферазы лимона, специфичной для геранилдифосфата. Физиол растений. 166, 80–90. doi: 10.1104/pp.114.246892
, Иноуэ Т., Коэдука Т., Карамат Ф., Олри А., Сугияма А. и др. (2014). Молекулярное клонирование и характеристика ароматической пренилтрансферазы лимона, специфичной для геранилдифосфата. Физиол растений. 166, 80–90. doi: 10.1104/pp.114.246892
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Мунаката Р., Олри А., Карамат Ф., Курдаво В., Сугияма А., Дате Ю. и др. (2016). Молекулярная эволюция мембраносвязанных пренилтрансфераз пастернака ( Pastinaca sativa ) для линейного и/или углового биосинтеза фуранокумарина. Новый Фитол. 211, 332–344. doi: 10.1111/nph.13899
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
Охара, К., Ямамото, К., Хамамото, М., Сасаки, К., и Язаки, К. (2006). Функциональная характеристика OsPPT1, который кодирует п-гидроксибензоатполипренилтрансферазу, участвующую в биосинтезе убихинона у Oryza sativa . Физиол клеток растений. 47, 581–590. doi: 10.1093/pcp/pcj025
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Садре Р. , Френтцен М., Саид М. и Хоукс Т. (2010). Каталитические реакции гомогентизатпренилтрансферазы, участвующей в пластохиноне-9биосинтез. J. Biol. хим. 285, 18191–18198. doi: 10.1074/jbc.M110.117929
, Френтцен М., Саид М. и Хоукс Т. (2010). Каталитические реакции гомогентизатпренилтрансферазы, участвующей в пластохиноне-9биосинтез. J. Biol. хим. 285, 18191–18198. doi: 10.1074/jbc.M110.117929
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Сасаки К., Мито К., Охара К., Ямамото Х. и Язаки К. (2008). Клонирование и характеристика нарингенин-8-пренилтрансферазы, флавоноид-специфичной пренилтрансферазы Sophora flavescens . Завод физиол. 146, 1075–1084. doi: 10.1104/pp.107.110544
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
Сэвидж Б., Вайс Дж. Д., Вонг Ю. Х., Ласснер М. В., Мицки Т. А., Шьюмейкер С. К. и др. (2002). Выделение и характеристика генов гомогентизат-фитилтрансфераз из Synechocystis sp. PCC 6803 и арабидопсис. Завод физиол. 129, 321–332. doi: 10.1104/pp.010747
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Такахаси С., Огияма Ю. , Кусано Х., Шимада Х., Кавамукаи М. и Кадоваки К. (2006). Метаболическая инженерия кофермента Q путем модификации изопреноидной боковой цепи в растении. ФЭБС Письмо. 580, 955–959. doi: 10.1016/j.febslet.2006.01.023
, Кусано Х., Шимада Х., Кавамукаи М. и Кадоваки К. (2006). Метаболическая инженерия кофермента Q путем модификации изопреноидной боковой цепи в растении. ФЭБС Письмо. 580, 955–959. doi: 10.1016/j.febslet.2006.01.023
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Таканаши К., Накагава Ю., Абурая С., Каминаде К., Аоки В., Саида-Мунаката Ю. и др. (2019). Сравнительный протеомный анализ Lithospermum erythrorhizon показывает регуляцию множества метаболических ферментов, что позволяет всесторонне понять пути биосинтеза шиконина. Физиол клеток растений. 60, 19–28. дои: 10.1093/pcp/pcy183
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Венкатеш Т.В., Карунанандаа Б., Фри Д.Л., Роттнек Дж.М., Базис С.Р. и Валентин Х.Е. (2006). Идентификация и характеристика паралога гомогентизат-фитилтрансферазы Arabidopsis . Планта 223, 1134–1144. doi: 10.1007/s00425-005-0180-1
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Уокер К. и Крото Р. (2000). Молекулярное клонирование кДНК 10-деацетилбаккатин III-10-O-ацетилтрансферазы из Taxus и функциональная экспрессия в Escherichia coli. Проц. Натл. акад. науч. США 97, 583–587. doi: 10.1073/pnas.97.2.583
и Крото Р. (2000). Молекулярное клонирование кДНК 10-деацетилбаккатин III-10-O-ацетилтрансферазы из Taxus и функциональная экспрессия в Escherichia coli. Проц. Натл. акад. науч. США 97, 583–587. doi: 10.1073/pnas.97.2.583
Полный текст CrossRef | Google Scholar
Уокер К., Шендорф А. и Крото Р. (2000). Молекулярное клонирование кДНК таксон-4(20),11(12)-диен-5α-ол-O-ацетилтрансферазы из Taxus и функциональная экспрессия в Escherichia coli . Арх. Биохим. Биофиз. 374, 371–380. doi: 10.1006/abbi.1999.1609
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Венг Дж. К., Филипп Р. Н. и Ноэль Дж. П. (2012). Возникновение хеморазнообразия у растений. Наука 336, 1667–1670. doi: 10.1126/science.1217411
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ву Х., Беннетт Г. Н. и Сан К.-Ю. (2015). Метаболический контроль дыхательных уровней у штаммов Escherichia coli с дефицитом биосинтеза кофермента Q, приводящий к точной аэробной ферментации лактата. Биотехнология. биоинж. 112, 1720–1726 гг. doi: 10.1002/bit.25585
Биотехнология. биоинж. 112, 1720–1726 гг. doi: 10.1002/bit.25585
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
Язаки, К. (2017). Lithospermum erythrorhizon Культуры клеток: настоящее и будущее. Завод Биотехнолог. 34, 131–142. doi: 10.5511/plantbiotechnology.17.0823a
CrossRef Полный текст | Google Scholar
Язаки К., Аримура Г. и Ониши Т. (2017). «Скрытые» терпеноиды в растениях: их биосинтез, локализация и экологическая роль. Физиол клеток растений. 58, 1615–1621. doi: 10.1093/pcp/pcx123
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
Ядзаки К., Кунихиса М., Фуджисаки Т. и Сато Ф. (2002). Геранилдифосфат: 4-гидроксибензоат геранилтрансфераза из Lithospermum erythrorhizon . Клонирование и характеристика ключевого фермента биосинтеза шиконина. J. Biol. хим. 277, 6240–6246. doi: 10.1074/jbc.M106387200
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ёнеяма К.


 2.282.01
2.282.01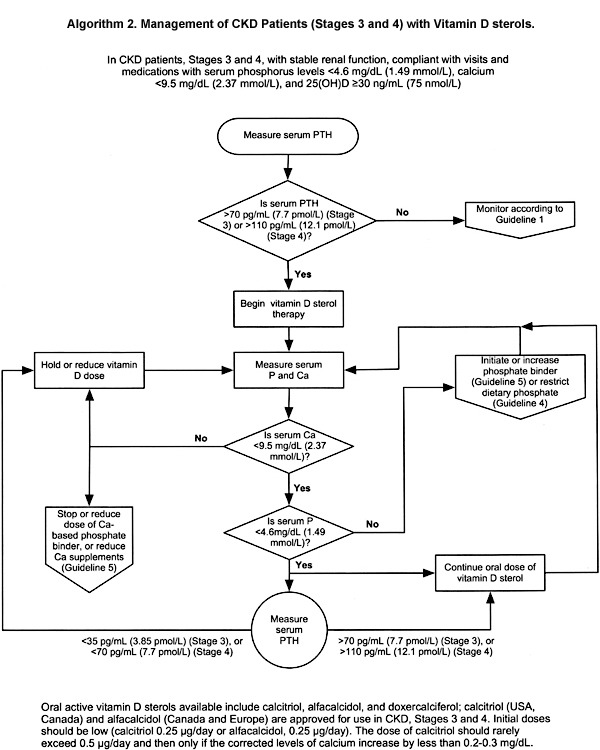 2.282.06
2.282.06 Порядок рецензирования
Порядок рецензирования ), воспалительные заболевания кишечника (болезнь Крона, язвенный
колит), аутовоспалительные заболевания (подагра тяжелого рецидивирующего течения, семейные периодические
лихорадки – периодическая болезнь, криопиринопатии, TRAPS, гипериммуно глобулинемия D), хронические
нагноения (туберкулез, бронхоэктатическая болезнь, остеомиелит и др.), злокачественные солидные опухоли
[1,2,4-6].
), воспалительные заболевания кишечника (болезнь Крона, язвенный
колит), аутовоспалительные заболевания (подагра тяжелого рецидивирующего течения, семейные периодические
лихорадки – периодическая болезнь, криопиринопатии, TRAPS, гипериммуно глобулинемия D), хронические
нагноения (туберкулез, бронхоэктатическая болезнь, остеомиелит и др.), злокачественные солидные опухоли
[1,2,4-6].

 Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].
Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].

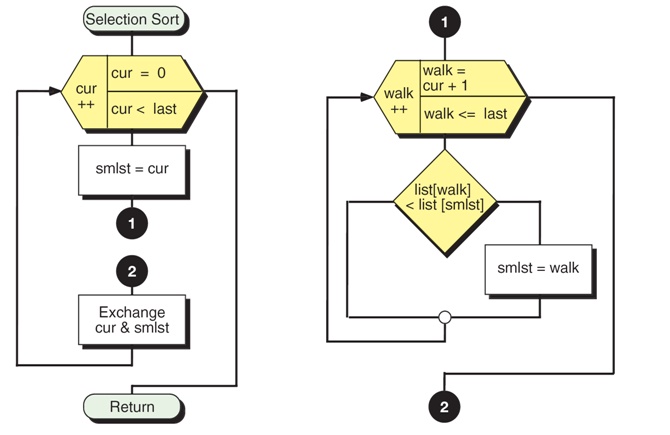 Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].

 Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.

 Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].
Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39]. Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51].
Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51]. Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
 Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].

 В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79].
В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79].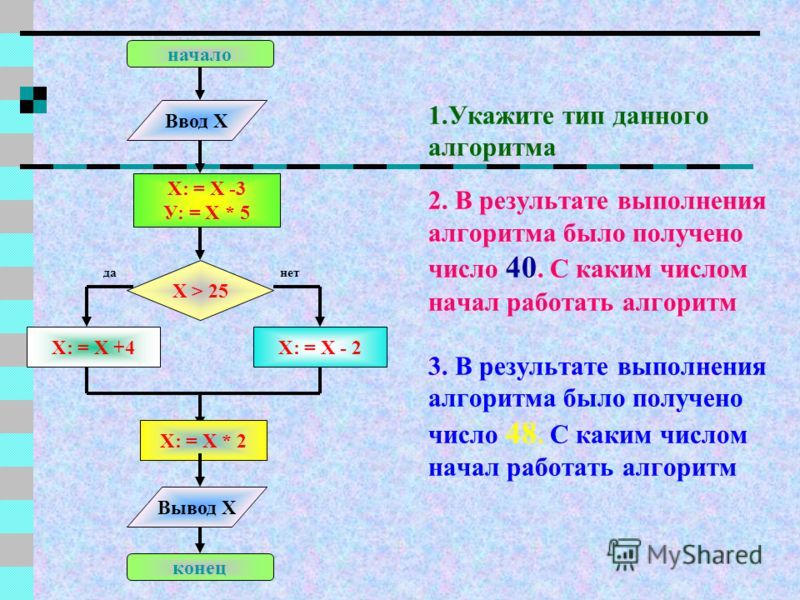 Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].





 В., Рамеева А.С., Тао П.П. Оптимизация страте-гии ведения больных вторичным АА-амилоидозом. Врач 2019;30(5):3-11[Rameev VV, Kozlovskaya LV, Rameeva AS, Tao PP. Optimization of the man-agement strategy for patients with secondary AA-amyloidosis. Vrach 2019;30(5):3-11 (In Russ.)].
В., Рамеева А.С., Тао П.П. Оптимизация страте-гии ведения больных вторичным АА-амилоидозом. Врач 2019;30(5):3-11[Rameev VV, Kozlovskaya LV, Rameeva AS, Tao PP. Optimization of the man-agement strategy for patients with secondary AA-amyloidosis. Vrach 2019;30(5):3-11 (In Russ.)].
 Monitoring neutrophil activationin juvenile rheumatoid arthritis by S100A12 serum concentrations. ArthritisRheum 2004;50(4):1286–95.
Monitoring neutrophil activationin juvenile rheumatoid arthritis by S100A12 serum concentrations. ArthritisRheum 2004;50(4):1286–95.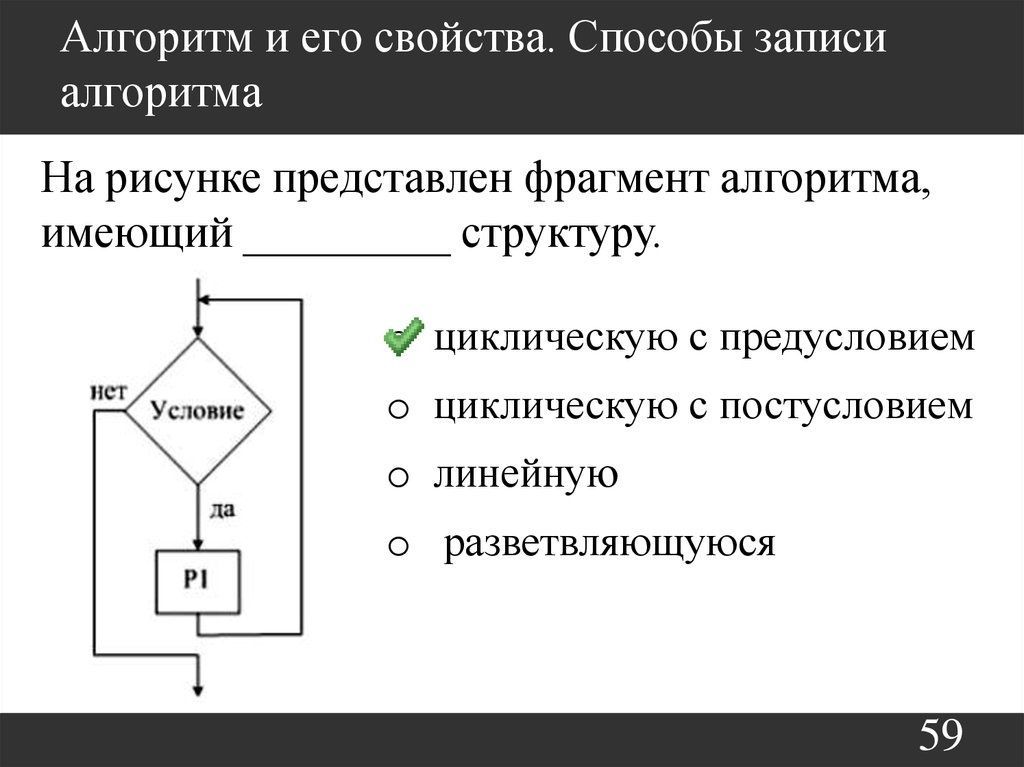

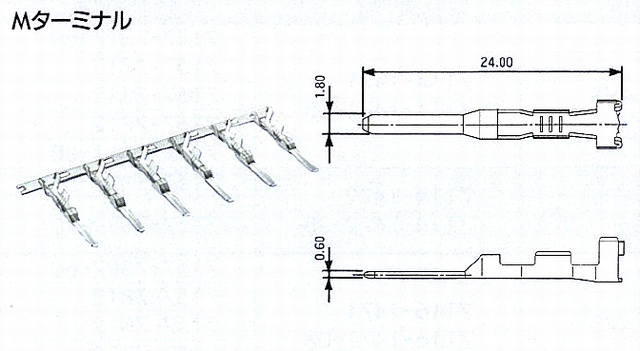 Amyloidosis: a review of recent diagnosticand therapeutic developments. Br J Haematol 1997;99:245-56.
Amyloidosis: a review of recent diagnosticand therapeutic developments. Br J Haematol 1997;99:245-56.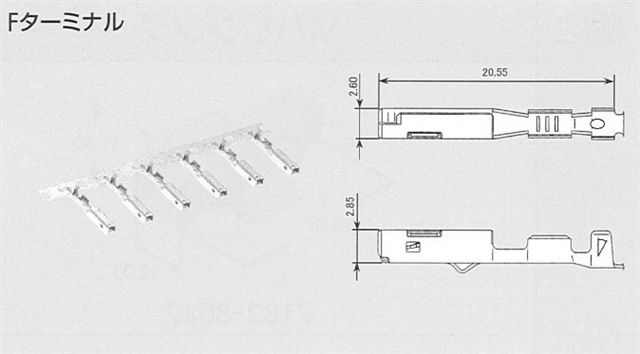 J Clin Pathol 2014;67:661–6.
J Clin Pathol 2014;67:661–6. Я., Полякова А.А., Амелин А.В. и др. Не VAL30MET-транстире-тиновая амилоидная кардиомиопатия. Обзор сведений литературы и кли-ническое наблюдение. Российский кардиологический журнал 2018;2(154):121-128 [Gudkova AJ, Polyakova AA, et al. Non-Val30Met-trans thyretin amyloidcardiomyopathy. Review of literature, data and clinical case. Rossijskij kardio-logicheskij zhurnal 2018;2(154):121-8 (In Russ.)].
Я., Полякова А.А., Амелин А.В. и др. Не VAL30MET-транстире-тиновая амилоидная кардиомиопатия. Обзор сведений литературы и кли-ническое наблюдение. Российский кардиологический журнал 2018;2(154):121-128 [Gudkova AJ, Polyakova AA, et al. Non-Val30Met-trans thyretin amyloidcardiomyopathy. Review of literature, data and clinical case. Rossijskij kardio-logicheskij zhurnal 2018;2(154):121-8 (In Russ.)]. J Neurol Neurosurg Psychiatry2015;86(9):1036-43.
J Neurol Neurosurg Psychiatry2015;86(9):1036-43.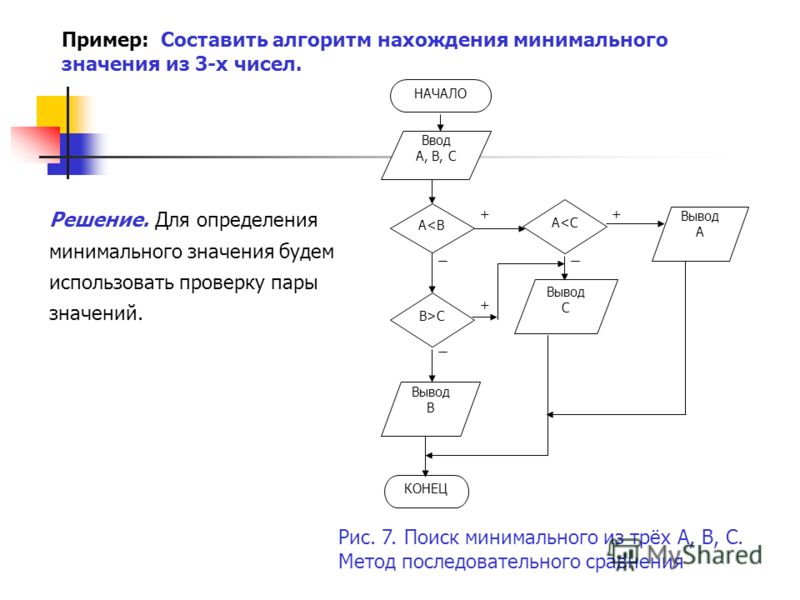 Kidney Dis 2016;2:10-9.
Kidney Dis 2016;2:10-9. Prolonged renal survival in light chainamyloidosis: speed and magnitude of light chain reduction is the crucial factor.Kidney Int 2017;92(6):1476-83.
Prolonged renal survival in light chainamyloidosis: speed and magnitude of light chain reduction is the crucial factor.Kidney Int 2017;92(6):1476-83. J Clin Oncol2012;30:4541–9.
J Clin Oncol2012;30:4541–9. Ann Med 2012;44(7):664–73.
Ann Med 2012;44(7):664–73.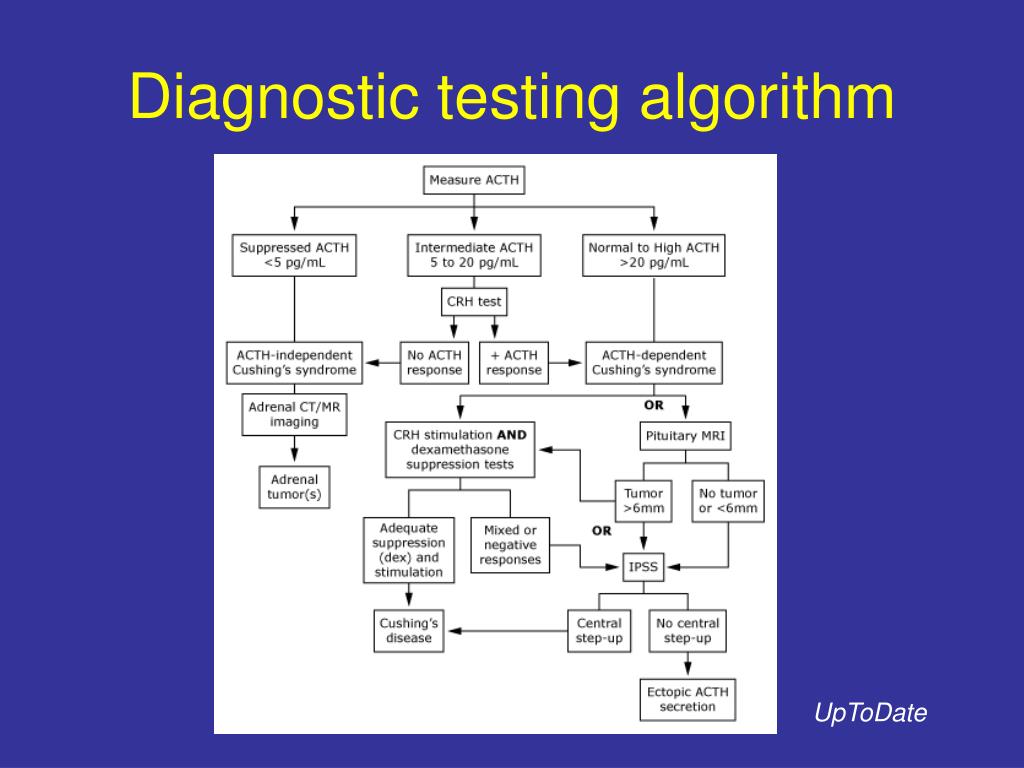
 Superior survival in primary systemicamyloidosis patients undergoing peripheral blood stem cell transplantation: a case-control study. Blood 2004;103(10):3960-3.
Superior survival in primary systemicamyloidosis patients undergoing peripheral blood stem cell transplantation: a case-control study. Blood 2004;103(10):3960-3. R. Review article: insights into colonic protein fermentation, its modulation and potential health implications // Aliment Pharmacol Th er. – 2016.-43(2). – 1–16
R. Review article: insights into colonic protein fermentation, its modulation and potential health implications // Aliment Pharmacol Th er. – 2016.-43(2). – 1–16 et al. Diagnosis of small intestinal bacterial overgrowth in the clinical practice // European Review for Medical and Pharmacological Sciences. – 2013.-17(Suppl 2). – 30–35.
et al. Diagnosis of small intestinal bacterial overgrowth in the clinical practice // European Review for Medical and Pharmacological Sciences. – 2013.-17(Suppl 2). – 30–35.
 – 2013. – Vol 5. – 234–252.
– 2013. – Vol 5. – 234–252. K., Chang H. W., Yan D. et al. Infl uence of diet on the gut microbiome and implications for human health // J Transl Med. – 2017. – 15(1).-73.
K., Chang H. W., Yan D. et al. Infl uence of diet on the gut microbiome and implications for human health // J Transl Med. – 2017. – 15(1).-73. Carbohydrate metabolism in Bifi dobacteria. // Genes Nutr. – 2011. – 6. – 285–306.
Carbohydrate metabolism in Bifi dobacteria. // Genes Nutr. – 2011. – 6. – 285–306. – p. 745–767.
– p. 745–767.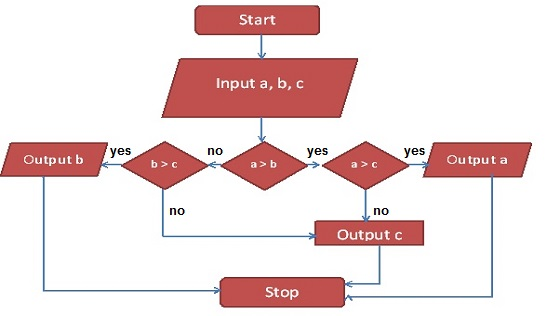

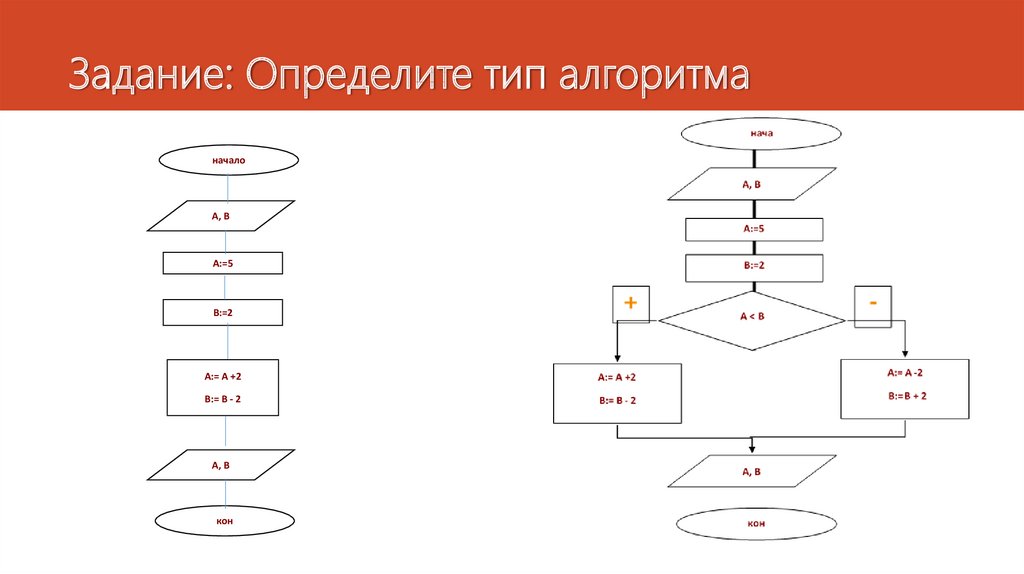


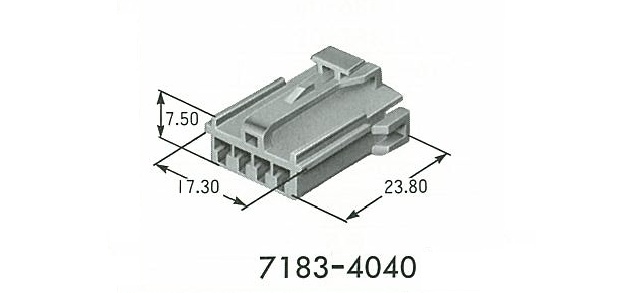

 Стабильный, если <1.
Стабильный, если <1.
 Н. Папакостас и Г. Папа Джорджиу, Математика вычислений, том 65, номер 215, 19 июля.96, страницы 1165-1181.
Н. Папакостас и Г. Папа Джорджиу, Математика вычислений, том 65, номер 215, 19 июля.96, страницы 1165-1181. A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558.
A.Luther and H.P.Konen, Siam Review, Vol. 3, № 7, (октябрь 1965 г.), страницы 551–558. 32, № 6, 1996, страницы с 15 по 28
32, № 6, 1996, страницы с 15 по 28 34, № 1 (1993), страницы с 62 по 74.
34, № 1 (1993), страницы с 62 по 74. constructVerner6
constructVerner6  constructchummund6
constructchummund6  Д. Лоусон, Siam Journal по численному анализу, Vol. 4, № 4 (19 декабря67) стр. 620-625.
Д. Лоусон, Siam Journal по численному анализу, Vol. 4, № 4 (19 декабря67) стр. 620-625. Е.А. Эль-Миккави и М.М.М. Эйса, Прикладная математика и вычисления, Vol. 143, № 2, (2003) страницы 259–267.
Е.А. Эль-Миккави и М.М.М. Эйса, Прикладная математика и вычисления, Vol. 143, № 2, (2003) страницы 259–267. constructTanakaYamasitaEfficient7
constructTanakaYamasitaEfficient7 

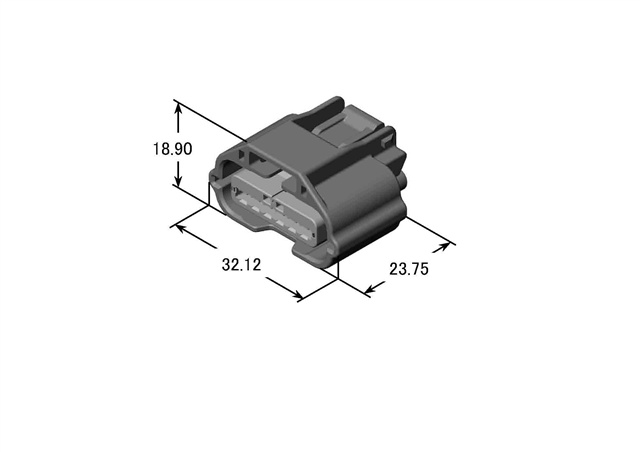
 constructFeagin10Tableau
constructFeagin10Tableau  6, № 3, (2006) страницы 177–186
6, № 3, (2006) страницы 177–186 constructLobattoIIIC2
constructLobattoIIIC2  constructRadauIIA3
constructRadauIIA3 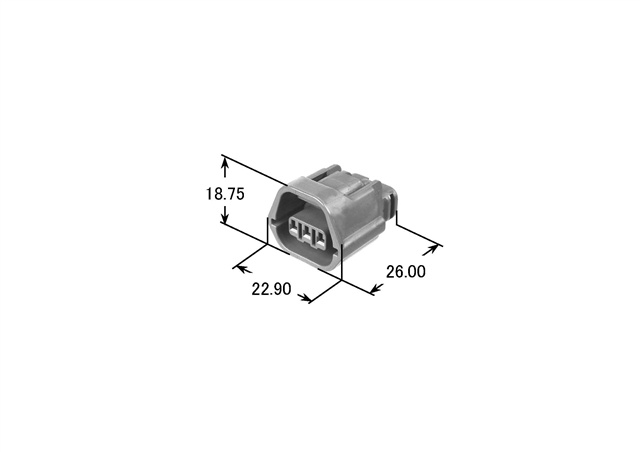 Шивли
Шивли Ву,
Ву, Язаки, Марк А. Шерман, Джон Э. Шивли, Дэвид Икл, Лоуренс Э. Уильямс, Джеффри Ю.К. Вонг, Дэвид Колчер, Анна М. Ву, Эндрю А. Раубичек, Гуманизация антитела против СЕА T84.66 на основе данных о кристаллической структуре, Белковая инженерия, дизайн и отбор , том 17, выпуск 5, май 2004 г., страницы 481–489, https://doi.org/10.1093/protein/gzh056
Язаки, Марк А. Шерман, Джон Э. Шивли, Дэвид Икл, Лоуренс Э. Уильямс, Джеффри Ю.К. Вонг, Дэвид Колчер, Анна М. Ву, Эндрю А. Раубичек, Гуманизация антитела против СЕА T84.66 на основе данных о кристаллической структуре, Белковая инженерия, дизайн и отбор , том 17, выпуск 5, май 2004 г., страницы 481–489, https://doi.org/10.1093/protein/gzh056 66 (cT84.66) представляет собой моноклональное антитело (мАт) с высокой специфичностью и аффинностью к опухолеассоциированному карциноэмбриональному антигену (СЕА). Радиоактивно-меченый cT84.66 продемонстрировал полезность в клинике в качестве реагента для радиоиммуносцинтиграфии и радиоиммунотерапии СЕА-положительных колоректальных опухолей и злокачественных новообразований молочной железы. Для увеличения терапевтической эффективности T84.66 использовали гуманизацию путем прививки определяющей комплементарность области (CDR). Прививка CDR является хорошо зарекомендовавшим себя методом, хотя часто для восстановления высокой аффинности требуется серия обратных мутаций каркаса. Недавно была определена кристаллическая структура диатела T84.66 (димер scFv), полученного из мышиного mAb T84.66, что облегчило процесс гуманизации благодаря наличию данных о кристаллической структуре как донора, так и акцептора трансплантата. Поиск в Protein Data Bank выявил близкое структурное сходство (среднеквадратичное отклонение 1,07 Å) между Fv T84.
66 (cT84.66) представляет собой моноклональное антитело (мАт) с высокой специфичностью и аффинностью к опухолеассоциированному карциноэмбриональному антигену (СЕА). Радиоактивно-меченый cT84.66 продемонстрировал полезность в клинике в качестве реагента для радиоиммуносцинтиграфии и радиоиммунотерапии СЕА-положительных колоректальных опухолей и злокачественных новообразований молочной железы. Для увеличения терапевтической эффективности T84.66 использовали гуманизацию путем прививки определяющей комплементарность области (CDR). Прививка CDR является хорошо зарекомендовавшим себя методом, хотя часто для восстановления высокой аффинности требуется серия обратных мутаций каркаса. Недавно была определена кристаллическая структура диатела T84.66 (димер scFv), полученного из мышиного mAb T84.66, что облегчило процесс гуманизации благодаря наличию данных о кристаллической структуре как донора, так и акцептора трансплантата. Поиск в Protein Data Bank выявил близкое структурное сходство (среднеквадратичное отклонение 1,07 Å) между Fv T84. 66 и Fv 4D5v8, гуманизированного анти-p185 9.Антитело 1121 HER2 , продаваемое как Герцептин® (трастузумаб). Это привело к двум гуманизированным версиям mAb M5A и M5B T84.66, которые различались только количеством мышиных остатков, присутствующих в C-концевой половине CDR-h3. Для оценки гуманизированных mAb были проведены биохимический анализ и исследования биораспределения на животных. мАт M5A, M5B и cT84.66 проявляли субнаномолярное сродство к СЕА, а в качестве радиоактивно меченых мАт обнаруживали специфическую локализацию в опухоли у мышей с опухолями. мАт T84.66 M5A было выбрано для клинической разработки из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и было переименовано в hT84.66. Ограниченное производство и исследование изображений на животных продемонстрировали способность hT84.66 поддерживать клинические испытания. Запланированные клинические испытания определят эффективное использование этого структурного подхода при разработке многообещающего нового терапевтического средства.
66 и Fv 4D5v8, гуманизированного анти-p185 9.Антитело 1121 HER2 , продаваемое как Герцептин® (трастузумаб). Это привело к двум гуманизированным версиям mAb M5A и M5B T84.66, которые различались только количеством мышиных остатков, присутствующих в C-концевой половине CDR-h3. Для оценки гуманизированных mAb были проведены биохимический анализ и исследования биораспределения на животных. мАт M5A, M5B и cT84.66 проявляли субнаномолярное сродство к СЕА, а в качестве радиоактивно меченых мАт обнаруживали специфическую локализацию в опухоли у мышей с опухолями. мАт T84.66 M5A было выбрано для клинической разработки из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и было переименовано в hT84.66. Ограниченное производство и исследование изображений на животных продемонстрировали способность hT84.66 поддерживать клинические испытания. Запланированные клинические испытания определят эффективное использование этого структурного подхода при разработке многообещающего нового терапевтического средства.
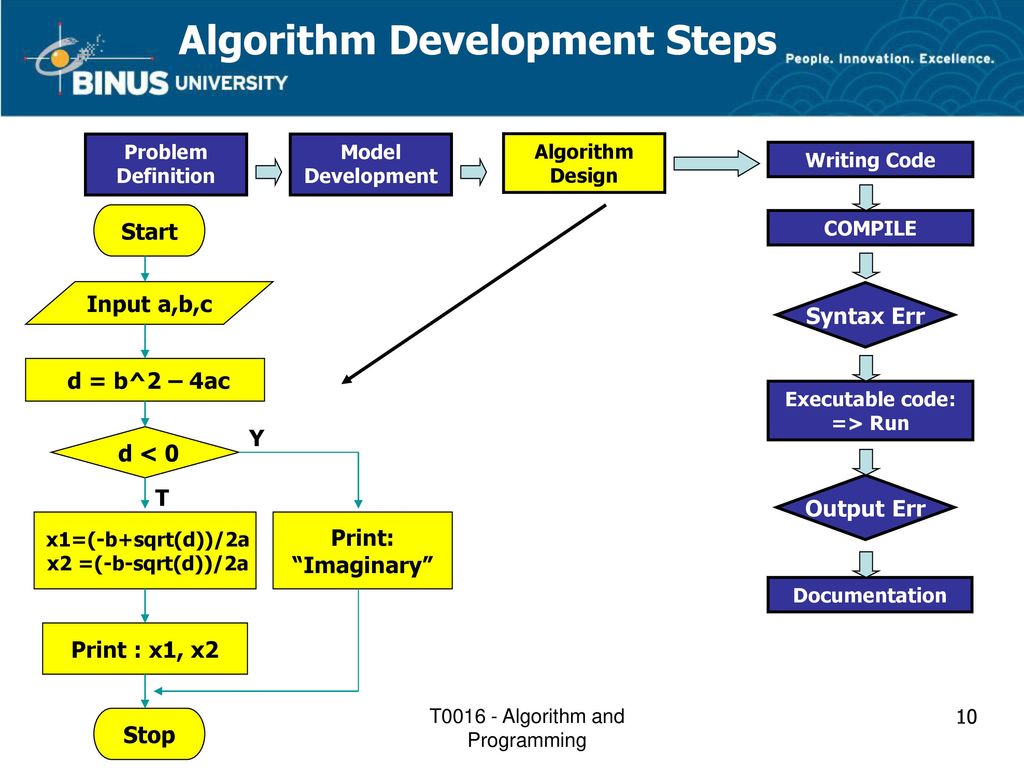 97) проходят текущую клиническую оценку.
97) проходят текущую клиническую оценку. 66. Это препятствовало выбору совершенно нового mAb из библиотек фагового дисплея генов иммуноглобулинов человека или трансгенных животных. Таким образом, проводилась гуманизация путем прививки мышиных CDR на Fv-каркас человека. В опубликованной литературе имеется множество примеров гуманизации антител с помощью прививки CDR (O'Brien, 2003). Однако часто наблюдалась существенная потеря аффинности связывания антигена из-за стерических столкновений между человеческим каркасом и остатками CDR мыши, которые изменяли конформацию антигенсвязывающих петель. Эти непредвиденные столкновения являются результатом использования молекулярных моделей для разработки трансплантата, а не реальных кристаллических структур молекул донора и акцептора трансплантата. Часто требуется трудоемкий и часто случайный повторяющийся процесс введения обратных мутаций для восстановления ключевых остатков мышиного каркаса, ответственных за поддержание правильной конформации петли (Foote, 19).92).
66. Это препятствовало выбору совершенно нового mAb из библиотек фагового дисплея генов иммуноглобулинов человека или трансгенных животных. Таким образом, проводилась гуманизация путем прививки мышиных CDR на Fv-каркас человека. В опубликованной литературе имеется множество примеров гуманизации антител с помощью прививки CDR (O'Brien, 2003). Однако часто наблюдалась существенная потеря аффинности связывания антигена из-за стерических столкновений между человеческим каркасом и остатками CDR мыши, которые изменяли конформацию антигенсвязывающих петель. Эти непредвиденные столкновения являются результатом использования молекулярных моделей для разработки трансплантата, а не реальных кристаллических структур молекул донора и акцептора трансплантата. Часто требуется трудоемкий и часто случайный повторяющийся процесс введения обратных мутаций для восстановления ключевых остатков мышиного каркаса, ответственных за поддержание правильной конформации петли (Foote, 19).92). 66 была решена с помощью рентгеноструктурного анализа диатела T84.66 (димер scFv) с разрешением 2,6 Å (Carmichael, 2003). Поиск в банке белковых данных выявил близкое структурное сходство с 4D5v8, гуманизированным антителом против p185 HER2 , продаваемым как Герцептин® (трастузумаб). Компьютерная графическая визуализация наложенных структур позволила сделать рациональный выбор сплайс-соединений трансплантатов и обратных мутаций каркаса. Путем прививки CDR были созданы две версии: mAb T84.66 M5A и mAb T84.66 M5B. Они различались только количеством мышиных остатков, присутствующих в С-концевой половине CDR-h3. Биохимические исследования и исследования биораспределения на животных использовали для сравнения гуманизированных mAb с химерной версией. Все mAb M5A, M5B и cT84.66 имели схожую субнаномолярную аффинность к СЕА и, будучи радиоактивно мечеными мАт, проявляли специфическую локализацию в опухоли у бестимусных мышей, несущих ксенотрансплантаты опухоли с положительным результатом на СЕА.
66 была решена с помощью рентгеноструктурного анализа диатела T84.66 (димер scFv) с разрешением 2,6 Å (Carmichael, 2003). Поиск в банке белковых данных выявил близкое структурное сходство с 4D5v8, гуманизированным антителом против p185 HER2 , продаваемым как Герцептин® (трастузумаб). Компьютерная графическая визуализация наложенных структур позволила сделать рациональный выбор сплайс-соединений трансплантатов и обратных мутаций каркаса. Путем прививки CDR были созданы две версии: mAb T84.66 M5A и mAb T84.66 M5B. Они различались только количеством мышиных остатков, присутствующих в С-концевой половине CDR-h3. Биохимические исследования и исследования биораспределения на животных использовали для сравнения гуманизированных mAb с химерной версией. Все mAb M5A, M5B и cT84.66 имели схожую субнаномолярную аффинность к СЕА и, будучи радиоактивно мечеными мАт, проявляли специфическую локализацию в опухоли у бестимусных мышей, несущих ксенотрансплантаты опухоли с положительным результатом на СЕА.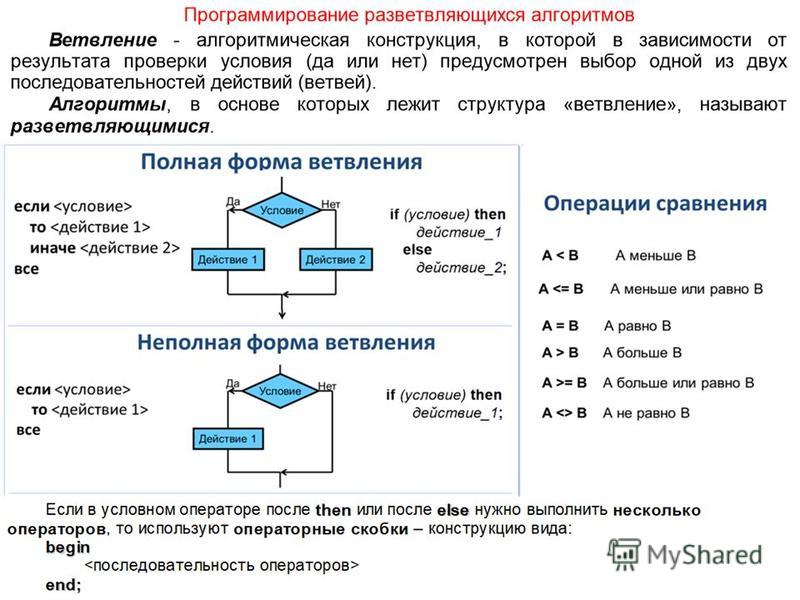 T84.66 M5A был выбран для доклинического производства из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и был переименован в mAb hT84.66. Было проведено масштабное производство, чтобы продемонстрировать способность этого клона поддерживать клинические испытания. Запланированные клинические испытания определят эффективность использования этого структурного подхода.
T84.66 M5A был выбран для доклинического производства из-за несколько более высокого поглощения опухолью и большего содержания человеческих остатков и был переименован в mAb hT84.66. Было проведено масштабное производство, чтобы продемонстрировать способность этого клона поддерживать клинические испытания. Запланированные клинические испытания определят эффективность использования этого структурного подхода. Из 20 антител, появившихся в списке гомологичных структур, пять были выбраны для дальнейшего рассмотрения на основании их высокой степени перекрытия альфа-углерода с запрашиваемой структурой (среднеквадратическое среднеквадратичное отклонение от 1,00 до 1,25 Å). Затем были идентифицированы остатки, определяющие каркасные области по Кабату, и они были наложены на атомы каркаса исследуемой структуры (1312 атомов), в результате чего было получено среднеквадратичное отклонение. значения 1,00 Å (файл PDB1CZ8), 1,00 Å (2FGW), 1,06 Å (1AD9), 1,06 Å (1FVC) и 1,06 Å (1BJ1). Учитывая близость этих значений, в качестве второго фактора скрининга рассчитывали процентную идентичность последовательностей (общую и только каркасную). Полученные значения для 1CZ8 (в целом 63%, каркас 54%), 2FGW (61% и 54%), 1AD9 (65% и 60%), 1FVC (67% и 61%) и 1BJ1 (63% и 53%). %), предположили, что 1FVC [гуманизированное антитело 4D5, версия 8, анти-p185 HER2 , герцептин трастузумаб, (Eigenbrot, 1993)] является наиболее подходящим источником каркаса, поскольку степень перекрытия и процент идентичности последовательностей были высокими.
Из 20 антител, появившихся в списке гомологичных структур, пять были выбраны для дальнейшего рассмотрения на основании их высокой степени перекрытия альфа-углерода с запрашиваемой структурой (среднеквадратическое среднеквадратичное отклонение от 1,00 до 1,25 Å). Затем были идентифицированы остатки, определяющие каркасные области по Кабату, и они были наложены на атомы каркаса исследуемой структуры (1312 атомов), в результате чего было получено среднеквадратичное отклонение. значения 1,00 Å (файл PDB1CZ8), 1,00 Å (2FGW), 1,06 Å (1AD9), 1,06 Å (1FVC) и 1,06 Å (1BJ1). Учитывая близость этих значений, в качестве второго фактора скрининга рассчитывали процентную идентичность последовательностей (общую и только каркасную). Полученные значения для 1CZ8 (в целом 63%, каркас 54%), 2FGW (61% и 54%), 1AD9 (65% и 60%), 1FVC (67% и 61%) и 1BJ1 (63% и 53%). %), предположили, что 1FVC [гуманизированное антитело 4D5, версия 8, анти-p185 HER2 , герцептин трастузумаб, (Eigenbrot, 1993)] является наиболее подходящим источником каркаса, поскольку степень перекрытия и процент идентичности последовательностей были высокими.
 66 присутствовала в пересаженной структуре, что привело к получению второй гуманизированной конструкции, M5B. Чтобы приспособить дополнительный сегмент, каркасный остаток H67 (phe) был заменен его мышиным эквивалентом (ala), чтобы облегчить стерическое столкновение с CDR-h3 остатком H63 (phe).
66 присутствовала в пересаженной структуре, что привело к получению второй гуманизированной конструкции, M5B. Чтобы приспособить дополнительный сегмент, каркасный остаток H67 (phe) был заменен его мышиным эквивалентом (ala), чтобы облегчить стерическое столкновение с CDR-h3 остатком H63 (phe). 1.
1.  Использование GeneAmp PCR 9600 (Perkin Elmer, Wellesley, MA), образцы нагревали в течение 2 мин при 94°C, после чего следовали 30 циклов нагревания по 30 с при 94°C, 30 с при 55°C и 30 с при 72°C. После 30 циклов температуру поддерживали постоянной на уровне 72°С в течение 10 мин для обеспечения полного удлинения. В каждом случае готовую реакционную смесь для ПЦР подвергали электрофорезу на 1% агарозном геле (Sigma Chemical, Сент-Луис, Миссури) и желаемый продукт экстрагировали из среза геля массой 200 мг с использованием колонки Qiaquik (Qiagen, Валенсия, Калифорния). Для второй, третьей и четвертой реакций в качестве матрицы использовали 10 нг очищенного продукта предыдущей реакции. По отдельности очищенные полноразмерные синтетические гены расщепляли Xba I и Xho I и лигировали в одну из двух экспрессионных плазмид (pEE12 для VL; pEE6 для VH). Эти плазмиды, которые содержат ген глутаминсинтетазы (GS) (Lonza Biologics, Slough, UK; Bebbington, 1992), были предварительно модифицированы, чтобы содержать кДНК, соответствующую константным областям человеческого антитела IgG 1 .
Использование GeneAmp PCR 9600 (Perkin Elmer, Wellesley, MA), образцы нагревали в течение 2 мин при 94°C, после чего следовали 30 циклов нагревания по 30 с при 94°C, 30 с при 55°C и 30 с при 72°C. После 30 циклов температуру поддерживали постоянной на уровне 72°С в течение 10 мин для обеспечения полного удлинения. В каждом случае готовую реакционную смесь для ПЦР подвергали электрофорезу на 1% агарозном геле (Sigma Chemical, Сент-Луис, Миссури) и желаемый продукт экстрагировали из среза геля массой 200 мг с использованием колонки Qiaquik (Qiagen, Валенсия, Калифорния). Для второй, третьей и четвертой реакций в качестве матрицы использовали 10 нг очищенного продукта предыдущей реакции. По отдельности очищенные полноразмерные синтетические гены расщепляли Xba I и Xho I и лигировали в одну из двух экспрессионных плазмид (pEE12 для VL; pEE6 для VH). Эти плазмиды, которые содержат ген глутаминсинтетазы (GS) (Lonza Biologics, Slough, UK; Bebbington, 1992), были предварительно модифицированы, чтобы содержать кДНК, соответствующую константным областям человеческого антитела IgG 1 . В плазмиде легкой цепи рЕЕ12 остаток L104, кодон которого является частью сайта рестрикции Xho I, мутировали с лейцина на валин с использованием набора QuikChange (Stratagene, Сан-Диего, Калифорния) для восстановления последовательности герцептина в этом область, край. Двухцепочечная плазмида была сконструирована путем расщепления плазмиды тяжелой цепи pEE6 с помощью Bgl II и Bam HI для выделения гена тяжелой цепи, который затем лигировали в сайт Bam HI плазмиды легкой цепи pEE12. Весь ген IgG 1 был секвенирован в обоих направлениях для подтверждения его идентичности. Перед электропорацией двухцепочечную плазмиду линеаризовали с помощью Sal I, фильтровали через связывающую белок мембрану для удаления рестриктазы (Millipore, Bedford, MA), осаждали этанолом и ресуспендировали в стерильной воде до концентрации 1 мкг/мл. мкл.
В плазмиде легкой цепи рЕЕ12 остаток L104, кодон которого является частью сайта рестрикции Xho I, мутировали с лейцина на валин с использованием набора QuikChange (Stratagene, Сан-Диего, Калифорния) для восстановления последовательности герцептина в этом область, край. Двухцепочечная плазмида была сконструирована путем расщепления плазмиды тяжелой цепи pEE6 с помощью Bgl II и Bam HI для выделения гена тяжелой цепи, который затем лигировали в сайт Bam HI плазмиды легкой цепи pEE12. Весь ген IgG 1 был секвенирован в обоих направлениях для подтверждения его идентичности. Перед электропорацией двухцепочечную плазмиду линеаризовали с помощью Sal I, фильтровали через связывающую белок мембрану для удаления рестриктазы (Millipore, Bedford, MA), осаждали этанолом и ресуспендировали в стерильной воде до концентрации 1 мкг/мл. мкл. Селекция трансфектантов в культуральной среде без глютамина (JRH Biosciences, Kenexa, KN) привела к многочисленным клонам, которые подвергали скринингу с использованием рекомбинантного фрагмента СЕА (Young, 1998) на основе ELISA (Yazaki, 2001). M5A mAb получали в биореакторе с полыми волокнами Cell Pharm (CP) 2000 в соответствии с руководством оператора (Biovest International, Minneapolis, MN). CP2000 был оснащен одним картриджем с полым волокном площадью 20 кв. футов (за исключением молекулярной массы 10 кДа) и оксигенатором площадью 10 кв. футов. Уровни рН, глюкозы, лактата, аммиака и продукции антител контролировали через день. Внесены коррективы в поступающий O 2 и CO 2 для поддержания pH в диапазоне от 7,0 до 7,2. Среду IMDM (Biowhittaker, Walkerville, MD) с добавлением 2% эмбриональной бычьей сыворотки (FBS) (Hyclone, Logan, UT) использовали во внутрикапиллярном пространстве (ICS). Селективную среду GS (JRH Bioscience, Lenexa, KS) +2% FBS использовали во внекапиллярном пространстве (ECS).
Селекция трансфектантов в культуральной среде без глютамина (JRH Biosciences, Kenexa, KN) привела к многочисленным клонам, которые подвергали скринингу с использованием рекомбинантного фрагмента СЕА (Young, 1998) на основе ELISA (Yazaki, 2001). M5A mAb получали в биореакторе с полыми волокнами Cell Pharm (CP) 2000 в соответствии с руководством оператора (Biovest International, Minneapolis, MN). CP2000 был оснащен одним картриджем с полым волокном площадью 20 кв. футов (за исключением молекулярной массы 10 кДа) и оксигенатором площадью 10 кв. футов. Уровни рН, глюкозы, лактата, аммиака и продукции антител контролировали через день. Внесены коррективы в поступающий O 2 и CO 2 для поддержания pH в диапазоне от 7,0 до 7,2. Среду IMDM (Biowhittaker, Walkerville, MD) с добавлением 2% эмбриональной бычьей сыворотки (FBS) (Hyclone, Logan, UT) использовали во внутрикапиллярном пространстве (ICS). Селективную среду GS (JRH Bioscience, Lenexa, KS) +2% FBS использовали во внекапиллярном пространстве (ECS). Скорость подачи ИКС составляла 1,0–2,2 л/сут, скорость рециркуляции – 350–500 мл/мин. К ECS был подключен автоуборочный комбайн (Biowest International), запрограммированный на производительность 30–80 мл в сутки.
Скорость подачи ИКС составляла 1,0–2,2 л/сут, скорость рециркуляции – 350–500 мл/мин. К ECS был подключен автоуборочный комбайн (Biowest International), запрограммированный на производительность 30–80 мл в сутки. Начальный захват проводили на колонке Prosep rA (Millipore, 1 см × 10 см, 2,5 мл/мин), предварительно уравновешенной PBS. Осветленный урожай загружали и промывали смесью 0,02 М цитрата натрия/0,02 М фосфата натрия, рН 7,4/0,5 М хлорида натрия. Антитело элюировали линейным градиентом от 100% 0,01 М фосфата натрия, рН 7,4, до 100% 0,01 М фосфата натрия, рН 4,0. Элюированный материал собирали в пробирки, содержащие 0,05 М фосфата натрия, рН 8,0 (10% по объему). Элюированный пик белка А подвергали диализу относительно 0,05 М фосфата натрия, рН 5,5, в течение ночи перед загрузкой на катионообменную колонку Source 15S (GE Biosciences, Piscataway, NJ; 0,4 см × 10 см, 2 мл/мин). МкАТ элюировали линейным градиентом от 0 до 0,4 М хлорида натрия/0,05 М фосфата натрия, рН 5,5. Элюированное антитело собирали в пробирки, содержащие 1 М трис, рН 8,0 (10% по объему). При анализе с помощью SDS-PAGE и ВЭЖХ фракции, содержащие антитела, объединяли и подвергали диализу в течение ночи по сравнению с PBS.
Начальный захват проводили на колонке Prosep rA (Millipore, 1 см × 10 см, 2,5 мл/мин), предварительно уравновешенной PBS. Осветленный урожай загружали и промывали смесью 0,02 М цитрата натрия/0,02 М фосфата натрия, рН 7,4/0,5 М хлорида натрия. Антитело элюировали линейным градиентом от 100% 0,01 М фосфата натрия, рН 7,4, до 100% 0,01 М фосфата натрия, рН 4,0. Элюированный материал собирали в пробирки, содержащие 0,05 М фосфата натрия, рН 8,0 (10% по объему). Элюированный пик белка А подвергали диализу относительно 0,05 М фосфата натрия, рН 5,5, в течение ночи перед загрузкой на катионообменную колонку Source 15S (GE Biosciences, Piscataway, NJ; 0,4 см × 10 см, 2 мл/мин). МкАТ элюировали линейным градиентом от 0 до 0,4 М хлорида натрия/0,05 М фосфата натрия, рН 5,5. Элюированное антитело собирали в пробирки, содержащие 1 М трис, рН 8,0 (10% по объему). При анализе с помощью SDS-PAGE и ВЭЖХ фракции, содержащие антитела, объединяли и подвергали диализу в течение ночи по сравнению с PBS. 66 подвергли электрофорезу с помощью SDS-PAGE (Laemmli, 1970). Эксклюзионную хроматографию проводили на колонке Superdex 200 HR10/30 (GE Biosciences, 0,5 мл/мин) в изократическом режиме с PBS. Колонку стандартизировали стандартами гель-фильтрации (Bio-Rad Laboratories). Изоэлектрическую точку каждого mAb определяли в гелях IEF с pH 3–10 (Novex Inc., Сан-Диего, Калифорния) и сравнивали со стандартами белка IEF (Serva Electrophoresis, Heidelberg, Germany).
66 подвергли электрофорезу с помощью SDS-PAGE (Laemmli, 1970). Эксклюзионную хроматографию проводили на колонке Superdex 200 HR10/30 (GE Biosciences, 0,5 мл/мин) в изократическом режиме с PBS. Колонку стандартизировали стандартами гель-фильтрации (Bio-Rad Laboratories). Изоэлектрическую точку каждого mAb определяли в гелях IEF с pH 3–10 (Novex Inc., Сан-Диего, Калифорния) и сравнивали со стандартами белка IEF (Serva Electrophoresis, Heidelberg, Germany).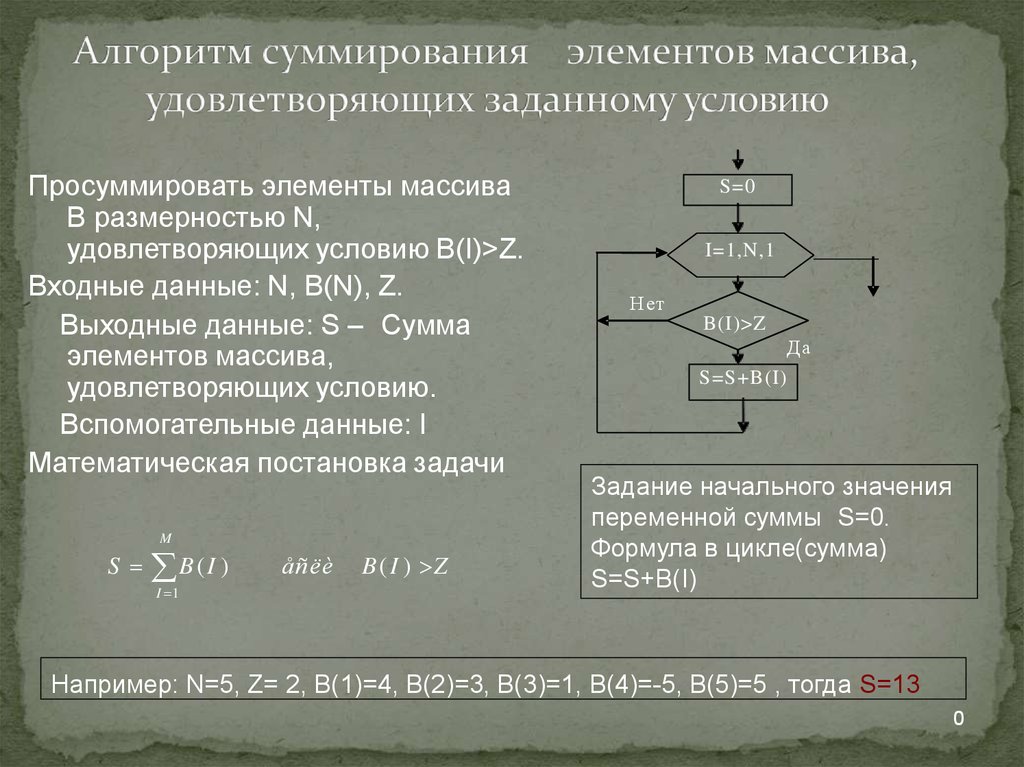 . Данные были проанализированы с помощью программного обеспечения BIAevaluation (v3.0) с использованием модели двухвалентного аналита для расчета K A = k на / k на . Концентрации белка определяли аминокислотным анализом.
. Данные были проанализированы с помощью программного обеспечения BIAevaluation (v3.0) с использованием модели двухвалентного аналита для расчета K A = k на / k на . Концентрации белка определяли аминокислотным анализом. Через 10 дней, когда опухолевые массы были в пределах 100–300 мг, 1–3 мкКи 131 I-меченые M5A, M5B или cT84.66 на животное вводили в хвостовую вену. В моменты времени 0, 6, 24, 48, 72 и 96 ч животных подвергали эвтаназии, проводили вскрытие, органы взвешивали и подсчитывали на радиоактивность. Все данные являются средними значениями и были скорректированы с учетом радиоактивного распада до момента инъекции, что позволяет сообщать о поглощении органами в процентах от введенной дозы на грамм (% ID г -1 ) со стандартными ошибками.
Через 10 дней, когда опухолевые массы были в пределах 100–300 мг, 1–3 мкКи 131 I-меченые M5A, M5B или cT84.66 на животное вводили в хвостовую вену. В моменты времени 0, 6, 24, 48, 72 и 96 ч животных подвергали эвтаназии, проводили вскрытие, органы взвешивали и подсчитывали на радиоактивность. Все данные являются средними значениями и были скорректированы с учетом радиоактивного распада до момента инъекции, что позволяет сообщать о поглощении органами в процентах от введенной дозы на грамм (% ID г -1 ) со стандартными ошибками. Седацию и визуализацию повторяли в дни 1, 2, 3, 6 и 7.
Седацию и визуализацию повторяли в дни 1, 2, 3, 6 и 7. 66 (в виде димера scFv) была предварительно определена с помощью рентгеноструктурного анализа с разрешением 2,6 Å (Carmichael, 2003). Доступность структурных данных значительно облегчила подход к гуманизации CDR-прививки. Обычно подходящие акцепторные последовательности VL и VH выбирают на основе поиска гомологии в базе данных последовательностей иммуноглобулинов Kabat (Johnson, 2001). В этом исследовании подходящая акцепторная структура была выбрана на основе поиска гомологов T84.66 в базе данных белков (Bernstein, 19).77) с использованием векторной программы структурного выравнивания (Gibrat, 1996). Это гарантировало, что родственная пара VL:VH будет выбрана с углом спаривания доменов, который соответствует углу спаривания T84.66, сохраняя относительную ориентацию петель CDR тяжелой и легкой цепей. Из антител, которые имели гомологичные структуры, гуманизированное антитело 4D5, версия 8 (анти-p185 HER2 , Герцептин, файл PDB 1FVC) (Eigenbrot, 1993) было выбрано в качестве наиболее подходящего поставщика каркаса.
66 (в виде димера scFv) была предварительно определена с помощью рентгеноструктурного анализа с разрешением 2,6 Å (Carmichael, 2003). Доступность структурных данных значительно облегчила подход к гуманизации CDR-прививки. Обычно подходящие акцепторные последовательности VL и VH выбирают на основе поиска гомологии в базе данных последовательностей иммуноглобулинов Kabat (Johnson, 2001). В этом исследовании подходящая акцепторная структура была выбрана на основе поиска гомологов T84.66 в базе данных белков (Bernstein, 19).77) с использованием векторной программы структурного выравнивания (Gibrat, 1996). Это гарантировало, что родственная пара VL:VH будет выбрана с углом спаривания доменов, который соответствует углу спаривания T84.66, сохраняя относительную ориентацию петель CDR тяжелой и легкой цепей. Из антител, которые имели гомологичные структуры, гуманизированное антитело 4D5, версия 8 (анти-p185 HER2 , Герцептин, файл PDB 1FVC) (Eigenbrot, 1993) было выбрано в качестве наиболее подходящего поставщика каркаса. Наложенные структуры показали высокую степень перекрытия со среднеквадратичным отклонением. 1,07 Å для 1326 атомов основной цепи. Кроме того, угол спаривания доменов VL-VH был практически одинаковым для обеих структур, как видно из двух ортогональных проекций на рис. 2.9.0419
Наложенные структуры показали высокую степень перекрытия со среднеквадратичным отклонением. 1,07 Å для 1326 атомов основной цепи. Кроме того, угол спаривания доменов VL-VH был практически одинаковым для обеих структур, как видно из двух ортогональных проекций на рис. 2.9.0419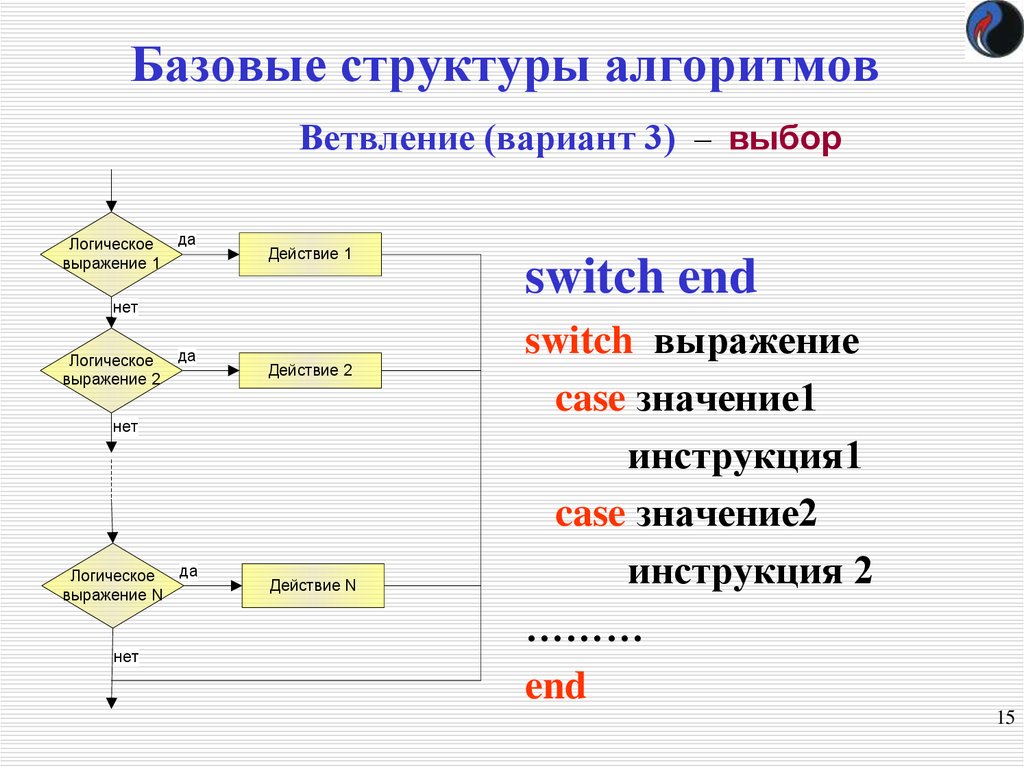 Однако было обнаружено, что петли CDR L1 и h4 являются структурно уникальными и, следовательно, требуют более тщательного изучения, чтобы определить, как сохраняются их необычные конформации. Петля CDR-L1 из 11 остатков напоминала каноническую петлю из 13 остатков, но удаление двух остатков с ее кончика вызвало непредвиденный поворот в этой области и нарушение сети водородных связей, которая стабилизирует остатки L30–L32. Структура петли CDR-h4 из 12 остатков также оказалась не такой, как предсказывалось на основе гомологичных структур, в основном из-за редкого остатка пролина, расположенного в каркасном положении H9.4. Пролин, лишенный амидного водорода, не может участвовать в сети водородных связей, которая обычно стабилизирует основание большинства петель h4 и в значительной степени определяет их конформацию (Morea, 1998). Чтобы компенсировать его неспособность образовывать водородные связи, боковая цепь пролина присоединяется к гидрофобному кластеру, образованному каркасными остатками h3 (val), h5 (leu) и h37 (phe), а также остатками CDR-h4 H99 (val) и h201 (tyr).
Однако было обнаружено, что петли CDR L1 и h4 являются структурно уникальными и, следовательно, требуют более тщательного изучения, чтобы определить, как сохраняются их необычные конформации. Петля CDR-L1 из 11 остатков напоминала каноническую петлю из 13 остатков, но удаление двух остатков с ее кончика вызвало непредвиденный поворот в этой области и нарушение сети водородных связей, которая стабилизирует остатки L30–L32. Структура петли CDR-h4 из 12 остатков также оказалась не такой, как предсказывалось на основе гомологичных структур, в основном из-за редкого остатка пролина, расположенного в каркасном положении H9.4. Пролин, лишенный амидного водорода, не может участвовать в сети водородных связей, которая обычно стабилизирует основание большинства петель h4 и в значительной степени определяет их конформацию (Morea, 1998). Чтобы компенсировать его неспособность образовывать водородные связи, боковая цепь пролина присоединяется к гидрофобному кластеру, образованному каркасными остатками h3 (val), h5 (leu) и h37 (phe), а также остатками CDR-h4 H99 (val) и h201 (tyr). , таким образом заставляя кончик петли CDR-h4 (H98-h200A) загибаться, а не вытягиваться к сайту объединения, как ожидается для петли такой длины. Поэтому мы постарались сохранить все эти уникальные структурные особенности при разработке гуманизированной версии T84.66.
, таким образом заставляя кончик петли CDR-h4 (H98-h200A) загибаться, а не вытягиваться к сайту объединения, как ожидается для петли такой длины. Поэтому мы постарались сохранить все эти уникальные структурные особенности при разработке гуманизированной версии T84.66. Было показано, что аланин H93 при обратной мутации в его мышиный аналог (серин) увеличивает сродство герцептина к антигену в 2 раза. Структурные последствия гуманизации каркасных остатков H71, H73 и H78 в нашей гибридной конструкции можно смело игнорировать, поскольку эти остатки одинаковы в донорных и акцепторных Fvs.
Было показано, что аланин H93 при обратной мутации в его мышиный аналог (серин) увеличивает сродство герцептина к антигену в 2 раза. Структурные последствия гуманизации каркасных остатков H71, H73 и H78 в нашей гибридной конструкции можно смело игнорировать, поскольку эти остатки одинаковы в донорных и акцепторных Fvs. При конструировании гибридной VH все три границы петель CDR были изменены. Определение по Кабату CDR-h2 (h41–h45) было расширено за счет включения h40, так как этот остаток упаковывается против кончика CDR-h3 в T84.66. Для CDR-h3 существует большое расхождение между определением Kabat, основанным на гипервариабельности последовательности (H50–H65), и определением Chothia, основанным на структурной изменчивости (H52–H56). Еще больше усложняет ситуацию то, что только остатки H50–H58 Kabat CDR-h3 взаимодействуют с антигеном в тех случаях, когда исследуются сокристаллы антитело-антиген (Padlan, 19).95; МакКаллум, 1996). Обратите внимание, однако, что два независимых отчета о гуманизации предполагают, что это не всегда так, поскольку неспособность сохранить мышиные остатки в положениях H59–H65 в гуманизированной конструкции снижала аффинность связывания более чем в 1000 раз в каждом случае (Eigenbrot, 1994; O' Коннор, 1998). По этой причине были разработаны две гуманизированные конструкции: T84.
При конструировании гибридной VH все три границы петель CDR были изменены. Определение по Кабату CDR-h2 (h41–h45) было расширено за счет включения h40, так как этот остаток упаковывается против кончика CDR-h3 в T84.66. Для CDR-h3 существует большое расхождение между определением Kabat, основанным на гипервариабельности последовательности (H50–H65), и определением Chothia, основанным на структурной изменчивости (H52–H56). Еще больше усложняет ситуацию то, что только остатки H50–H58 Kabat CDR-h3 взаимодействуют с антигеном в тех случаях, когда исследуются сокристаллы антитело-антиген (Padlan, 19).95; МакКаллум, 1996). Обратите внимание, однако, что два независимых отчета о гуманизации предполагают, что это не всегда так, поскольку неспособность сохранить мышиные остатки в положениях H59–H65 в гуманизированной конструкции снижала аффинность связывания более чем в 1000 раз в каждом случае (Eigenbrot, 1994; O' Коннор, 1998). По этой причине были разработаны две гуманизированные конструкции: T84.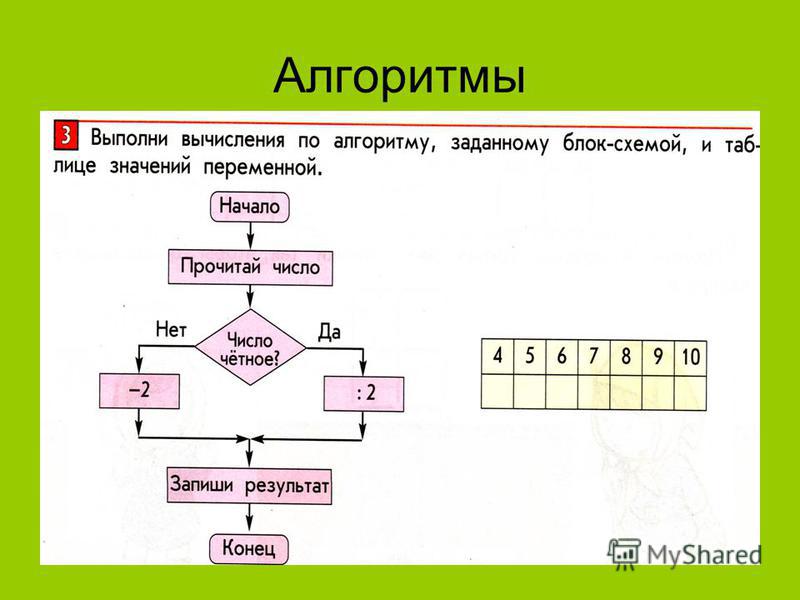 66 M5A, в которой остатки H59–H65 соответствуют последовательности акцептора человека (рис. 3a), и T84.66 M5B, в которой эти остатки соответствуют последовательности донора мыши (рис. 3b). Наконец, основываясь на наших знаниях о ключевой структурной роли, которую играет редкий пролин в положении H94 в T84.66 и важности H93 (Xiang, 1995), мы расширили определение CDR-h4 по Кабату, включив в него каркасные остатки H93 и H94. Стратегия трансплантации CDR показана путем выравнивания последовательностей на рисунке 4.
66 M5A, в которой остатки H59–H65 соответствуют последовательности акцептора человека (рис. 3a), и T84.66 M5B, в которой эти остатки соответствуют последовательности донора мыши (рис. 3b). Наконец, основываясь на наших знаниях о ключевой структурной роли, которую играет редкий пролин в положении H94 в T84.66 и важности H93 (Xiang, 1995), мы расширили определение CDR-h4 по Кабату, включив в него каркасные остатки H93 и H94. Стратегия трансплантации CDR показана путем выравнивания последовательностей на рисунке 4.
 Очистка с помощью протеина А и катионообменная хроматография с использованием стандартных условий привели к получению высокоочищенных антител. мАт М5А и М5В подвергали биохимической характеристике, при этом мАт cT84.66 служили контролем. Правильная сборка антител была подтверждена эксклюзионной хроматографией ВЭЖХ после очистки (фиг. 5, левая панель) и после радиоактивного йодирования (фиг. 5, правая панель). Гуманизированные mAb M5A и M5B имеют изоэлектрическую точку (стр. I ) в диапазоне 8,4, демонстрируя явную миграцию от исходного mAb T84.66 (p I 7,4) к более щелочному герцептину (p I > 9,0) (рис. 6). SPR-анализ с помощью BIAcore продемонстрировал субнаномолярное сродство к СЕА для mAb M5A, M5B и cT84,66 с K A = 1,1×10 10 M -1 , 1,9×10 12 -1 21 10 и 1,6×10 10 M -1 соответственно (таблица I).
Очистка с помощью протеина А и катионообменная хроматография с использованием стандартных условий привели к получению высокоочищенных антител. мАт М5А и М5В подвергали биохимической характеристике, при этом мАт cT84.66 служили контролем. Правильная сборка антител была подтверждена эксклюзионной хроматографией ВЭЖХ после очистки (фиг. 5, левая панель) и после радиоактивного йодирования (фиг. 5, правая панель). Гуманизированные mAb M5A и M5B имеют изоэлектрическую точку (стр. I ) в диапазоне 8,4, демонстрируя явную миграцию от исходного mAb T84.66 (p I 7,4) к более щелочному герцептину (p I > 9,0) (рис. 6). SPR-анализ с помощью BIAcore продемонстрировал субнаномолярное сродство к СЕА для mAb M5A, M5B и cT84,66 с K A = 1,1×10 10 M -1 , 1,9×10 12 -1 21 10 и 1,6×10 10 M -1 соответственно (таблица I). Аликвоты очищенных mAb M5A, M5B и cT84.66 анализировали с помощью эксклюзионной хроматографии ВЭЖХ после очистки на калиброванной колонке Superdex 200 HR10/30 (справа) и после радиоактивного иодирования на калиброванной колонке Superdex 60 HR10/30 (слева). Отображается поглощение при 280 нм (мАЕ) или радиоактивность в зависимости от времени (минуты).
Аликвоты очищенных mAb M5A, M5B и cT84.66 анализировали с помощью эксклюзионной хроматографии ВЭЖХ после очистки на калиброванной колонке Superdex 200 HR10/30 (справа) и после радиоактивного иодирования на калиброванной колонке Superdex 60 HR10/30 (слева). Отображается поглощение при 280 нм (мАЕ) или радиоактивность в зависимости от времени (минуты).



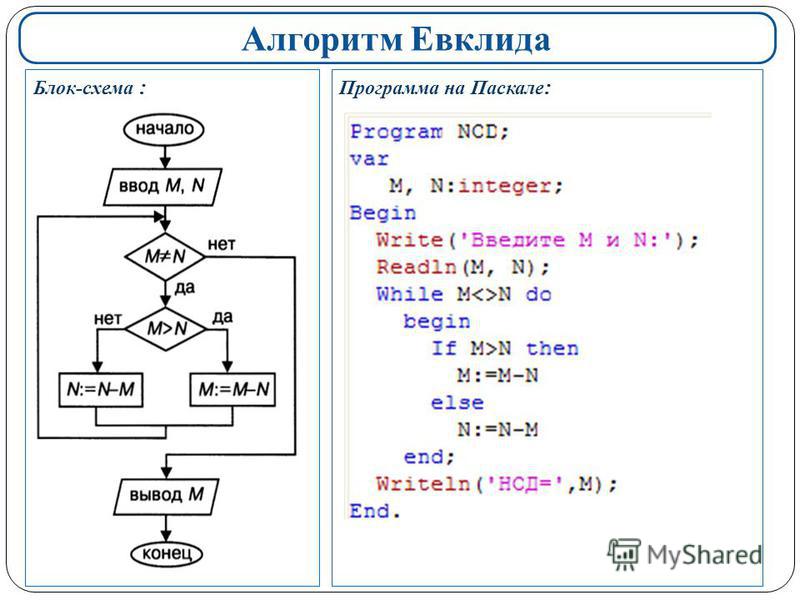 Результаты, представленные в Таблице II, показывают, что уровни поглощения mAb M5A статистически не отличались от уровней захвата cT84.66 в крови, опухоли или любых других органах. Точно так же mAb M5B в целом статистически не отличались от mAb cT84.66 в отношении поглощения кровью или любым другим нормальным органом. Однако M5B имел несколько более низкое поглощение опухолью (9).0437 p = 0,012), как показано на фигуре 7. При сопоставимой аффинности, клиренсе крови и 100% иммунореактивности после мечения растворимым антигеном in vitro (данные не показаны) было неясно, почему mAb M5B имело более низкое поглощение опухолью, чем M5A и может быть результатом экспериментальной вариации.
Результаты, представленные в Таблице II, показывают, что уровни поглощения mAb M5A статистически не отличались от уровней захвата cT84.66 в крови, опухоли или любых других органах. Точно так же mAb M5B в целом статистически не отличались от mAb cT84.66 в отношении поглощения кровью или любым другим нормальным органом. Однако M5B имел несколько более низкое поглощение опухолью (9).0437 p = 0,012), как показано на фигуре 7. При сопоставимой аффинности, клиренсе крови и 100% иммунореактивности после мечения растворимым антигеном in vitro (данные не показаны) было неясно, почему mAb M5B имело более низкое поглощение опухолью, чем M5A и может быть результатом экспериментальной вариации.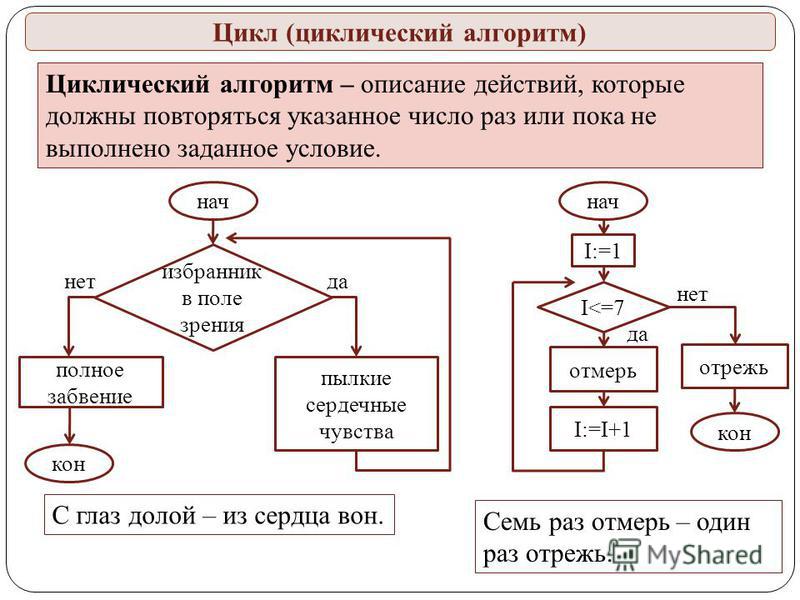 Поглощение опухолью (сплошные линии) и клиренс крови (пунктирные линии) измеряли в процентах от введенной дозы на грамм на 0, 6, 24, 48, 72 и 96 ч.
Поглощение опухолью (сплошные линии) и клиренс крови (пунктирные линии) измеряли в процентах от введенной дозы на грамм на 0, 6, 24, 48, 72 и 96 ч. 75 (1.36) a
75 (1.36) a  08 (3.75)
08 (3.75)  75 (0.11)
75 (0.11)  83)
83)  36 (0.18)
36 (0.18)  19 (0.72)
19 (0.72)  21)
21)  06 (0.33)
06 (0.33) 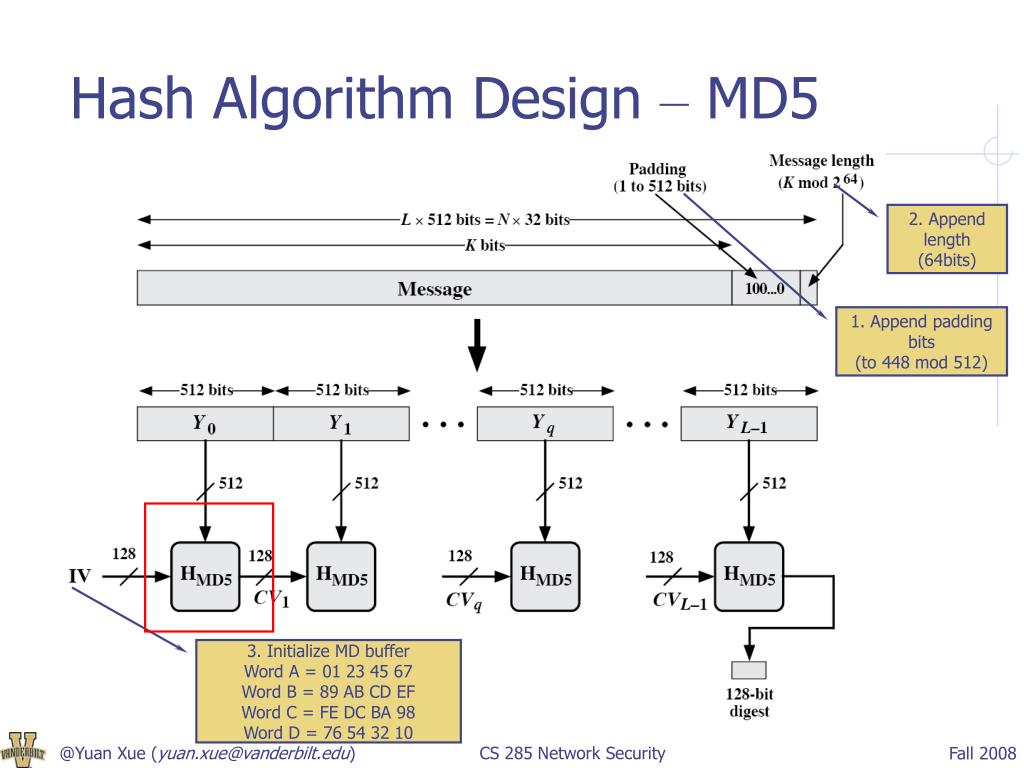 вводили отдельным группам бестимусных мышей с ксенотрансплантатами опухоли LS174T. В каждый момент времени для каждого mAb умерщвляли пять животных. Исследования биораспределения в тканях проводились на 0, 6, 24, 48, 72 и 96 ч.
вводили отдельным группам бестимусных мышей с ксенотрансплантатами опухоли LS174T. В каждый момент времени для каждого mAb умерщвляли пять животных. Исследования биораспределения в тканях проводились на 0, 6, 24, 48, 72 и 96 ч.
 05 (0.56)
05 (0.56)  37)
37) 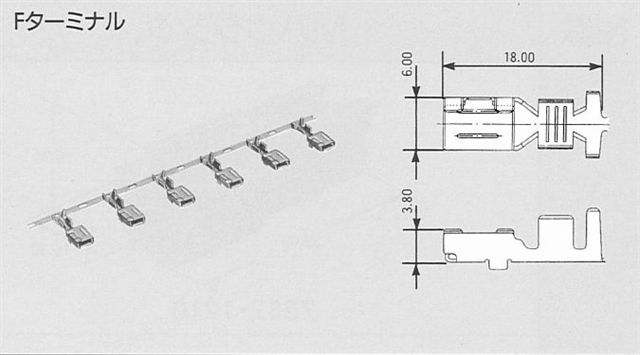 37 (1.00)
37 (1.00)  83 (4.84)
83 (4.84)  75 (1.36) a
75 (1.36) a  11 (0.94)
11 (0.94)  75 (0.11)
75 (0.11)  83)
83)  36 (0.18)
36 (0.18)  Часть урожая очищали, конъюгировали с макроциклом 1,4,7,10-тетраазациклододеканом 9.0437 N , N ′, N ″, N ″′-тетрауксусной кислоты (DOTA) (Lewis, 2001) и радиоактивно меченных 111 In. [ 111 In]DOTA-hT84.66 вводили внутривенно двум бестимусным мышам, несущим ксенотрансплантаты LS174T. Мышам ввели седацию и сделали снимки с помощью планарной сцинтиграфической камеры высокого разрешения. мАт hT84.66 продемонстрировали высокоспецифичную локализацию опухоли и удаление из нормальных тканей в течение 7 дней (фиг. 8). Эта комбинация данных свидетельствует о терапевтическом потенциале mAb hT84.66.
Часть урожая очищали, конъюгировали с макроциклом 1,4,7,10-тетраазациклододеканом 9.0437 N , N ′, N ″, N ″′-тетрауксусной кислоты (DOTA) (Lewis, 2001) и радиоактивно меченных 111 In. [ 111 In]DOTA-hT84.66 вводили внутривенно двум бестимусным мышам, несущим ксенотрансплантаты LS174T. Мышам ввели седацию и сделали снимки с помощью планарной сцинтиграфической камеры высокого разрешения. мАт hT84.66 продемонстрировали высокоспецифичную локализацию опухоли и удаление из нормальных тканей в течение 7 дней (фиг. 8). Эта комбинация данных свидетельствует о терапевтическом потенциале mAb hT84.66.
 Радиоактивно меченое hT84.66 mAb является многообещающим новым терапевтическим средством, которое может помочь в решении этой проблемы.
Радиоактивно меченое hT84.66 mAb является многообещающим новым терапевтическим средством, которое может помочь в решении этой проблемы.
 Дж. Иммунол.
Дж. Иммунол. Mol. биол.
Mol. биол.